Professional Documents
Culture Documents
Propiedades Fisicoquimicas Del Agua
Uploaded by
Leo OO0 ratings0% found this document useful (0 votes)
18 views54 pagesPROPIEDADES FISICOQUIMICAS DEL AGUA
Original Title
PROPIEDADES FISICOQUIMICAS DEL AGUA
Copyright
© © All Rights Reserved
Available Formats
PPTX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentPROPIEDADES FISICOQUIMICAS DEL AGUA
Copyright:
© All Rights Reserved
Available Formats
Download as PPTX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
18 views54 pagesPropiedades Fisicoquimicas Del Agua
Uploaded by
Leo OOPROPIEDADES FISICOQUIMICAS DEL AGUA
Copyright:
© All Rights Reserved
Available Formats
Download as PPTX, PDF, TXT or read online from Scribd
You are on page 1of 54
Universidad Alas Peruanas
ASIGNATURA:
QUÍMICA AMBIENTAL
TEMA: EL AGUA, PROPIEDADES
FISICOQUÍMICAS
Docente: Mg. Ing. Sonia M. Loayza Chácara
EL AGUA
Es el compuesto más abundante en la naturaleza. Es
el disolvente de muchas sustancias y por ello se le
llama “disolvente universal”.
• El agua es importante porque siendo el compuesto
mas abundante del protoplasma se le considera
indispensable en toda forma de vida.
• El agua es una molécula notable, fundamental para
la vida, solubiliza y modifica las propiedades de las
biomoléculas, como ácidos nucleicos, proteínas,
carbohidratos al formar enlaces de hidrógeno con
los grupos polares funcionales de dichas
biomoléculas.
Estructura del agua.-
La molécula del agua está constituida por dos
átomos de hidrógeno unidos por enlaces
covalentes a átomos de oxígeno
• En la molécula del agua el oxígeno posee 8
electrones de valencia, de los cuales dos pares
enlazantes y dos pares no enlazantes; la teoría de
repulsión de pares electrónicos del nivel de
valencia predice la forma de una molécula de
agua.
• La molécula del agua es una molécula polar que
presenta dos polos de carga negativa y positiva
que resulta de la diferente concentración de
electrones en el espacio.
Aquel sitio donde existe mayor concentración da
origen a un centro donde gravita carga negativa y
en el otro extremo gravita la carga positiva
• Cuando en una molécula existe un dipolo, esta
puede atraer a sus vecinas por fuerzas de
atracción entre cargas de diferente signo y eso
es lo que sucede en los enlaces puente
hidrógeno de las moléculas del agua
• Estas fuerzas se llaman dipolo-dipolo, las
cuales son importantes en sustancias al estado
líquido o sólido donde la cercanía molecular
es muy grande
• La polaridad de la molécula del agua, no solo
es consecuencia de su geometría molecular:
tetraédrica irregular, sino que también de la
naturaleza de sus átomos: El hidrógeno, el átomo
más pequeño de la química. El oxígeno, un átomo
pequeño pero de alta electronegatividad, esto hace
que en los enlaces de la molécula del agua atrae
hacia sí los electrones de los enlaces covalentes con
el H, hecho que da lugar a la polaridad del enlace
PROPIEDADES FISICOQUÍMICAS DEL AGUA.-
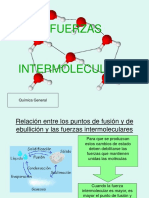
Casi todas las propiedades físicas del agua se
deben a la existencia del puente hidrógeno en el
estado sólido y líquido y estas son:
1) Enlace puente hidrógeno.- La atracción
dipolo-dipolo, que es inusualmente fuerte y
en la que participa el átomo de hidrógeno, se
denomina “enlace puente hidrógeno”
se deduce que las atracciones dipolo-dipolo
entre las moléculas del agua son importantes,
en realidad muy fuertes.
Si el agua no tuviera la capacidad de formar
enlaces hidrógeno, sería un gas a temperatura
ambiente.
2) Acción disolvente. El agua es el líquido que
más sustancias disuelve (disolvente universal),
esta propiedad se debe a su capacidad para
formar puentes de hidrógeno con otras
sustancias, ya que estas se disuelven cuando
interaccionan con las moléculas polares del
agua.
La capacidad disolvente es la responsable de dos
funciones importantes para los seres vivos: a) Es el
medio en que transcurren la mayoría de las
reacciones del metabolismo, y
b) el otro es el aporte de nutrientes y la
eliminación de desechos que se realizan a través
de sistemas de transporte acuosos.
3.- Tensión superficial.- es la resistencia que
ofrece un líquido para aumentar su superficie. Por
lo que es necesaria una cantidad de energía para
estirar la superficie de un líquido por unidad de
área.
La tensión superficial también se define como la
fuerza elástica que hay en la superficie de un
líquido
En cambio, las moléculas que se encuentran en la
superficie, solo son atraídas hacia abajo o hacia el
lado por otras moléculas, provocando que la
superficie se tense como una capa elástica.
La tensión superficial se manifiesta en el fenómeno
de capilaridad que permite la ascensión de la savia
en los vegetales. La tensión superficial del agua,
hace que esta película se contraiga y jale hacia la
parte superior del tubo.
La capilaridad, es el resultado de dos tipos de
fuerzas:
Fuerzas de Cohesión, atracción intermolecular entre
moléculas semejantes (en este caso moléculas del
agua).
Fuerzas de adhesión, atracción entre moléculas
distintas (como las del agua y el vidrio) elástica.
Fuerza de cohesión entre sus moléculas. Los
puentes de hidrógeno mantienen a las
moléculas fuertemente unidas, formando una
estructura compacta que la convierte en un
líquido casi incompresible.
Elevada fuerza de adhesión.- De nuevo los
puentes de hidrógeno del agua son los
responsables, al establecerse entre estos y otras
moléculas polares, y es responsable, junto con la
cohesión de la capilaridad, al cual se debe, en
parte, la ascensión de la sabia bruta desde las
raíces hasta las hojas.
4. Densidad.- La máxima densidad del agua está a
4ºC, es decir al estado líquido (D=0.99995 g/mL) y
a 0ºC, al estado sólido es menor (D=0.917 g/mL).
• Para entender esta propiedad, supongamos que
tenemos una masa de hielo, que por efecto del
calor externo el hielo comienza a fundirse.
• En esta transformación un número
relativamente pequeño de moléculas adquieren
energía cinética suficiente como para romper
sus enlaces hidrógeno.
• Estas moléculas se liberan de la red cristalina
que comienza a desmoronarse y quedan
ocupando los huecos hexagonales que
forman canales , con lo cual comienza a
aumentar la masa por unidad de volumen
• A medida que crece la energía externa,
aumenta la densidad del agua líquida, porque
se ocupa mas espacios vacíos hasta llegar al
máximo de 4ºC.
• Esta es la razón por la cual el hielo es menos
denso que el agua y por tanto flota sobre ella.
• Entre 0 y 4ºC, la densidad del agua líquida
aumenta, porque predomina la ocupación de
huecos hexagonales y el agua se torna mas
densa
• Sobre los 4ºC, la densidad del líquido
disminuye, porque predomina la expansión
térmica.
Las variaciones de la densidad del agua con la
temperatura tienen una profunda repercusión
en el ambiente:
• En cuerpos de agua como un lago, el agua a
4ºC que es mas densa se sumerge hacia el
fondo, mientras que el agua sobre los 4ºC,
menos densa sube a la parte superior
• Este desplazamiento de agua por convección,
produce que casi la totalidad del cuerpo de
agua alcance los 4ºC.
• Bajo esta temperatura , la densidad
disminuye, pero como el agua no es mas
pesada que la que esta a 4ºc, no se desplaza
hacia el fondo, sino que permanece en la
superficie, hasta que a 0ºc se congela.
• La capa de hielo que se forma, que es menos
densa no se sumerge y como que da sobre la
superficie del cuerpo de agua forma una capa
aislante que evita que el agua del interior se
congele.
• Si el hielo llegara al fondo, no podría aislar el
interior del frío ambiental, por lo que todo se
congelaría y los peces y otros organismos
vivos morirían.
4) Gran calor específico.- El calor específico de
una sustancia, es la cantidad de calor que
requiere para elevar 1ºC la temperatura de 1 g
de agua. El calor específico del agua es 4.184
J/g.ºC, implica que necesita una gran cantidad
de calor para calentar 1 g de agua
• El agua absorbe grandes cantidades de calor
que utiliza en romper los puentes de
hidrógeno.
• En el estado líquido y en el estado sólido, las
moléculas de agua están atraídas por enlaces
hidrógeno y requieren energía para romper
dichos enlaces, con lo cual las moléculas se
Moléculas se mueven más rápido
• A 100ºC todavía hay un gran número grande de
enlaces de hidrógeno sin romper, para
vaporizar 1 mol de agua, se necesita cerca de 4
veces, mas calor que lo esperado de no haber
dicho enlace. Esta explica porque la
temperatura de ebullición es de 100ºC.
• En invierno los cuerpos de agua desprenden
calor (lo absorbido en verano), con lo que la
temperatura del agua baja levemente y en el
ambiente hay menos frío
El alto calor específico del agua ayuda a templar
la temperatura ambiente.
El fenómeno del niño, es una corriente de aguas
cálidas que recorre la región sur oeste del océano
pacífico, llegando parte de esta a las costas del
Ecuador, Perú, parte de Chile en donde las aguas
aumentan la temperatura desde 14º a 15ºC,
propia de años normales y de 17 a 18ºC en años
anormales.
5) Elevado calor de vaporización.- A 20°C se
precisan 540 calorías para evaporar un gramo de
agua, lo que da idea de la energía necesaria para
romper los puentes de hidrógeno establecidos
entre las moléculas del agua
líquida y, posteriormente, para dotar a estas
moléculas de la energía cinética suficiente para
abandonar la fase líquida y pasar al estado de
vapor.
6) Elevada constante dieléctrica.-
Por tener moléculas dipolares, el agua es un
gran medio disolvente de compuestos iónicos,
como las sales minerales, y de compuestos
covalentes polares como los glúcidos
PROPIEDADES BIOQUÍMICAS DEL AGUA
Los seres vivos se han adaptado para utilizar
químicamente el agua en dos tipos de
reacciones:
a) En la fotosíntesis en la que los enzimas
utilizan el agua como fuente de átomos de
hidrógeno.
b) En las reacciones de hidrólisis, en que las
enzimas hidrolíticas han explotado la capacidad
del agua para romper determinados enlaces
hasta degradar los compuestos orgánicos en
otros más simples, durante los procesos
digestivos.
IONIZACIÓN DEL AGUA Y ESCALA DE pH
Si observamos la figura siguiente,
comprobarás que dos moléculas
polares de agua pueden
Ionizarse debido a las fuerzas
de atracción por puentes de
hidrogeno que se establecen entre ellas
Un ión hidrógeno se disocia de su átomo de
oxígeno de la molécula (unidos por enlace
covalente), y pasa a unirse con el átomo de
oxígeno de la otra molécula, con el que ya
mantenía relaciones mediante el enlace de
hidrógeno.
Como vemos, el agua no es un líquido
químicamente puro, ya que se trata de una
solución iónica que siempre contiene algunos
iones H3O + y OH- . (Se utiliza el símbolo H+, en
lugar de H3O+).
El producto [H+]·[OH -]= 10 -14, se denomina
producto iónico del agua, y constituye la base
para establecer la escala de pH, que mide la
acidez o alcalinidad de una disolución acuosa ,
es decir, su concentración de iones [H +] o [OH-]
respectivamente.
pH.- el pH, es la medida de la concentración de
iones hidrógeno en cualquier sustancia:
pH=-log[H +]
pOH = -log [OH- ]
14 = pH + pOH
El pH del agua es 7 y lo consideramos neutro.
Valores mayores serán básicos o alcalinos y
valores menores ácidos.
ESCALA DEL pH.-
Concenc H+ pH
(mol/L)
EL pH Y LOS SISTEMAS BUFFER
AMORTIGUADORES O TAMPOS EN LOS SISTEMAS
BIOLOGICOS
En los organismos vivos se producen
continuamente ácidos orgánicos que son
productos finales de reacciones metabólicas,
catabolismo de proteínas y otras moléculas
biológicamente activas. Mantener el pH en los
fluidos intra y extracelulares es fundamental
puesto que ello influye en la actividad biológica
de las proteínas, enzimas, hormonas, la
distribución de iones a través de membranas, etc.
• El pH de los medios biológicos es una
constante fundamental para el mantenimiento
de los procesos vitales.
• La acción enzimática y las transformaciones
químicas de las células se realizan dentro de
unos estrictos márgenes de pH .
• En humanos los valores extremos compatibles
con la vida y con el mantenimiento de
funciones vitales oscilan entre 6,8 y 7,8;
siendo el estrecho margen de 7,35 a 7,45 el de
normalidad.
• Ecuación de Henderson-Hasselbalch.
Concepto de pK
La concentración de H+ está vinculada a la
naturaleza del electrolito débil. Considerando un
ácido débil, de modo genérico como HAc, su
equilibrio de disociación sería:
HAc <--------------------> Ac- + H+
• Aplicando la ley de acción de masas, la
constante de equilibrio K será:
K = ( Ac- ) x ( H+ ) / (HAc )
Realizando las operaciones correspondientes en
la ecuación, despejando H + y aplicando logaritmo
llegamos a:
log ( H+ ) = log K + log (HAc ) - log ( Ac- )
multiplicando por -1 a la educación anterior:
-log ( H+ ) = pH
-log K = pK
Así se obtiene la ecuación de Henderson-
Hasselbalch.
pH = pK + log ( base ) / ( ácido )
• Si en la ecuación la concentración de ácido es
igual a la de la base, el cociente es 1, siendo el
log de 1 = 0, se tiene que
pH = pK
por tanto, se puede definir el pK como el valor de
pH de una solución amortiguadora en el que el
ácido y la base se encuentran a concentraciones
equimoleculares o al 50% cada una.
La manera en que podemos regular el pH dentro
de los límites compatibles con la vida son:
1) Los tampones fisiológicos
2) La eliminación de ácidos y bases por
compensación respiratoria y renal.
Las soluciones de ácidos débiles y sus bases
conjugados (o sus bases débiles y sus ácidos
conjugados) tienen capacidad amortiguador
Capacidad amortiguadora.- la tendencia de una
solución a resistir de manera eficaz que un
volumen igual de agua, un cambio en el pH
después de una adición de un ácido o una base
fuertes.
En el caso del suelo, se denomina poder
amortiguador, a la resistencia que presenta a
modificar su pH cuando se le añaden ácidos o
bases. Esta propiedad es de gran importancia, ya
que permite mantener el pH dentro de limites
muy estrechos, evitando modificaciones
radicales en el ambiente del suelo que podrían
afectar desfavorablemente a las plantas
superiores, microorganismos y, sobre todo, al
aprovechamiento de los elementos nutrientes.
Tampones fisiológicos
Son sistemas encargados de mantener el pH de
los medios biológicos dentro de los valores
compatibles con la vida.
Los tampones fisiológicos son la primera línea de
defensa frente a los cambios de pH de los líquidos
corporales, entre los que destacan: el tampón
fosfato, el tampón bicarbonato y el tampón
hemoglobina.
Permitiendo con ello la realización de funciones
bioquímicas y fisiológicas de las células, tejidos,
órganos, aparatos y sistemas.
Según su naturaleza química, los amortiguadores
se clasifican en orgánicos e inorgánicos y, así
mismo, atendiendo a su ubicación, se distribuyen
en plasmáticos y tisulares.
Tampones orgánicos.-
a) Las proteínas y aminoácidos como tampón
• Los aminoácidos y proteínas son electrolitos
anfóteros, es decir, pueden tanto ceder
protones (ácidos) como captarlos (bases) y, a
un determinado pH tener ambos
comportamientos al mismo tiempo.
La carga depende del pH del medio. En un
medio muy básico se cargan negativamente,
mientras que en el fuertemente ácido lo hacen
positivamente. Resulta de especial interés a
nivel tisular.
b) Tampón hemoglobina
Es un tampón fisiológico muy eficiente debido
tanto al cambio de pK que experimenta al pasar
de la forma oxidada a la reducida, como a la
gran abundancia de esta proteína en la sangre
(15 % del volumen total sanguíneo).
• La oxihemoglobina (pK= 7,16) es un ácido más
fuerte que la desoxihemoglobina (pK= 7,71).
Los valores de pK son tales que determinan
que en la disociación siguiente, el valor x sea,
aproximadamente, 0,7.
HbH+x + O2 → HbO2 + xH+
Esta propiedad de la hemoglobina, de cambiar
su valor de pK, demuestra el efecto tampón,
permite el transporte de una determinada
cantidad de CO2 liberada en los tejidos
Tampones inorgánicos
a) Tampón carbónico/bicarbonato
Está constituido por H2CO3 y HCO3-. Aunque su
valor de pK (6,1) está algo alejado del pH
fisiológico de la sangre (7,4), es un sistema muy
eficaz debido a que:
1) La relación HCO3-/ H2CO3 es muy alta (20/1), lo
que le proporciona una alta capacidad tampón
frente a los ácidos
2) Es un sistema abierto, con lo que el exceso de
CO2 puede ser eliminado por ventilación
pulmonar de manera rápida; y
3) Además, el HCO3- puede ser eliminado por los
riñones mediante un sistema de intercambio
con solutos.
• Respecto al origen y formación de este
sistema carbónico/bicarbonato, resaltaremos
lo siguiente:
• En el plasma el CO2, procedente del
metabolismo celular, se encuentra como:
• -CO2 disuelto, que según la ley de Henry es
directamente proporcional a la presión parcial
del gas (PCO2)
• -HCO3-, que es la fracción más importante, y
Formando compuestos carbamínicos con los
grupos NH2 de la hemoglobina. Alrededor del
10% es transportado en el eritrocito en forma
de carbaminohemoglobina
• Tampón fosfato
• A pH fisiológico, las especies del fosfato con
capacidad de tamponar son H2PO4- y HPO42- ya
que su valor de pK es de 6,8. Así pues, para el
tampón fosfato:
• pH = 6,8 + log HPO42- / H2PO4-
A pH fisiológico de 7,4, la concentración de
HPO42- (un 80%) es 4 veces superior a la de
H2PO4- (un 20%). Así pues, el tampón fosfato es
un sistema muy eficaz para amortiguar ácidos.
La concentración de fosfato en la sangre es baja
(2 mEq/L) por lo que tiene escasa capacidad de
tamponar si lo comparamos con otros tampones
(ej el bicarbonato). En cambio, a nivel
intracelular, las concentraciones de fosfato son
elevadas lo que le convierte en un tampón
eficiente.
Las grandes cantidades de fosfato dentro de las
células corporales y en el hueso hacen que el
fosfato sea un depósito grande y eficaz para
amortiguar el pH.
You might also like
- Química General Ing Civil S4Document54 pagesQuímica General Ing Civil S4Wilson Irigoin BustamanteNo ratings yet
- Pharmaceutics 10 00074.en - EsDocument33 pagesPharmaceutics 10 00074.en - Esmaria fernandaNo ratings yet
- Leord Perez Herrera Practica Computacion 21.06.2022Document9 pagesLeord Perez Herrera Practica Computacion 21.06.2022Leo OONo ratings yet
- Qué Es La Sucesión EcológicaDocument5 pagesQué Es La Sucesión EcológicaLeo OONo ratings yet
- Acta de Socializacion de La Problemática A Partir de Los ResultadosDocument1 pageActa de Socializacion de La Problemática A Partir de Los ResultadosLeo OONo ratings yet
- Evaluacion Practico de WordDocument9 pagesEvaluacion Practico de WordLeo OONo ratings yet
- Confirmacion de Reserva14095530047341Document2 pagesConfirmacion de Reserva14095530047341Leo OONo ratings yet
- EXPODocument3 pagesEXPOLeo OONo ratings yet
- Tratabajo LeopoldDocument4 pagesTratabajo LeopoldLeo OONo ratings yet
- Tablas LeordDocument3 pagesTablas LeordLeo OONo ratings yet
- Trabajo Leord Perez HerreraDocument3 pagesTrabajo Leord Perez HerreraLeo OONo ratings yet
- TransgénesisDocument10 pagesTransgénesisLeo OONo ratings yet
- Ethy Trabajo Monografico MineriaDocument23 pagesEthy Trabajo Monografico MineriaLeo OONo ratings yet
- Gobierno Del PerúDocument2 pagesGobierno Del PerúLeo OONo ratings yet
- EtrategasDocument8 pagesEtrategasLeo OONo ratings yet
- Introduccion Biorremediacion - 3 ClaseDocument66 pagesIntroduccion Biorremediacion - 3 ClaseLeo OONo ratings yet
- Grupo 1 - ValoraciónDocument23 pagesGrupo 1 - ValoraciónLeo OONo ratings yet
- Acfrogclf3gulro0ljn5ry4i 3z-Pdzlvlp2evx1j7luagdd9s7maiflouw Bi8dpupyxpjamxwoab6qdheitmyxacewmpxfctxivwlbzguqvwbirs4hqsa57ocvrb0u9k-Xp4f441qi 8nd9qtDocument5 pagesAcfrogclf3gulro0ljn5ry4i 3z-Pdzlvlp2evx1j7luagdd9s7maiflouw Bi8dpupyxpjamxwoab6qdheitmyxacewmpxfctxivwlbzguqvwbirs4hqsa57ocvrb0u9k-Xp4f441qi 8nd9qtLeo OONo ratings yet
- Tomo 6: Analisis de Estudios de Impacto Ambiental - Ard SchoemakerDocument58 pagesTomo 6: Analisis de Estudios de Impacto Ambiental - Ard SchoemakerardNo ratings yet
- Leord Perez ConductorDocument2 pagesLeord Perez ConductorLeo OONo ratings yet
- Numeros Bienestar SocialDocument1 pageNumeros Bienestar SocialLeo OONo ratings yet
- Cvleord PDFDocument4 pagesCvleord PDFLeo OONo ratings yet
- Gobierno Del PerúDocument2 pagesGobierno Del PerúLeo OONo ratings yet
- Covid 19 Benef Canasta PDFDocument743 pagesCovid 19 Benef Canasta PDFLeo OONo ratings yet
- Ba 002 Cas Anina 2020Document10 pagesBa 002 Cas Anina 2020Leo OONo ratings yet
- AB980 - Estatuto de La UTEA (Vigente)Document132 pagesAB980 - Estatuto de La UTEA (Vigente)Leo OONo ratings yet
- Exa CuencasDocument2 pagesExa CuencasLeo OONo ratings yet
- Reglamento Utea PDFDocument32 pagesReglamento Utea PDFcristian echevarriaNo ratings yet
- SuelosssssssssDocument5 pagesSuelosssssssssLeo OONo ratings yet
- Articulo EpiDocument7 pagesArticulo EpiLeo OONo ratings yet
- SuelosssssssssDocument5 pagesSuelosssssssssLeo OONo ratings yet
- Ley Universitaria 30220 - 2014Document21 pagesLey Universitaria 30220 - 2014uveruverNo ratings yet
- Informe Determinacion Del Punto de EbullicionDocument9 pagesInforme Determinacion Del Punto de EbullicionMiguel RodriguesNo ratings yet
- CapilaridadDocument2 pagesCapilaridadjulissa CadenaNo ratings yet
- Cuestionario de Quimica OrganicaDocument2 pagesCuestionario de Quimica OrganicaJhoany SanchezNo ratings yet
- Q 5ºaño - S3 - TEORÍA DEL ENLACE COVALENTE Y FUERZAS INTERMOLECULARES PDFDocument5 pagesQ 5ºaño - S3 - TEORÍA DEL ENLACE COVALENTE Y FUERZAS INTERMOLECULARES PDFdavidNo ratings yet
- Práctica 4 Fuerzas IntermolecularesDocument2 pagesPráctica 4 Fuerzas IntermolecularesNicolás Grinberg100% (1)
- Propiedades de Los Cuerpos SólidosDocument14 pagesPropiedades de Los Cuerpos SólidosCurieNo ratings yet
- 5 Ficha 5 (T) SolidosDocument4 pages5 Ficha 5 (T) SolidosHappinessNo ratings yet
- Programa Quimica InorganicaDocument6 pagesPrograma Quimica InorganicaMartha leonNo ratings yet
- Fuerzas IntermolecularesDocument2 pagesFuerzas IntermolecularesEstefany TexeiraNo ratings yet
- QUIMICA MEDICA UNIDAD I Tabla Periodica Enlaces Geometria Molecular 2017 IIDocument84 pagesQUIMICA MEDICA UNIDAD I Tabla Periodica Enlaces Geometria Molecular 2017 IIArni Paul Marreros SorianoNo ratings yet
- Química General - Propiedades de la materiaDocument4 pagesQuímica General - Propiedades de la materiajoimir rafael perezNo ratings yet
- Fuerzas IntermolecularesDocument3 pagesFuerzas IntermolecularesVeronica DaniellsNo ratings yet
- Caso de Práctica Fuerzas IntermolecularesDocument2 pagesCaso de Práctica Fuerzas IntermolecularesBruce Jean Paul Mori MenesesNo ratings yet
- Análisis de grupos funcionales orgánicosDocument8 pagesAnálisis de grupos funcionales orgánicosAndres LozanoNo ratings yet
- Fuerzas intermoleculares y estados materiaDocument7 pagesFuerzas intermoleculares y estados materiaSantiago ValenciaNo ratings yet
- Estado de Agregacion de La Materia. Y PETROLEO.Document12 pagesEstado de Agregacion de La Materia. Y PETROLEO.Jose Pepe QmaNo ratings yet
- Práctica 1Document16 pagesPráctica 1Juan Diego Cabrera AbadNo ratings yet
- Quimica Dif Presentacion Fuerzas IntermolecularesDocument15 pagesQuimica Dif Presentacion Fuerzas IntermolecularesTony LedesmaNo ratings yet
- Ciencias Naturales 1Document59 pagesCiencias Naturales 1ErickAguilarAltamiranoNo ratings yet
- Capilaridad y Termodinámica de SuperficiesDocument39 pagesCapilaridad y Termodinámica de SuperficiesJulio Camel0% (1)
- Cta3 U3Document5 pagesCta3 U3ulises salasNo ratings yet
- Sesion S05 - Tercera Ley de La TermodinámicaDocument16 pagesSesion S05 - Tercera Ley de La TermodinámicaManuel Sebastian Laura MamaniNo ratings yet
- CT Quim GenDocument15 pagesCT Quim GenJavier AlejandroNo ratings yet
- Resumen de Biologia Capitulo 1 y 2 PDFDocument60 pagesResumen de Biologia Capitulo 1 y 2 PDFZekeNo ratings yet
- CROMATOGRAFIADocument43 pagesCROMATOGRAFIAEmma Romero100% (2)
- 9 Na Clase Comportamiento de Las Particulas Solidas 2014 2Document79 pages9 Na Clase Comportamiento de Las Particulas Solidas 2014 2Rosa Milagros Roca CoronelNo ratings yet
- Discusión de Resultados Fuerzas InterDocument4 pagesDiscusión de Resultados Fuerzas InterAndrea GirónNo ratings yet
- Clase 2 FarmacoquimicaDocument25 pagesClase 2 Farmacoquimicajanet huanca choqueNo ratings yet