Professional Documents
Culture Documents
Determinacion Proteínas
Uploaded by
Felipe0 ratings0% found this document useful (0 votes)
501 views4 pagesCopyright
© Attribution Non-Commercial (BY-NC)
Available Formats
DOC, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Attribution Non-Commercial (BY-NC)
Available Formats
Download as DOC, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
501 views4 pagesDeterminacion Proteínas
Uploaded by
FelipeCopyright:
Attribution Non-Commercial (BY-NC)
Available Formats
Download as DOC, PDF, TXT or read online from Scribd
You are on page 1of 4
DETERMINACIÓN CUANTITATIVA DE PROTEÍNAS
MUÑOZ, James; PAZ Claudia; VIDAL, Iván F.
Universidad del Cauca, Departamento de Química, Laboratorio de Bioquímica
Popayán, Colombia
OBJETIVOS METODOLOGIA
Determinar la concentración de proteína Se prepararon 7 soluciones diluidas de
(albúmina bovina) mediante el método de concentración 2, 4, 6, 8, 10, 12, 14 ppm a
Lowry. partir de 100 mL de una solución de 30
ppm. Seguidamente se realizó el método de
Determinar la concentración de 3 muestras Lowry (ver Figura 1).
problema a partir la construcción de una
curva de calibración.
Figura 1. Diagrama de flujo.
RESULTADOS
Cuadro 1. Registro del valor de absorbancia para las muestras de trabajo.
Valor de la absorbancia
Concentración (ppm)
observada (750 nm)
Blanco 0.26
2 0.38
4 0.56
6 0.4
8 0.41
10 0.52
12 0.41
14 0.56
MP1 0.7
MP2 0.66
MP3 0.7
Datos en rojo: datos descartados.
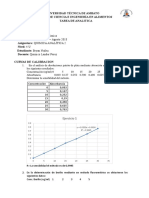
Figura 2. Curva calibración Proteína para 5 datos. Absorbancia-Concentración (ppm).
Tabla1. Datos obtenidos curva de calibración Proteína.
x y r b a sb sa
-5
8. 0.19 0.916 0.016 0.06 1.725x10 1.38x10-3
0 4 7 5 2
Significancia de la correlación. Limites de confianza de la pendiente
Ho: r =0 (b) y la ordenada (a).
Para t(n-2) grados de libertad, y un nivel
r n −2 0.9167 5 −2 de confianza del 95%.
t= t= = 3.97
1−r2 1 − 0.9167 2
b ± t ( n −2 ) s b
t(calculado)>t(tabulado); 0.0165 ±(3.18 )(1.725 x10 −5 )
3.97>3.18 para un contraste t de dos colas, = 0.0165 ±5.4855 x10 −5
t(n-2) grados de libertad, y un nivel de
confianza del 95%. Se rechaza Ho. Existe a ± t ( n −2 ) s a
correlación significativa. 0.062 ±(3.18 )(1.38 x10 −3 )
= 0.062 ±4.3884 x10 −3
Cuadro 2. Concentración calculada para las muestras problema.
Concentración
Muestra Absorbancia
calculada (ppm)
Muestra problema 1 0.44 22.9
Muestra problema 2 0.4 20.48
Muestra problema 3 0.44 22.9
Error aleatorio de las concentraciones debido a que el posterior cálculo de las
calculadas (Sxo). concentraciones de las soluciones
∑( y i − yˆi ) 2 = 0,02088468 problema presenta un error aleatorio muy
alto lo que a su vez genera un límite de
confianza muy amplio (88.5% para MP1 y
Sy =
∑ (y i − yˆ ) 2 MP3, 98.97% para MP2) por encima y por
x n−2 debajo de la concentración obtenida,
generando que estas concentraciones
0,02088468 obtenidas no sean confiables.
Sy = = 0.0834335 La tendencia no lineal de la curva es
x 5−2 debida a la precipitación de la proteína, la
cual fue diferente en cada muestra,
∑( x i − x ) 2 = 400 causando lecturas variables de la
absorbancia.
Sy
1 ( y − y) 2
Sx o = x
1+ + 2 o Análisis método de Lowry. El fundamento
b n b ∑ ( xi − x ) 2 del método de Lowry para cuantificación
de proteínas esta basado en la interacción
Sx o = 6,3756439 de las proteínas con el reactivo de Folin
(tungstato, molibdato y fosfato) en medio
alcalino (pH 10-10.5) y con Cu 2+. Es una
Límite de confianza de las valoración colorimétrica cuantitativa de las
concentraciones calculadas (xo). proteínas, siendo la intensidad de color
Para t(n-2) grados de libertad, y un nivel de proporcional a la concentración de
confianza del 95%. proteínas. Este método consta de dos
etapas:
x o ± t ( n −2 ) Sx o En la primera los iones Cu2+, en medio
alcalino, se unen a las proteínas formando
22 .9 ± (3.18 )6,375 = 22 .9 ± 20 .27
complejos con los átomos de nitrógeno de
20 .48 ± (3.18 )6.375 = 20 .48 ± 20 .27
los enlaces peptídicos. Estos complejos
22 .9 ± (3.18 )6,375 = 22 .9 ± 20 .27
Cu2+-proteína tienen un color azul claro.
Además, provocan el desdoblamiento de la
estructura tridimensional de la proteína,
ANALISIS DE RESULTADOS exponiéndose los residuos fenólicos de
tirosina que van a participar en la segunda
Análisis curva de calibración Proteína. Al etapa de la reacción. El Cu2+ se mantiene
observar la tendencia de los puntos sobre la en solución alcalina en forma de su
curva de calibración fácilmente se puede complejo con tartrato.
concluir que no existe una tendencia lineal. En la segunda parte se da la reducción,
Sin embargo al aplicar la estadística del también en medio básico, del reactivo de
caso se tiene que: el coeficiente de Folin-Ciocalteau, por los grupos fenólicos
correlación para los todos los datos es muy de los residuos de tirosina, presentes en la
inferior (r=0.3465) al aceptado (>0.95), mayoría de las proteínas, actuando el cobre
por lo que se excluyen 2 datos (los más como catalizador. El principal
alejados del intervalo según prueba Q), constituyente del reactivo de Folin-
para obtener un r=0.9167 el cual sigue Ciocalteau es el ácido
estando muy alejado del aceptado, pero fosfomolibdotúngstico, de color amarillo,
que sin embargo presenta correlación que al ser reducido por los grupos
significativa. Aunque el número de datos fenólicos da lugar a un complejo de color
escogido (n=5) presente significacia azul intenso.
correlativa, no es una significancia ideal
Cuando el reactivo de Folin es adicionado necesarios para que la movilidad de la
a la proteína tratada con Cu2+ el máximo proteína en una electroforesis SDS-PAGE
color se da si la reducción ocurre alrededor sea acorde con su masa molecular.
de un pH 10. En este punto el reactivo, La eficiencia del DTT como reductor de
solo esta reactivo por un corto periodo de puentes disulfuro que se ubican
tiempo. generalmente en el interior de la proteína,
Posibles explicaciones de la precipitación se debe a su estructura química que le
de la proteína para nuestro caso pueden ser permite formar un anillo de seis átomos al
que no se dio la reacción previa de la oxidarse.
proteína en medio alcalino con iones Cu2+,
en presencia de tartrato, lo que permite la
precipitación de la misma. Entre otras se CONCLUSIONES
pudo presentar un rearreglo en la reducción
primaria del producto por lo que el No fue posible demostrar la efectividad del
espectro de absorción cambia de forma método de Lowry para la cuantificación de
entre 3-30 minutos. Además durante el proteína de albúmina bobina, debido a que
primer minuto o más después de la adición al adicionar el reactivo de Folin a los pocos
del reactivo de Folin, éste libera ácido minutos la proteína se precipitó, muy
extra, lo cual podría ser resultado de la posiblemente a que el buffer no pudo
disociación del fosfomolibdato, generando amortiguar un exceso de ácido generado en
que el buffer no pueda cumplir su función la disociación del fosfomolibdato.
y se sobrepase el punto isoelectrico de la
proteína lo que a su vez la precipita. Las concentraciones obtenidas para las
muestras problema presentan poca
confiabilidad ya que su rango de límite de
PREGUNTAS COMPLEMENTARIAS confianza en muy amplio.
Determine las concentraciones de las
muestras problema en función de la BIBLIOGRAFIA
curva de calibración.
BOHINSKI, Robert. BIOQUIMICA. 5 ed.
Cuadro 3. Concentración calculada. Mexico: Pearson. 1991. p. 80-96
Concentración
MILLER, J. N.; MILLER, J. C. Estadística
Muestra calculada
y Quimiometría para Química Analítica. 4
(ppm)
ed. España: Prentice Hall, 2002.p. 113-124
Muestra problema 1 22.9
Muestra problema 2 20.48 LEHNINGER, A. Principles of
Muestra problema 3 22.9 Biochemistry. 4 ed. New York: Worth
Publishers. 2006. p.38-41
¿Para qué se emplea el meso-1,4- LOWRY, O.; ROSEBROUGH, N; FARR,
dimercapto-2,3-butanodiol? Explicar el A.; and RANDALL, R. (1951) PROTEIN
fundamento químico MEASUREMENT WITH THE FOLIN PHENOL
El meso-1,4-dimercapto-2,3-butanodiol o REAGENT. The Journal of the Biological.
ditiotreitol (DTT) es un compuestos capaz Chemistry. 193: 265-275
de reducir los enlaces disulfuro de las
proteínas (-S-S-) a grupos sulfhidrilo (-
SH). Permite desplegar completamente una
proteína y separar las subunidades de una
proteína multimérica; ambos efectos son
You might also like
- Problemas de Curva de Calibracion y Adicion EstandarDocument16 pagesProblemas de Curva de Calibracion y Adicion EstandarLeo0% (1)
- Devore Pag 453Document4 pagesDevore Pag 453Paola KasandraNo ratings yet
- Reporte de Practica 2.1Document9 pagesReporte de Practica 2.1Angel ZurielNo ratings yet
- Ejercicios EspectrofotometriaDocument3 pagesEjercicios EspectrofotometriaJaviera M. Valdés100% (1)
- Determinación Gravimétrica de Un Componente (Enviar)Document4 pagesDeterminación Gravimétrica de Un Componente (Enviar)ANDERSON RUBIO CLEVESNo ratings yet
- CALCUlOS ACETAMINOFENDocument3 pagesCALCUlOS ACETAMINOFENJuanka Gonzalez100% (1)
- Quiz Intervalos para Dos Poblaciones 5 Oct 2018Document3 pagesQuiz Intervalos para Dos Poblaciones 5 Oct 2018Mario Jo SeNo ratings yet
- Cuantificación de Etanol en Bebidas Alcohólicas Por Refractometria 2 PDFDocument7 pagesCuantificación de Etanol en Bebidas Alcohólicas Por Refractometria 2 PDFharold diazNo ratings yet
- Fisicoquimica Fase 4Document11 pagesFisicoquimica Fase 4Dani Ortegon BejaranoNo ratings yet
- Caracterizacíon de CombustiblesDocument5 pagesCaracterizacíon de CombustiblesJessica Cuellar RamirezNo ratings yet
- Problemas Tarea Cinetica 1Document83 pagesProblemas Tarea Cinetica 1Marisol BravoNo ratings yet
- Demanda Química de Oxígeno (Dqo) en Una Muestra de AguaDocument8 pagesDemanda Química de Oxígeno (Dqo) en Una Muestra de AguaLINA FERNANDA JURADO TORRESNo ratings yet
- Informe Determinación de Colorante en Bebidas - FinalDocument8 pagesInforme Determinación de Colorante en Bebidas - FinalJORGE LEONARDO FRASSER QUIÑONES0% (1)
- INFORME AcetaminofénDocument16 pagesINFORME AcetaminofénwendyNo ratings yet
- Analisis Problemas EliseoDocument12 pagesAnalisis Problemas EliseoLimon C. UrielNo ratings yet
- Informe 04 Analisis InstrumentalDocument5 pagesInforme 04 Analisis InstrumentalJorge Luis CastilloNo ratings yet
- Acetaminofen Uv TerminadoDocument7 pagesAcetaminofen Uv TerminadoJuanka GonzalezNo ratings yet
- Acetaminofen Uv TerminadoDocument9 pagesAcetaminofen Uv TerminadoJuanka GonzalezNo ratings yet
- 06C DestFraccProbDocument14 pages06C DestFraccProbAriana NuñezNo ratings yet
- Dqo Informe FinalDocument3 pagesDqo Informe FinalSebastian ViverosNo ratings yet
- Sesion 3Document27 pagesSesion 3Rocio DelgadoNo ratings yet
- Análisis proteínas método BradfordDocument8 pagesAnálisis proteínas método BradfordBrenDa Man Cera MolNo ratings yet
- Portafolio 1-3Document3 pagesPortafolio 1-3ruben antoNo ratings yet
- Determinación espectrofotométrica de Fe(II) en jarabe farmacéuticoDocument10 pagesDeterminación espectrofotométrica de Fe(II) en jarabe farmacéuticoJ Mora GañanNo ratings yet
- Informe Practica #1 Colorante en Un Bon Bon Bum RojoDocument10 pagesInforme Practica #1 Colorante en Un Bon Bon Bum Rojogerson velezNo ratings yet
- HPLC FinDocument8 pagesHPLC FinCARLOS MARIO RAMOS CALDERONNo ratings yet
- Determinación Del Contenido de Fósforo Por EspectrofotometríaDocument10 pagesDeterminación Del Contenido de Fósforo Por EspectrofotometríaCamila ValdesNo ratings yet
- Deberes Totales AnaliticaDocument17 pagesDeberes Totales AnaliticaDiego Tobar100% (3)
- Informe Colorimetria HierroDocument4 pagesInforme Colorimetria HierroEstefa Valencia0% (1)
- Errores y precisión en análisis químicoDocument63 pagesErrores y precisión en análisis químicocarlosNo ratings yet
- Determinación Cloruros OrinaDocument7 pagesDeterminación Cloruros Orinaangie santanaNo ratings yet
- Informe Cloruros ListoDocument11 pagesInforme Cloruros ListoSantiago CalderónNo ratings yet
- balances_septimo_tema_2021_2__1_.pptxDocument20 pagesbalances_septimo_tema_2021_2__1_.pptxLinkoriginalNo ratings yet
- E LL EstudiantesDocument9 pagesE LL EstudiantesZAHIRA SOFIA RODRIGUEZ MORENONo ratings yet
- EP - MB535 - 2005 - 2 - Solucionario - PDFDocument6 pagesEP - MB535 - 2005 - 2 - Solucionario - PDFAnonymous 6ZVBcXy7nrNo ratings yet
- Ejercicios CSC, Enero 2021 (Audio)Document31 pagesEjercicios CSC, Enero 2021 (Audio)José Ramón DuarteNo ratings yet
- Informe Practica 3Document7 pagesInforme Practica 3Edwin CanteroNo ratings yet
- Ensayo de Aptitud EA - EjemploDocument7 pagesEnsayo de Aptitud EA - EjemploGLORIA JIMENEZNo ratings yet
- Análisis químico prácticaDocument4 pagesAnálisis químico prácticaNavarro ValeriaNo ratings yet
- Me4 PDFDocument36 pagesMe4 PDFper302No ratings yet
- Fase 3 - Metodos Instrumentales ....Document23 pagesFase 3 - Metodos Instrumentales ....Marlon Andres LopezNo ratings yet
- Determinación de Ácido Cítrico en BebidasDocument4 pagesDeterminación de Ácido Cítrico en BebidasFrAn MirandaNo ratings yet
- Espectroscopía UvDocument7 pagesEspectroscopía UvLEIDY RENTERÍANo ratings yet
- PermanganometriaDocument3 pagesPermanganometriaSantiago CalderónNo ratings yet
- Determinacion de Simeticona PDFDocument6 pagesDeterminacion de Simeticona PDFJuan D GiraldoNo ratings yet
- Análisis espectrofotométrico de muestras de químicaDocument8 pagesAnálisis espectrofotométrico de muestras de químicaDiana Marcela Martinez50% (2)
- Error métodos gravimétricos precipitadoDocument14 pagesError métodos gravimétricos precipitadoAlejandra Martinez LeguizamonNo ratings yet
- Calibración AA Zn aguaDocument20 pagesCalibración AA Zn aguapamela gonzalezNo ratings yet
- INFORME 9 SimeticonaDocument13 pagesINFORME 9 SimeticonaWENDY NATHALIA ROJAS ARCENo ratings yet
- Calculos FluorescenciaDocument6 pagesCalculos FluorescenciaIlanid Alejandra BotinaNo ratings yet
- Experimentos de Determinación de MN Por Medio de Un Tratamiento de Oxido Reducción U Otro Por Acomplejamiento.Document4 pagesExperimentos de Determinación de MN Por Medio de Un Tratamiento de Oxido Reducción U Otro Por Acomplejamiento.Maria Vanessa Dominguez AcevedoNo ratings yet
- Informe Practicas EnzimologiaDocument11 pagesInforme Practicas EnzimologiapauladelmarlmNo ratings yet
- Informe de Mezcla de TintesDocument6 pagesInforme de Mezcla de TintesjohanamarcelasambonyNo ratings yet
- Alumnos Univariante (2) Calibracion 20-21 PDFDocument12 pagesAlumnos Univariante (2) Calibracion 20-21 PDFAna Rodriguez PedrouzoNo ratings yet
- Determinación de Mg(OH)2 en leche de magnesia por conductimetríaDocument8 pagesDeterminación de Mg(OH)2 en leche de magnesia por conductimetríaPRAYME SACNo ratings yet
- Obtener Archivo RecursoDocument31 pagesObtener Archivo Recursoyati EvelynNo ratings yet
- Práctica 8: Polarimetría y RefractometríaDocument11 pagesPráctica 8: Polarimetría y RefractometríaMELANY ELIZABETH MONROY CRUZNo ratings yet
- Problemas Unidad I Ai 2020-2021 Cal ValDocument3 pagesProblemas Unidad I Ai 2020-2021 Cal ValMajo LaraNo ratings yet
- PRÁCTICA N 6 María Paula Carvajal NaviaDocument9 pagesPRÁCTICA N 6 María Paula Carvajal NaviaMaría Paula Carvajal NaviaNo ratings yet
- Practica #4Document6 pagesPractica #4JúpiterNo ratings yet
- NanoporoDocument22 pagesNanoporoFelipeNo ratings yet
- Integridad Del RNADocument11 pagesIntegridad Del RNAFelipeNo ratings yet
- Conductimetro 2Document7 pagesConductimetro 2Mimi RomeroNo ratings yet
- Integridad Del RNADocument11 pagesIntegridad Del RNAFelipeNo ratings yet
- Informe NicotinaDocument21 pagesInforme NicotinaFelipeNo ratings yet
- Grasas y Aceites Info LabDocument7 pagesGrasas y Aceites Info LabFelipe100% (1)
- Disminución de Fenoles, DQO, DBO 5 y Color en Licor Negro Por El Hongo Pleurotus OstreatusDocument17 pagesDisminución de Fenoles, DQO, DBO 5 y Color en Licor Negro Por El Hongo Pleurotus OstreatusFelipeNo ratings yet
- Polimerizacion Acrilamida PDFDocument61 pagesPolimerizacion Acrilamida PDFKristem KertzeifNo ratings yet
- Biología Especial CompletaDocument83 pagesBiología Especial CompletaGastonCarballoNo ratings yet
- Electroforesis proteínas SDS-PAGEDocument15 pagesElectroforesis proteínas SDS-PAGECamila Paulina Aravena SotoNo ratings yet
- Practica 7. Bases de Datos en Proteínas y Enzimas - Aplicaciones de La Proteómica y El Docking MolecularDocument24 pagesPractica 7. Bases de Datos en Proteínas y Enzimas - Aplicaciones de La Proteómica y El Docking MolecularDaniela RiverosNo ratings yet
- Alfa AmilasaDocument18 pagesAlfa AmilasaAndreaNo ratings yet
- Hidrolisis Endoproteasas y ExoproteasasDocument8 pagesHidrolisis Endoproteasas y ExoproteasaskevinNo ratings yet
- ProteínasDocument23 pagesProteínasCamiluhiNo ratings yet
- Blue NativeDocument238 pagesBlue NativeMichael VillacisNo ratings yet
- Electroforesis y Cromatografia PDFDocument25 pagesElectroforesis y Cromatografia PDFjose ricardoNo ratings yet
- Reporte. Purificación de ProteínasDocument11 pagesReporte. Purificación de ProteínasAlta Gracia ArguellesNo ratings yet
- Prelaboratorio 5Document10 pagesPrelaboratorio 5Laura Cecilia Morales MarroquinNo ratings yet
- Guia Lab Inmuno (1° Par)Document29 pagesGuia Lab Inmuno (1° Par)Arturo SalazarNo ratings yet
- Guía laboratorio virología clínica UNICOLMAYORDocument20 pagesGuía laboratorio virología clínica UNICOLMAYORLAURA NATALY VILLAMARIN GALINDONo ratings yet
- Métodos ElectroforéticosDocument34 pagesMétodos Electroforéticosmariipiii100% (2)
- Tesis Maestra en Viticultura y Enologa Pereira CarolinaDocument58 pagesTesis Maestra en Viticultura y Enologa Pereira CarolinaPaolo Gianfranco Luna Victoria GutierrezNo ratings yet
- Técnica ElectroforesisDocument14 pagesTécnica ElectroforesisCarlos VNo ratings yet
- 02 Mothe and Reddy 2016 - Production Purification and Characterization-Protease-Bacillus - En.esDocument10 pages02 Mothe and Reddy 2016 - Production Purification and Characterization-Protease-Bacillus - En.esArturo PeñablassiNo ratings yet
- Reporte 4.proteinasDocument6 pagesReporte 4.proteinasXochitl Razo HernandezNo ratings yet
- Folio 11-AnalisisDocument8 pagesFolio 11-AnalisisKarolayn TeránNo ratings yet
- Conductimetría y Electroforesis en Anlisis de AlimentosDocument26 pagesConductimetría y Electroforesis en Anlisis de AlimentosthaliazairaNo ratings yet
- Microcistina PDFDocument118 pagesMicrocistina PDFJhoan AndreNo ratings yet
- Evidencia FinalDocument17 pagesEvidencia FinalAtzi CortésNo ratings yet
- Practica 5. Electroforesis SDS-PAGE y LípidosDocument9 pagesPractica 5. Electroforesis SDS-PAGE y Lípidosjacobo caicedo angelNo ratings yet
- Electroforesis de Gel de Poliacrilamida en Gel de Agarosa y Diferencia Entre Ambas Analisis InstrumentalDocument36 pagesElectroforesis de Gel de Poliacrilamida en Gel de Agarosa y Diferencia Entre Ambas Analisis InstrumentalJuan OrtizNo ratings yet
- Artículo 7Document6 pagesArtículo 7Cele Lbo JaraNo ratings yet
- Clase Control de CalidadDocument83 pagesClase Control de CalidadRudimentalNo ratings yet
- Manual de Virología 2022Document163 pagesManual de Virología 2022Lesly GalindoNo ratings yet
- Recolección de MuestraDocument2 pagesRecolección de MuestraJhoan Yampol Perez MendezNo ratings yet
- Equipo 7 Práctica 4 Electroforesis RevisadoDocument14 pagesEquipo 7 Práctica 4 Electroforesis RevisadoSamuel SosaNo ratings yet