Professional Documents
Culture Documents
Diagnostico Entrada
Uploaded by
Daniela RomeroOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Diagnostico Entrada
Uploaded by
Daniela RomeroCopyright:
Available Formats
COLEGIO LICEO FEMENINO “MERCEDES NARIÑO” J. M.
ÁREA: CIENCIAS NATURALES Y EDUCACIÓN AMBIENTAL
DIAGNOSTICO ENTRADA
QUÍMICA GRADO 11° JM
Prof. Juan Gabriel Perilla J. / Veronica Isabel Pinzón T / Ramiro González Gómez
ESTUDIANTE: __________________________________________ CURSO: _________ Fecha: ___________
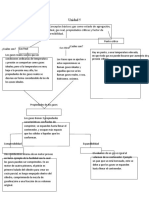
I. ACTIVIDAD A presión
constante, el
Estado gaseoso volumen
ocupado por
un gas es
Es el estado de la materia que se distingue porque
directamente
no tiene forma ni volumen fijo; se caracteriza por la
proporcional a
casi nula cohesión (atracción entre sus moléculas) y
su
la gran energía cinética de sus moléculas. Su
temperatura.
principal composición son moléculas no unidas, que
Es decir que si
hacen que este se expanda para ocupar todo el
el volumen
volumen del recipiente que lo contiene y que se
aumenta, la
pueda también comprimir. Existen diversas leyes
temperatura
que relacionan la presión, el volumen y la
también
temperatura de un gas.
aumenta.
Las unidades para las principales variables de un gas
son:
Variable Unidad
Ley de Gay-Lussac
Presión Atmósferas
A volumen
Volumen Litros constante, la
Temperatura Grados Kelvin presión del
gas es
Cantidad Moles directamente
proporcional a
Boyle – Mariotte
la
A temperatura temperatura.
constante, el
volumen de un
gas será
inversamente
proporcional a la
presión. (La masa
Ley de los gases ideales
debe ser también
constante). Es
Las tres leyes mencionadas pueden combinarse
decir que cuando
matemáticamente en la llamada ley general de los
aumenta la
gases. Su expresión matemática es:
presión, el
volumen
disminuye; si la
presión
disminuye el Siendo P la presión, V el volumen, n el número de
volumen moles, R la constante universal de los gases ideales
aumenta. y T la temperatura en grados Kelvin
El valor de R es: R = 0,082 atm•l•K-1•mol-1
Ley de Charles De esta ley se deduce que un mol de gas ideal
ocupa siempre un volumen igual a 22,4 litros.
Se dice que un gas está bajo condiciones ideales
cuando su temperatura es 0°C (273°K) y su presión
es una atmósfera
Ley de Avogadro ser sólida, liquida o gaseosa, estudiaremos las
soluciones líquidas cuyo disolvente es el agua
Es aquella en el que las constantes son presión y (soluciones acuosas)
temperatura, siendo el Volumen directamente Solvente: Es el componente más abundante en una
proporcional al Número de moles (n) solución. El agua es un excelente disolvente de
matemáticamente, la fórmula es: sustancias polares y algunas no polares.
Soluto: sustancia que se encuentra en menor
proporción en una solución. Puede ser sólida,
líquida o gaseosa.
Formada por enlaces iónicos que
indican formación de iones o átomos
Sustancia
Taller de lectura 24 con cargas eléctricas. La mayoría de las
polar
sales, ácido e hidróxidos inorgánicos,
1. ¿Qué es el estado gaseoso? son sustancias polares
2. ¿Por qué se caracteriza el estado gaseoso? Formada por enlaces covalentes o
3. ¿Qué se da a entender cuando se dice que un moleculares. No hay interacción de
gas se expande o se comprime? Sustancia cargas eléctricas. El yodo y el azufre,
4. ¿En qué consiste la ley de Boyle? Escriba la no polar junto con la mayoría de los
fórmula y la gráfica que relaciona las variables compuestos orgánicos, son sustancias
5. ¿En qué consiste la ley de Charles? Escriba la no polares
fórmula y la gráfica que relaciona las variables Por lo general, un solvente polar disuelve sustancias
6. ¿En qué consiste la ley de Gay-Lussac? Escriba la polares y un solvente no polar, disuelve sustancias
fórmula y la gráfica que relaciona las variables no polares
7. ¿En qué consiste la ley de los gases ideales?
Escriba la fórmula que relaciona las variables Conceptos:
Solubilidad: Cantidad de soluto que se disuelve en
8. ¿Cuál es el valor de la constante universal de los una cantidad establecida de solvente, bajo
gases ideales? condiciones específicas de presión y temperatura.
9. ¿Qué volumen ocupa un mol de gas ideal? La solubilidad aumenta con el aumento de
10. ¿Cuándo se dice que un gas está bajo temperatura en la mayoría de los casos.
condiciones ideales? Solución diluida o insaturada: Es aquella que
11. ¿En qué consiste la ley de Avogadro? Escriba la contiene una cantidad de soluto muy bajo en
fórmula que relaciona las variables. comparación con la cantidad que el solvente puede
disolver
12. Resuelva los siguiente problemas mostrando el
Solución saturada: Aquella que tiene una cantidad
proceso completo:
de soluto aproximadamente igual a la cantidad que
I. Un gas ocupa un volumen de 2 l en condiciones el soluto puede disolver
normales. ¿Qué volumen ocupará esa misma Solución sobresaturada: Aquella que tiene una
masa de gas a 2 atm y 50ºC? cantidad de soluto mayor que la cantidad que el
II. Un recipiente cerrado de 2 l. contiene oxígeno a solvente puede disolver. Quedará parte del soluto
200ºC y 2 atm. Calcula: a) Los gramos de sin disolver
oxígeno contenidos en el recipiente. b) Las Concentración: Es la relación cuantitativa entre la
moléculas de oxígeno presentes en el cantidad de soluto y la cantidad de solución. Las
recipiente. unidades de concentración, pueden ser físicas o
III. Un recipiente contienen 100 l de O2 a 20ºC. químicas.
Calcula: a) la presión del O2, sabiendo que su Unidad de
masa es de 3,43 kg. b) El volumen que ocupara Definición Fórmula
concentración
esa cantidad de gas en c.n.
Masa de
IV. Calcula la fórmula molecular de un compuesto
soluto en
sabiendo que 1 l de su gas, medido a 25ºC y 750
relación
mm Hg de presión tiene una masa de 3,88 g y % en
con la
que su análisis químico ha mostrado la siguiente peso
masa de la
composición centesimal: C, 24,74 %; H, 2,06 % y
solución
Cl, 73,20 %.
por cien
Físicas
Volumen
II. Actividad de soluto
Disoluciones % en en
volume relación al
Las soluciones son mezclas homogéneas formadas n volumen
principalmente, por dos componentes: el soluto y el de la
solvente o disolvente. Aunque una solución puede solución
por cien 6. ¿Qué es soluto? ¿En qué estados puede
presentarse?
Masa de 7. ¿Qué es una sustancia polar?
soluto en
8. ¿Qué es una sustancia no polar?
Peso a relación
volume con el 9. ¿Qué tipo de sustancias se disuelven en
n volumen solventes polares?
de la 10. ¿Qué tipo de sustancias se disuelven en
solución solventes no polares?
Moles de 11. ¿Qué es solubilidad?
Molarid soluto por 12. ¿Cómo varía la solubilidad con la variación de la
ad (M) litro de temperatura?
solución 13. Escriba las definiciones de solución insaturada,
saturada y sobresaturada.
Moles de
soluto por 14. ¿Qué es concentración?
Molalid
kilogramo 15. Copie la tabla que resume las unidades de
ad (m)
de concentración con sus definiciones y fórmulas
solvente 16. ¿A qué hacen referencia las propiedades
Número coligativas?
Quími
cas de 17. Defina cada una de las propiedades coligativas
equivalent 18. ¿En qué tipo de soluciones funcionan mejor los
Normali es gramo cálculos de las propiedades coligativas?
dad (N) de soluto 19. Resuelva los siguientes ejercicios mostrando el
por litro procedimiento:
de
19.1 Se prepara una solución acuosa con 55.0 g
solución
de KNO3 (nitrato de potasio), disolviendo la sal
Moles de hasta completar 500 mL de solución. Calcule su
Fracció
soluto por concentración en % m/v. (Rsta: 11.0 % m/v)
n molar
moles de 19.2 Se obtiene una solución de c = 33.5 % m/v.
(x)
la solución
Propiedades coligativas: hacen relación a las a) ¿Qué significa 33.5 % m/v?
propiedades físicas de una solución que cambian al b) ¿Qué densidad posee la solución si 100.0 mL
variar su concentración. Estas propiedades son: de ella pesan 111.0 g? (Rsta: 1.11
Aumento del punto de ebullición: en g/mL).
soluciones cuyo soluto es no volátil, el punto de c) ¿Cuántos gramos de soluto habrá en 40.0 mL
ebullición de la solución, aumenta con la de solución? (Rsta: 44.4 g).
concentración. d) Si se agrega agua a estos 40.0 mL de solución
Descenso del punto de congelación: el hasta completar 100.0 mL. ¿Cuál será el %
punto de congelación de una solución, disminuye al m/v de la solución resultante?. (Rsta: 13.4 %
aumentar la concentración m/v).
19.2 Calcule el número de mol de soluto en las
Descenso de la presión de vapor: la presión
siguientes disoluciones:
de vapor disminuye con el aumento de la
concentración
a) L de BaCl2 (cloruro de bario), 2.0 M. (Rsta:
Presión osmótica: Aumenta con la 5.0 mol).
concentración de la solución
Nota: Estas propiedades son medibles con más b) 5.0 L de NaI (yoduro de sodio), 0.53 M. (Rsta:
exactitud en soluciones diluidas 2.65 mol).
Taller 19.3 Se desea preparar 500 mL de solución de
ácido clorhídrico (HCl) 0.10 M a partir de un
1. ¿Qué es una solución? ácido comercial cuya densidad es 1.19 g/mL y
2. ¿En qué estados pueden presentarse las su concentración 37.0 %p/p. Calcule el volumen
soluciones?
del ácido que necesite para preparar esta
3. ¿Cómo se llaman las soluciones cuyo solvente solución. (Rsta: 4.17 x 10-3 L).
es el agua?
4. ¿A qué hace referencia la palabra solvente o 19.4 Calcule la normalidad de las siguientes
disolvente? disoluciones:
5. ¿Qué tipo de sustancias puede disolver el agua? a) 9g de H3PO4 en 500mL de solución.
b) 100g de NaCl en 2L de solución.
Para obtener el material K3Q2J se llevan a cabo las
III ACTIVIDAD siguientes reacciones
Paso I: K + M KM
Resuelva la siguiente prueba en el cuaderno
Paso II: 3KM + Q2X M3X + K3Q2
justificando cada respuesta.
Paso III: K3Q2 + J K3Q2J
PREGUNTAS TIPO I: Selección múltiple con única
Masa Molecular
respuesta. Lea con mucha atención antes de
Sustancia (g/mol)
responder las preguntas.
Conteste las preguntas 1 y 2, teniendo en cuenta la X 20
siguiente información: K 27
M 35
Algunas reacciones del material T se presentan en Q 18
los siguientes esquemas de reacción: J 41
1. T + O2 A
2. A + H2O H2TO3
3. H2TO3 + B X2TO3 4. De acuerdo con la información anterior, es
correcto afirmar que a partir de:
1. De acuerdo con la información anterior, es A. 2 moles de KM se obtiene 1 mol de K3Q2J
válido afirmar que la formula más probable para B. 2 mol de K3Q2 se obtiene 1 mol de K3Q2J
el compuesto A es: C. 1 mol de KM se obtiene 1 mol de K3Q2.
A. TO D. 1 mol de K3Q2 se obtiene 1 mol de K3Q2J
B. TO3
C. TO2 5. Si se hace reaccionar 186 g de KM con
D. T2O suficiente Q2X, es correcto afirmar que se
2. De acuerdo con la información anterior, la obtienen:
formula más probable del compuesto B es: A. 2 moles de K3Q2
A. XOH B. 1 moles de K3Q2
B. H2TO3 C. 3 moles de K3Q2
C. TO3 D. 0,5 moles de K3Q2
D. XH
6. Se requiere obtener 474 g de K3Q2J; para ello,
3. Se realizó un análisis para determinar la es necesario hacer reaccionar:
composición iónica de tres muestras de suelo. A. 2 moles de K3Q2 con 2 moles de J
Los resultados del análisis se presentan en la B. 6 moles de KM con 1 moles de Q2X
siguiente tabla. C. 6 moles de KM con 3 moles de Q2X
D. 3 moles de K3Q2 con 2 moles de J
Muestra 1 Muestra 2 Muestra 3
Las preguntas 7 y 8 se responden teniendo en
Na+1 Ca+2 Cl -1
cuenta la siguiente información.
NH4+1 K+1 PO4 -3
SO4-2 NO3 -1 Ca+2
El Ciclo del cobre consta de una serie de reacciones
K+1 F-1 Na+1
que permiten observar una secuencia de reacciones
del cobre que forman un ciclo y además aprender a
De acuerdo con la información anterior, es muy registrar observaciones referentes a las reacciones
probable que en la muestra 3 se encuentren las químicas utilizando un esquema de clasificación
sales: simple y practicar técnicas cuantitativas sencillas de
A. Na2Ca, CaCl2, Na3PO4 y Ca3(PO4)2. laboratorio para determinar el porcentaje de cobre
B. NaCl, Na(PO4)3 y Ca3(PO4)2. recuperado. Las etapas en desorden de las que
consta son las siguientes:
C. CaCl2, Ca3(PO4)2 y Na2Ca.
D. NaCl, CaCl2, Na3PO4 y Ca3(PO4)2. 1. Óxido de cobre (II) + ácido sulfúrico →
sulfato de cobre (II) + agua
Las preguntas 4 a la 6 se contestan de acuerdo con 2. Cobre + ácido nítrico → nitrato de cobre (II)
la siguiente información. + dióxido de nitrógeno + agua
3. Sulfato de cobre (II) + potasio → sulfato de D. 39.13 g de C7H6O3
potasio + cobre
4. Hidróxido de cobre (II) + calor → óxido de 10. Si el químico farmacéutico obtiene de esta
cobre (II) reacción 35 g de aspirina (C9H8O4), el porcentaje
5. Nitrato de cobre (II) + hidróxido de sodio →
del rendimiento de este proceso es:
Hidróxido de cobre (II) + nitrato de sodio
A. 89, 44 %
Elemento Masa atômica o B. 76,66 %
molar (g/mol) C. 98, 54 %
Cu 63 D. 111, 8 %
Reflexión de Bienvenida
H 1
O 16 CÓMO PENSAR
N 14 Sir Ernest Rutherford, presidente de la Sociedad Real
S 32 Británica y Premio Nóbel de Química en 1908, contaba la
Na 23 siguiente anécdota: Hace algún tiempo, recibí la llamada
K 39 de un colega. Estaba a punto de poner un cero a un
estudiante por la respuesta que había dado en un
problema de física, pese a que este afirmaba
7. De acuerdo con los procesos del ciclo del cobre rotundamente que su respuesta era absolutamente
es correcto afirmar que el orden exacto de las acertada. Profesores y estudiantes acordaron pedir
arbitraje de alguien imparcial y fui elegido yo. Leí la
reacciones debe ser:
pregunta del examen y decía:
A. 2, 4, 5, 1, 3 Demuestre cómo es posible determinar la altura de un
B. 2, 5, 4, 1, 3 edificio con la ayuda de un barómetro. El estudiante
C. 1, 2, 3, 4, 5 había respondido: llevo el barómetro a la azotea del
edificio y le ato una cuerda muy larga. Lo descuelgo hasta
D. 3, 5, 4, 1, 2
la base del edificio, marco y mido. La longitud de la
cuerda es igual a la longitud del edificio.
8. En una de las etapas anteriormente
mencionada, el Nitrato de cobre (II) + hidróxido Realmente, el estudiante había planteado un serio
de sodio → Hidróxido de cobre (II) + nitrato de problema con la resolución del ejercicio, porque había
respondido a la pregunta correcta y completamente. Por
sodio, según esta es correcto afirmar que si
otro lado, si se le concedía la máxima puntuación, podría
reacciona 2.5 g de Nitrato de cobre (II), se
alterar el promedio de su año de estudio, obtener una
obtendrán: nota más alta y así certificar su alto nivel en física; pero la
A. 97 g de Hidróxido de cobre (II) respuesta no confirmaba que el estudiante tuviera ese
B. 187 g de Hidróxido de cobre (II) nivel.
C. 1, 29 g de Hidróxido de cobre (II)
D. 2, 9 g de Hidróxido de cobre (II) Sugerí que se le diera al alumno otra oportunidad. Le
concedí seis minutos para que me respondiera la misma
Las preguntas 9 y 10 se contestan de acuerdo con la pregunta pero esta vez con la advertencia de que en la
siguiente información. respuesta debía demostrar sus conocimientos de física.
Habían pasado cinco minutos y el estudiante no había
La aspirina (C9H8O4) se produce haciendo reaccionar
escrito nada.
ácido salicílico (C7H6O3) con anhídrido acético Le pregunté si deseaba marcharse, pero me contestó que
(C4H6O3), en esta reacción se obtiene además ácido tenía huchas respuestas al problema. Su dificultad era
acético (C2H4O2). Un químico farmacéutico prueba elegir la mejor de todas. Me excusé por interrumpirle y le
rogué que continuara. En el minuto que le quedaba
un nuevo procedimiento para obtener aspirina escribió la siguiente respuesta: tomo el barómetro y lo
utilizando 30 g de ácido salicílico (C7H6O3) y 25 de lanzo al suelo desde la azotea del edificio, calculo el
anhídrido acético (C4H6O3). tiempo de caída con un cronometro. Después se aplica la
formula altura = 0,5 por A por t^2. Y así obtenemos la
altura del edificio.
Elemento Masa atômica o
molar (g/mol) En este punto le pregunté a mi colega si el estudiante se
C 12 podía retirar. Le dio la nota más alta. Tras abandonar el
despacho, me reencontré con el estudiante y le pedí que
H 1 me contara sus otras respuestas a la pregunta.
O 16 Bueno, respondió, hay muchas maneras, por ejemplo:
tomas el barómetro en un día soleado y mides la altura
del barómetro y la longitud de su sombra. Si medimos a
9. La máxima cantidad de aspirina que puede continuación la longitud de la sombra del Edificio y
obtener es: aplicamos una simple proporción, obtendremos también
A. 180 g de C9H8O4 la altura del edificio.
B. 102 g de C4H6O3 Perfecto, le dije, ¿y de otra manera?.
C. 39.13 g de C9H8O4
Si, contestó, éste es un procedimiento muy básico para
medir la altura de un edificio, pero también sirve.
En este método, tomas el barómetro y te sitúas en las
escaleras del edificio en la planta baja. Según subes las
escaleras, vas marcando la altura del barómetro y
cuentas el número de marcas hasta la azotea. Multiplicas
al final la altura del barómetro por el número de marcas
que has hecho y ya tienes la altura.
Este es un método muy directo. Por supuesto, si lo que
quiere es un procedimiento más sofisticado, puede atar
el barómetro a una cuerda y moverlo corno si fuera un
péndulo. Si calculamos que cuando el barómetro está a la
altura de la azotea la gravedad es cero y si tenemos en
cuenta la medida de la aceleración de la gravedad al
descender el barómetro en trayectoria circular al pasar
por la perpendicular del edificio, de la diferencia de estos
valores, y aplicando una sencilla fórmula trigonométrica,
podríamos calcular, sin duda, la altura del edificio.
En este mismo estilo de sistema, atas el barómetro a una
cuerda y lo descuelgas desde la azotea a la calle.
Usándolo como un péndulo puedes calcular la altura
midiendo su período de precisión.
En fin, concluyó, existen otras muchas maneras.
Probablemente, la mejor sea tomar el barómetro y
golpear con el la puerta de la casa del portero. Cuando
abra, decirle: "Señor portero, aquí tengo un bonito
barómetro. Si usted me dice la altura de este edificio, se
lo regalo".
En este momento de la conversación, le pregunté si no
conocía la respuesta convencional al problema (la
diferencia de presión marcada por un barómetro en dos
lugares diferentes nos proporciona la diferencia de altura
entre ambos lugares) evidentemente, dijo que la conocía,
pero que durante sus estudios, sus profesores habían
intentado enseñarle a pensar. El estudiante se llamaba
Niels Bohr, físico danés, premio Nóbel de física en 1922,
más conocido por ser el primero en proponer el modelo
de átomo con protones y neutrones y los electrones que
lo rodeaban. Fue fundamentalmente un innovador de la
teoría cuántica.
Al margen del personaje, lo divertido y curioso de la
anécdota, lo esencial de esta historia es que LE HABÍAN
ENSEÑADO A PENSAR.
Por cierto, para los escépticos, esta historia es
absolutamente verídica.
Aprendamos a pensar, hay mil soluciones para un mismo
problema, pero lo realmente interesante, lo
auténticamente genial es elegir la solución más práctica y
rápida, de forma que podamos acabar con el problema
de raíz... y dedicarnos a solucionar OTROS problemas.
ÉXITOS Y LOS MEJORES DESEOS EN EL
NUEVO AÑO.
Con fraternidad, Equipo docentes Química JM
You might also like
- Volumen Molar de Un Gas en Condiciones NormalesDocument4 pagesVolumen Molar de Un Gas en Condiciones NormalesLuis Felipe Martínez Vargas50% (2)
- Expo Ley de HenryDocument4 pagesExpo Ley de HenryDaniela PeñarandaNo ratings yet
- Ley de CharlesDocument11 pagesLey de Charlesalfredo_1313No ratings yet
- Capitulo 1 GasDocument24 pagesCapitulo 1 GasOmar Catañed PeñaNo ratings yet
- Capitulo 1 Wark TermodinamicaDocument5 pagesCapitulo 1 Wark TermodinamicaAlberto LeónNo ratings yet
- Informe Quimica 7Document14 pagesInforme Quimica 7Gene ValenzuelaNo ratings yet
- Práct. Bomba de MahlerDocument13 pagesPráct. Bomba de MahlereugeniaNo ratings yet
- Tema 4 Exámenes de LaboratorioDocument41 pagesTema 4 Exámenes de LaboratorioHujiNo ratings yet
- Biografias BalancesDocument35 pagesBiografias BalancesJuan Manuel Hernández Reyes100% (1)
- Universidad Del Atlantico Facultad de IngenieriaDocument14 pagesUniversidad Del Atlantico Facultad de IngenieriaRAUL ALEJANDRO ORTIZ GARCIANo ratings yet
- Ley de HenryDocument10 pagesLey de HenryKim ChanNo ratings yet
- Gases Ideales LAB FISQUIMDocument2 pagesGases Ideales LAB FISQUIMCarlosLondoño0% (1)
- Informe Gases Ideales (1) 2018Document11 pagesInforme Gases Ideales (1) 2018lorenaNo ratings yet
- Determinacion de Plomo en Lapiz LabialDocument8 pagesDeterminacion de Plomo en Lapiz Labialvictor_cordova_66No ratings yet
- Práctica 1 Conocimiento y Manejo Del Material de LaboratorioDocument34 pagesPráctica 1 Conocimiento y Manejo Del Material de LaboratorioAdrian Osorio100% (1)
- Trabajo Gases PDFDocument7 pagesTrabajo Gases PDFVictor AlexanderNo ratings yet
- Medición de Calor Específico de Un MetalDocument5 pagesMedición de Calor Específico de Un MetalAlanis Portillo Rawlins100% (1)
- Termodinamica de La AtmosferaDocument57 pagesTermodinamica de La AtmosferaAranValdomeroNo ratings yet
- Entalpía de Vaporización Del AguaDocument27 pagesEntalpía de Vaporización Del AguaDea Carla JassoNo ratings yet
- Termo - PUCP-2016-DG-Eqilib-1Document12 pagesTermo - PUCP-2016-DG-Eqilib-1NEXARNo ratings yet
- Laboratorio Fisicoquimica - GasesDocument18 pagesLaboratorio Fisicoquimica - GasesDaniel Carmen Orozco100% (1)
- 2 Gases Ideales SolucionesDocument7 pages2 Gases Ideales SolucionesAquaSecta OwONo ratings yet
- Química PDFDocument35 pagesQuímica PDFmonNo ratings yet
- Clase 03 CCNN 02Document89 pagesClase 03 CCNN 02NICOLE ERIKA DEL CARMEN HUAPAYA PAUCARNo ratings yet
- Exposición de GasesDocument24 pagesExposición de GasesMaryel Elizabeth Salazar SarmientoNo ratings yet
- Unidad 2 Estado de La Materia 530.0011Document21 pagesUnidad 2 Estado de La Materia 530.0011Paula PaivaNo ratings yet
- Infografia GasesDocument1 pageInfografia GasesDanielNo ratings yet
- Área: Ciencias Naturales Asignatura: Física Docente: Esp. Yenny R. Osorio Suárez Fecha de Devolución: 25/08/20 Grado: Octavo Estudiante: ObjetivoDocument4 pagesÁrea: Ciencias Naturales Asignatura: Física Docente: Esp. Yenny R. Osorio Suárez Fecha de Devolución: 25/08/20 Grado: Octavo Estudiante: ObjetivoAlexis McallisterNo ratings yet
- Estequiometria de Los GasesDocument4 pagesEstequiometria de Los GasesJuliana carrillo HerreraNo ratings yet
- TALLER SOBRE GASES Y SUS LEYES SolucionDocument6 pagesTALLER SOBRE GASES Y SUS LEYES Solucionnatalia vertel martinezNo ratings yet
- Grupo 03 - Gases Ideales y Gases RealesDocument21 pagesGrupo 03 - Gases Ideales y Gases RealesnfernandezNo ratings yet
- Mapa Conceptual Quimica Unidad 5Document11 pagesMapa Conceptual Quimica Unidad 5Benito CameloNo ratings yet
- Estado GaseosoDocument17 pagesEstado GaseosoCiro Alejandro Pacheco CardenasNo ratings yet
- Lab Quimica 7.1Document9 pagesLab Quimica 7.1Cesar MendozaNo ratings yet
- Mapa Conceptual-Ley de Los GasesDocument1 pageMapa Conceptual-Ley de Los GasesPiscis Yallercco67% (3)
- Informe 3Document8 pagesInforme 3JENI MARCILLO MORÁNNo ratings yet
- Trabajo de GasesDocument4 pagesTrabajo de GasesMiguel GómezNo ratings yet
- Tema - 05 - GasesDocument29 pagesTema - 05 - GasesMaria RegeneaNo ratings yet
- Ley de Los GasesDocument8 pagesLey de Los GasesLaura GarcíaNo ratings yet
- Termodinamica (13177) Franklin Munoz 2016-1 PDFDocument407 pagesTermodinamica (13177) Franklin Munoz 2016-1 PDFNaty Paez BarrazaNo ratings yet
- Práctica de GasesDocument9 pagesPráctica de GasesCristina Mercedes Oclocho AltamiranoNo ratings yet
- T3 Estados Agregación 2324 JMAG Alumnos-4DiapDocument15 pagesT3 Estados Agregación 2324 JMAG Alumnos-4DiapAlejandro MariscalNo ratings yet
- 2.1 Generalidades Del Estado Gaseoso y Leyes de Los GasesDocument3 pages2.1 Generalidades Del Estado Gaseoso y Leyes de Los GasesMEJIA EUTIMIO GABRIELA100% (1)
- TRABAJO 3. - Ley General de Los Gases y La Ecuación de Bernoulli PDFDocument9 pagesTRABAJO 3. - Ley General de Los Gases y La Ecuación de Bernoulli PDFeduplay 11No ratings yet
- El Estado Gaseoso Leyes de Los GasesDocument27 pagesEl Estado Gaseoso Leyes de Los Gasesmaga_azulNo ratings yet
- Los Gases y Las Leyes de Los GasesDocument28 pagesLos Gases y Las Leyes de Los GasesNany HeddrichNo ratings yet
- Infografía de Proceso Pantalla Interfaz Pixel Rosa - 20240315 - 013851 - 0000.pdf - 20240315 - 014237 - 0000Document5 pagesInfografía de Proceso Pantalla Interfaz Pixel Rosa - 20240315 - 013851 - 0000.pdf - 20240315 - 014237 - 0000Juan rafael QuibNo ratings yet
- Leyes de Los GasesDocument29 pagesLeyes de Los GasesJherson Chata GomezNo ratings yet
- Ley de Los Gases IdealesDocument6 pagesLey de Los Gases IdealesvanessaNo ratings yet
- Estado-Gaseoso 4Document28 pagesEstado-Gaseoso 4Helen AndreaNo ratings yet
- Ley de Los Gases InformeDocument5 pagesLey de Los Gases InformeSharid Dayan Verjan AcostaNo ratings yet
- Clase Gases. Leyes de Los GasesDocument42 pagesClase Gases. Leyes de Los GasesEMILIO RODRIGUEZ CALDERONNo ratings yet
- Sesion 10 Estados de La Materia y Leyes de Los GasesDocument23 pagesSesion 10 Estados de La Materia y Leyes de Los Gasesgarcia5512No ratings yet
- U2-E1-Lopez Zamora Luis FernandoDocument8 pagesU2-E1-Lopez Zamora Luis FernandoLuis Fërnandö LòpezNo ratings yet
- Semana 11Document6 pagesSemana 11MISHELL JULISA MAMANI FLORESNo ratings yet
- Estado GaseosoDocument28 pagesEstado GaseosoGrover Quispe CallisayaNo ratings yet
- Vocabulario de Gases QuimicaDocument9 pagesVocabulario de Gases Quimicaguadalupe guadalupeNo ratings yet
- FQ Gpo224 Ei6Document4 pagesFQ Gpo224 Ei6DacKZoneYTNo ratings yet
- Trabajo GasesDocument3 pagesTrabajo GasesSheila100% (1)
- Gases Ideales y RealesDocument18 pagesGases Ideales y RealesEMMA BERENICE ASCENCIO LOPEZNo ratings yet
- Propiedades de Los Gases-Ley Convinada... QuímicaDocument15 pagesPropiedades de Los Gases-Ley Convinada... QuímicaPaola JimenezNo ratings yet
- GUIA No 7Document15 pagesGUIA No 7Cristian Alexander0% (1)
- Cuestionario #2 - Gases Perfecto y RealesDocument2 pagesCuestionario #2 - Gases Perfecto y RealesMagui MNo ratings yet
- Ley de Los Gases IdealesDocument2 pagesLey de Los Gases IdealesErikita OcañaNo ratings yet
- Fisica II - Gases IdealesDocument7 pagesFisica II - Gases IdealesluciitautecNo ratings yet
- PDC 5to Química - LHDocument12 pagesPDC 5to Química - LHRosendo Justiniano60% (5)
- Clase de Gases IdealesDocument31 pagesClase de Gases IdealesGIAN FRANCO ALTAMIRANO TORRESNo ratings yet
- Plan Anual Ciencias Naturales 8°Document8 pagesPlan Anual Ciencias Naturales 8°Daniela Soto ValleNo ratings yet
- I.1.1 Ecuación de Gases IdealesDocument3 pagesI.1.1 Ecuación de Gases IdealesMartin Kittsteiner OyanedelNo ratings yet
- Guia 8 Producción y Reconocimiento de GasesDocument8 pagesGuia 8 Producción y Reconocimiento de GasesKelly Díaz50% (2)
- Eds 2020u1 4Document44 pagesEds 2020u1 4Kevin IzaguirreNo ratings yet
- Análisis DimensionalDocument3 pagesAnálisis Dimensionaljosee lopezNo ratings yet
- Práctica #01 de Lab de FQDocument20 pagesPráctica #01 de Lab de FQAlejandro CarvelliNo ratings yet
- Ley de BoyleDocument5 pagesLey de BoyleCarlos Duran Salazar ✅100% (1)
- Tpn3 GasesDocument6 pagesTpn3 GasesFeryi RudoNo ratings yet
- 01-Gas IdealDocument11 pages01-Gas IdealEduardo AlemánNo ratings yet
- 3 CuestionarioDocument1 page3 CuestionarioAlejoNo ratings yet
- Ley Combinada de Los GasesDocument8 pagesLey Combinada de Los GasesLuisa BotiaNo ratings yet
- Clase 1 Semana 2 - Gases RealesDocument25 pagesClase 1 Semana 2 - Gases RealesCarlos AlarconNo ratings yet
- Sesion 01-Curso Procesos Industriales Octubre - 2023Document134 pagesSesion 01-Curso Procesos Industriales Octubre - 2023Luis Sanchez CamachoNo ratings yet
- Termodinámica Unidad 2Document21 pagesTermodinámica Unidad 2Jael SanchezNo ratings yet
- Formulario de Termodinámica-1-1Document2 pagesFormulario de Termodinámica-1-1CristhianMauricioAguilarNo ratings yet
- 10 Termodinamica IDocument7 pages10 Termodinamica IPool PosadaNo ratings yet
- Temario FisicoquimicaDocument6 pagesTemario FisicoquimicaDavid MolinaNo ratings yet
- Ejercicios de Estequiometría Unidad 4 y 5Document30 pagesEjercicios de Estequiometría Unidad 4 y 5aldahirpacheco87No ratings yet
- TeoriaCinetica PresiónDocument5 pagesTeoriaCinetica PresiónSebastian VeraNo ratings yet
- Determinación de La Masa Molar de Un Líquido Fácilmente VaporizableDocument2 pagesDeterminación de La Masa Molar de Un Líquido Fácilmente VaporizableManuel Alejandro Collazos Botero0% (1)
- Laboratorio N°3Document21 pagesLaboratorio N°3FV AlexNo ratings yet
- Reportep 9Document5 pagesReportep 9Daniela MolinaNo ratings yet