Professional Documents
Culture Documents
Cálculos de pH y preparación de buffers
Uploaded by
Dylan Navarro LOriginal Description:
Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Cálculos de pH y preparación de buffers
Uploaded by
Dylan Navarro LCopyright:
Available Formats
1.Cuál es el pH de una solución cuya concentración de hidrogeniones es 3.2*10 -4 M?
2.¿El pH de una solución de ácido fórmico 0.03 M es?
¿Cuánto molar hay de ácido disociado (anión-ion formato) y cuanto hay sin disociar?
pKa = 3.25
3.Un buffer acetato es hecho de mezclar 400 ml de 1 M ácido acético y 600 ml de
acetato de sodio 2M. Cuál será el pH? pKa=4,76
4.Cuál es el pH de un buffer preparado adicionando 60 ml de 0.1 M
CH3COOH a 40 ml de una solución de CH3COONa 0.1 M?
5.Cuál es el pH de un buffer acetato preparado por adicionar 20 ml de 1 M HCl a 100
ml de una solución de acetato de sodio 0.3 M? pka = 4,76
6.Cuál es el valor de pH de un buffer hecho de 10 ml de Tris 0.1 M y 5
ml de Tris- HCL 0.14 M? pKa=8.06
7. ¿Cómo se prepararía un buffer de ácido acético, concentración total 0.1 M pH=4.9?
pKa= 4,76
a. Calcular las molaridades de cada especie
b. (Con respecto a los resultados de a) Si tengo ácido acético glacial (96 % p/p,
densidad 1,2 g/ml) y acetato de sodio sólido (PM ácido acético = 60, PM
acetato de sodio = 82), para un volumen final de 1 L ¿cuántos ml de ácido
acético glacial se requieren y cuántos gramos de acetato de sodio sólido?
Pka = 4,76
8. Cuántos gramos de cada especie (supuestas sales de sodio NaH 2PO4, etc) se
encuentran por litro de solución amortiguadora que se indica?
a) Solución pH 1.70, y el balance de fosfato (concentración total) es 0.5 M
b) Solución pH 3.00, y el balance de fosfato (concentración total) es 0.15 M
c) Solución pH 1.50, y el balance de acetato (concentración total) es 0.2 M
d) Solución pH 4.00, y el balance de fostato (concentración total) es 0.25 M
e) Solución pH 7.32 y el balance de fosfato (concentración total) es 0.35 M
f) Solución pH 9.50, y el balance de tris (concentración total) es 0.4 M
g) Solución pH 10.70, y el balance de tris (concentración total) es 0.25 M
h) Solución pH 11.70, y el balance de fosfato (concentración total) es 0.3 M
i) Solución pH 7.00, y el balance de fosfato (concentración total) es 0.6 M
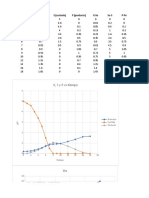
Fosfato TRIS
1 1
0.9 0.9
0.8 0.8
0.7 0.7
0.6 0.6
Alpha
0.5
Alpha
0.5
0.4
0.4
0.3
0.3
0.2
0.2
0.1
0.1
0
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 0
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
pH
pH
Acetato
1
0.9
0.8
0.7
Alpha 0.6
0.5
0.4
0.3
0.2
0.1
0
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
pH
You might also like
- Prueba Vibracion MecánicaDocument12 pagesPrueba Vibracion MecánicaMiguelNo ratings yet
- Dashboard EhsDocument3 pagesDashboard EhsElvis Wilbert Sahuma BautistaNo ratings yet
- Importancia cálculo integral aplicacionesDocument2 pagesImportancia cálculo integral aplicacionesDylan Navarro L100% (2)
- ASTM C 172 ResumenDocument2 pagesASTM C 172 ResumenJoelNo ratings yet
- Dashboard Indicadores Sso Avance MensualDocument3 pagesDashboard Indicadores Sso Avance MensualGonzalo CaroNo ratings yet
- Introducción Al PROMODELDocument36 pagesIntroducción Al PROMODELhectorsimula100% (3)
- Segundo Parcial de Operaciones de Transferencia de Masa IIDocument7 pagesSegundo Parcial de Operaciones de Transferencia de Masa IIjesusmachorroNo ratings yet
- Graficas de TitulacionDocument4 pagesGraficas de TitulacionGustavo Adolfo Rodriguez GasparNo ratings yet
- Ejercicio Extraccion Liq-LiqDocument19 pagesEjercicio Extraccion Liq-LiqKando Madrigal AlejandroNo ratings yet
- Datos para Elaborar Diagramas TDocument2 pagesDatos para Elaborar Diagramas TJared PérezNo ratings yet
- Excel de Linea de InfluenciaDocument36 pagesExcel de Linea de InfluenciaJonathan Yapo CalsinNo ratings yet
- Excel de Linea de InfluenciaDocument36 pagesExcel de Linea de InfluenciaBryan Yeison Onofre CachicatariNo ratings yet
- Acetato etilo agua acetona 30°C ejemplo 7-7 Ocon TojoDocument1 pageAcetato etilo agua acetona 30°C ejemplo 7-7 Ocon TojoJanice RicaldiNo ratings yet
- Diagrama Ternario Ac. de Etilo - Agua - Acetona A 30 °cDocument1 pageDiagrama Ternario Ac. de Etilo - Agua - Acetona A 30 °cJanice RicaldiNo ratings yet
- AttachmentDocument4 pagesAttachmentmariajrods31No ratings yet
- Mezcla Ternaria TareaDocument5 pagesMezcla Ternaria TareaTiliche MxNo ratings yet
- McCabe Tolueno-BencenoDocument4 pagesMcCabe Tolueno-BencenoKimberly Godoy VargasNo ratings yet
- 2da Clase Teoria Liq-Liq Fundamentos Op3Document12 pages2da Clase Teoria Liq-Liq Fundamentos Op3sselmerssNo ratings yet
- Problema 11.3 PropuestoDocument5 pagesProblema 11.3 PropuestoAbraham LópezNo ratings yet
- 11a - Clasificación de Cadenas de MarkovDocument21 pages11a - Clasificación de Cadenas de Markovjulissa milenaNo ratings yet
- QAA Curvas de ValoraciónDocument4 pagesQAA Curvas de ValoraciónmartinaNo ratings yet
- ENZIMOLDocument2 pagesENZIMOLDAYANA JAZMIN MERINO ANDRADENo ratings yet
- Presentación 2Document8 pagesPresentación 2Karla FelixNo ratings yet
- DitizonaDocument2 pagesDitizonaMaría Fernanda López DíazNo ratings yet
- Lectura QuintoDocument14 pagesLectura QuintoHugo Tarco ValenciaNo ratings yet
- Tabla Graficas - CANAL CIRCULARDocument1 pageTabla Graficas - CANAL CIRCULARMonica PintoNo ratings yet
- Titulación de AminoácidosDocument3 pagesTitulación de AminoácidosMeliangelisNo ratings yet
- Lectura TerceroDocument16 pagesLectura TerceroHugo Tarco ValenciaNo ratings yet
- Graficas SemiconductoresDocument10 pagesGraficas SemiconductoresSantiago GascaNo ratings yet
- LAMINA 1 Proyecto Dos Asai Norte 2 PDFDocument1 pageLAMINA 1 Proyecto Dos Asai Norte 2 PDFLuis Fernando RobledoNo ratings yet
- Dashboard Indicadores Sso Avance MensualDocument3 pagesDashboard Indicadores Sso Avance MensualJuan Angel ZuñigaNo ratings yet
- Dashboard Indicadores Sso Avance MensualDocument3 pagesDashboard Indicadores Sso Avance Mensualsamuel sanchezNo ratings yet
- Guia Primer CertamenDocument18 pagesGuia Primer CertamenjoseNo ratings yet
- Ejemplo de Preguntas de Examen Categoria I PDFDocument17 pagesEjemplo de Preguntas de Examen Categoria I PDFmaquiniadoNo ratings yet
- Dashboard Indicadores Sso Avance MensualDocument3 pagesDashboard Indicadores Sso Avance MensualSandor MirandaNo ratings yet
- Dashboard Indicadores Sso Avance MensualDocument3 pagesDashboard Indicadores Sso Avance MensualIngridNo ratings yet
- FísicaDocument3 pagesFísicaMichelle SaldivarNo ratings yet
- Extracción líquido-líquido: principios y aplicacionesDocument70 pagesExtracción líquido-líquido: principios y aplicacionesviviana velascoNo ratings yet
- De ProyectoDocument10 pagesDe ProyectoSilvana LópezNo ratings yet
- IsobarasDocument1 pageIsobarasJuan Camilo Lugo RojasNo ratings yet
- PRIMERO A - LECTURA y ESCRITURADocument25 pagesPRIMERO A - LECTURA y ESCRITURAHugo Tarco ValenciaNo ratings yet
- Laboratorio 2 Regresion Lineal Parte 2Document2 pagesLaboratorio 2 Regresion Lineal Parte 2laura farfanNo ratings yet
- Informe Spat BT Lourdes San IgnacioDocument8 pagesInforme Spat BT Lourdes San IgnacioJIM JOSEPH KEVIN SALFATE SUAREZNo ratings yet
- HierroDocument2 pagesHierronathalie uribe quirogaNo ratings yet
- Grafico Faury-JvtDocument2 pagesGrafico Faury-JvtNiní FigueroaNo ratings yet
- potenciometría ibuprofenoDocument5 pagespotenciometría ibuprofenoSabrina ElizondoNo ratings yet
- GraficoDocument1 pageGraficoCarmen RiveroNo ratings yet
- Ejercicios Curso Mantenimiento PredictivoDocument13 pagesEjercicios Curso Mantenimiento PredictivoRodrigo AlvarezNo ratings yet
- 1360-EMB-TAL-PAV-Sin NombreDocument1 page1360-EMB-TAL-PAV-Sin NombreMario MoralesNo ratings yet
- Graficas Lab 1Document2 pagesGraficas Lab 1Camila Camacho DiazNo ratings yet
- L4 Mezcla Acetona - Cloroformo Con Tablas y GraficasDocument10 pagesL4 Mezcla Acetona - Cloroformo Con Tablas y GraficasMinerva AguilarNo ratings yet
- Proyecto de AulaDocument6 pagesProyecto de AulaLindsy Paola Cantin SalcedoNo ratings yet
- Baca LolaDocument19 pagesBaca LolaFkl Porroa DaavidNo ratings yet
- Tabla Graficas - CANAL TRIANGULARDocument1 pageTabla Graficas - CANAL TRIANGULARMonica PintoNo ratings yet
- Lectura PrimeroDocument14 pagesLectura PrimeroHugo Tarco ValenciaNo ratings yet
- Reserva Nacional de TambopataDocument14 pagesReserva Nacional de Tambopatacarmela gamarra alagónNo ratings yet
- Proyecto Cadenas de MarkovDocument13 pagesProyecto Cadenas de MarkovLaura MarinNo ratings yet
- Bioingeniería ParámetrosDocument15 pagesBioingeniería ParámetrosIvana Cortés MárquezNo ratings yet
- Química 11 2doDocument6 pagesQuímica 11 2doDylan Navarro LNo ratings yet
- Guia Quimica Gladys PDFDocument4 pagesGuia Quimica Gladys PDFDylan Navarro LNo ratings yet
- Cómo afectan las redes sociales al cerebroDocument19 pagesCómo afectan las redes sociales al cerebroDylan Navarro LNo ratings yet
- Preguntas GenéticaDocument3 pagesPreguntas GenéticaDylan Navarro LNo ratings yet
- Analisisi Cronica de Una Muerte Anunciada PDFDocument2 pagesAnalisisi Cronica de Una Muerte Anunciada PDFDylan Navarro LNo ratings yet
- Notas Clase Propiedades de La Materia 2 PDFDocument23 pagesNotas Clase Propiedades de La Materia 2 PDFDylan Navarro LNo ratings yet
- Química Primer Guía Tercer PeriodoDocument7 pagesQuímica Primer Guía Tercer PeriodoDylan Navarro LNo ratings yet
- GUIA GEOMETRIA 7moDocument7 pagesGUIA GEOMETRIA 7moDylan Navarro LNo ratings yet
- Guia Quimica 3 OrganicaDocument3 pagesGuia Quimica 3 OrganicaDylan Navarro LNo ratings yet
- Generación de filtros de carbón activado a partir de biomasa forestalDocument8 pagesGeneración de filtros de carbón activado a partir de biomasa forestalDylan Navarro LNo ratings yet
- Codificación digital y genéticaDocument13 pagesCodificación digital y genéticaDylan Navarro LNo ratings yet
- Guia Quimica Gladys PDFDocument4 pagesGuia Quimica Gladys PDFDylan Navarro LNo ratings yet
- LF3196 - i-FRAME - IOM - SpanishLatinAmerica 1 PDFDocument150 pagesLF3196 - i-FRAME - IOM - SpanishLatinAmerica 1 PDFDylan Navarro LNo ratings yet
- Analisisi Cronica de Una Muerte Anunciada PDFDocument2 pagesAnalisisi Cronica de Una Muerte Anunciada PDFDylan Navarro LNo ratings yet
- Mapa Conceptual EcosistemaDocument1 pageMapa Conceptual EcosistemaDylan Navarro LNo ratings yet
- Tema 1 - La Materia 1Document32 pagesTema 1 - La Materia 1Dylan Navarro LNo ratings yet
- Division de AngulosDocument2 pagesDivision de AngulosDylan Navarro LNo ratings yet
- Tema 1 - El ÁtomoDocument22 pagesTema 1 - El ÁtomoDylan Navarro LNo ratings yet
- Informe Simulacion TanquesDocument4 pagesInforme Simulacion TanquesDylan Navarro LNo ratings yet
- Cromatografía intercambio iónico separa 4 sustanciasDocument4 pagesCromatografía intercambio iónico separa 4 sustanciasDylan Navarro LNo ratings yet
- Informe 6 Análisis IR Final 2020Document8 pagesInforme 6 Análisis IR Final 2020Dylan Navarro L100% (1)
- Presentación Control FinalDocument25 pagesPresentación Control FinalDylan Navarro LNo ratings yet
- Case Study - World Bank - Dylan Alexis Navarro LizcanoDocument4 pagesCase Study - World Bank - Dylan Alexis Navarro LizcanoDylan Navarro LNo ratings yet
- Japon ECYPI by Navarro, D PDFDocument13 pagesJapon ECYPI by Navarro, D PDFDylan Navarro LNo ratings yet
- Informe 4. Mezclas PDFDocument4 pagesInforme 4. Mezclas PDFDylan Navarro LNo ratings yet
- Informe Python-Simulink Reacción en CSTRDocument8 pagesInforme Python-Simulink Reacción en CSTRDylan Navarro LNo ratings yet
- Preinforme 7Document3 pagesPreinforme 7Dylan Navarro LNo ratings yet
- Ejercicio Cromatografía ColumnaDocument2 pagesEjercicio Cromatografía ColumnaDylan Navarro LNo ratings yet
- Informe 5 Navarro y Bonilla PDFDocument5 pagesInforme 5 Navarro y Bonilla PDFDylan Navarro LNo ratings yet
- 1201-18 - Construcción e Instalación de Pisos de Concreto Pretensado en Puente Peatonal Prototipo para BogotáDocument10 pages1201-18 - Construcción e Instalación de Pisos de Concreto Pretensado en Puente Peatonal Prototipo para BogotáEdwín Rodríguez100% (1)
- Causa Báez PDFDocument167 pagesCausa Báez PDFSerá JusticiaNo ratings yet
- Macro Matriz de Recursos SST 2023Document6 pagesMacro Matriz de Recursos SST 2023SARA LUCIA TANGARIFE PINEDANo ratings yet
- Fisicoquimica de los alimentos: reacciones gaseosas y cálculos termodinámicosDocument5 pagesFisicoquimica de los alimentos: reacciones gaseosas y cálculos termodinámicosaprendiz35No ratings yet
- Origen de La Constitucion de VenezuelaDocument15 pagesOrigen de La Constitucion de VenezuelaVinicio AndradeNo ratings yet
- Limites InfinitosDocument29 pagesLimites InfinitostmacspiderNo ratings yet
- Captura de Pantalla 2022-11-13 A La(s) 18.10.29Document8 pagesCaptura de Pantalla 2022-11-13 A La(s) 18.10.29camila belen toralesNo ratings yet
- Saneamiento AmbientalDocument13 pagesSaneamiento AmbientalThainette BurgosNo ratings yet
- Comunicado Del 20may2021 Actualizacion Datos PasivocolDocument15 pagesComunicado Del 20may2021 Actualizacion Datos PasivocolÂ'łëjő M'ōřēnôNo ratings yet
- Instalación de zócalos de vinílico flexible en hospitalDocument2 pagesInstalación de zócalos de vinílico flexible en hospitaldeyvisNo ratings yet
- La Madera en La ConstrucciónDocument25 pagesLa Madera en La ConstrucciónItzel Mac0% (1)
- Trabajo Final LoggiDocument73 pagesTrabajo Final LoggiMariana Shiary Saldivar BendezúNo ratings yet
- Determinacion Del Error de IndicacionDocument4 pagesDeterminacion Del Error de IndicacionJonathan Steven B RamirezNo ratings yet
- Ensayo de La Firma ElectrónicaDocument2 pagesEnsayo de La Firma ElectrónicaKRISTIAN RONALDO ZERON RODRIGUEZNo ratings yet
- EXPO (BJT) Transistor de Unión BipolarDocument3 pagesEXPO (BJT) Transistor de Unión Bipolarjesus natoNo ratings yet
- Aques MsicanotadahabaneraparapianoDocument12 pagesAques MsicanotadahabaneraparapianoBrahmsianistNo ratings yet
- Parasitos IntestinalesDocument9 pagesParasitos Intestinalesmorenorossi20039509No ratings yet
- TAREA I Música - ERIKAEUGENIDocument3 pagesTAREA I Música - ERIKAEUGENIErika EugeniNo ratings yet
- Taller Sobre La CrónicaDocument3 pagesTaller Sobre La CrónicaLaura Sofía TrujilloNo ratings yet
- Power Point Narrativa Pedagógica Práctica IIIDocument15 pagesPower Point Narrativa Pedagógica Práctica IIIMilagros LuceroNo ratings yet
- Definición e importancia de los grandes proyectosDocument6 pagesDefinición e importancia de los grandes proyectosYanneth VichegaNo ratings yet
- PSICOLOGÍA EMOCIÓN EXAMEN TIPODocument4 pagesPSICOLOGÍA EMOCIÓN EXAMEN TIPOAdyNo ratings yet
- Identificacion Puntos Criticos SI... +Document3 pagesIdentificacion Puntos Criticos SI... +cristian felipe ortega ceronNo ratings yet
- YAN-HS-STA-021 Control de Materiales y Químicos Peligrosos V 15Document14 pagesYAN-HS-STA-021 Control de Materiales y Químicos Peligrosos V 15ivan saldañaNo ratings yet
- Iumar 2023Document3 pagesIumar 2023fernando guillen telloNo ratings yet
- Taller de Matematica Con FosforosDocument31 pagesTaller de Matematica Con FosforosJavier100% (1)
- Capitulo 4Document52 pagesCapitulo 4Maria SarayNo ratings yet