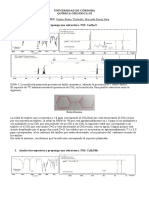
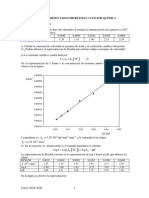
Professional Documents
Culture Documents
ENTREGADO Práctica 2, Preparación de Benzoe Por Catálisis Con Vitamina B A Partir de Benzaldehído
Uploaded by
Luis IslasOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
ENTREGADO Práctica 2, Preparación de Benzoe Por Catálisis Con Vitamina B A Partir de Benzaldehído
Uploaded by
Luis IslasCopyright:
Available Formats
PREPARACIÓN DE BENZOE POR CATÁLISIS CON VITAMINA B1 A PARTIR DE
BENZALDEHÍDO
Estefanía León Marmolejo, María Fernanda Amézaga González y Luis Alberto Ramírez Islas.
Universidad Autónoma de Ciudad Juárez, Instituto de Ciencias Biomédicas, Química Orgánica III,
Programa de Químico Farmacéutico Biólogo.
RESUMEN
<aszdxfgvhbjnkml,kmjnhbgvfcdxsza<Qszdxfgvhbjnkmjnhgfcdxsza<SZxdfcgvhbnjm
INTRODUCCIÓN reacción llega al equilibrio. Dado que la
velocidad de una reacción es en función de la
Los aldehídos se denominan
energía libre de activación, un catalizador actúa
compuestos carbónicos, donde el carbono
mediante la disminución de la altura de la
carboxílico siempre va unido a un átomo de
barrera cinética, por lo tanto, un catalizador
hidrógeno mientras que el enlace restante se
estabiliza el estado de transición con respecto a
une a un grupo alquilo o arilo. La única
la reacción no catalizada. (Voet & Voet, 2004)
excepción es el formaldehído que tiene dos
hidrógenos unidos al átomo de carbono del Existen distintos tipos de catálisis
grupo carbonilo. (Linstromberg, 1997) presentes dentro del cuerpo humano, sin
embargo, las cual incluye la utilización de dos
La benzoína o benzoe (C6H5-CH(OH)-
vitaminas del complejo B rusultan importantes,
CO-C6H5) es una sustancia cristalina con un
dentro del cuerpo humano, estas se presentan
punto de fusión de 193˚C (410 K) que reúne
en forma de pirofosfato de tiamina y el fosfato
propiedades tanto de alcoholes como de
de piridoxal; siendo las vitaminas B1 y B6
cetonas. La adición bezoínica o condensación
respectivamente. (Bender & Brubacher, 1977)
benzoínica es una reacción típica de los
aldehídos aromáticos en la que, a partir de dos OBJETIVO
moles de benzaldehído y bajo la influencia
Sintetizar benzoína en términos de química
catalítica del cianuro de potasio, en disolución
verde utilizando vitamina B1 como catalizado.
alcohólico-acuosa, resulta la benzoína. Sin
embargo, la condensación benzoínica MATERIALES Y MÉTODOS
catalizada con tiamina es una reacción de
“química verde”, ya que elimina el uso de un En un mortero se colocaron 15 pastillas de
reactivo sumamente tóxico y peligroso, el ion complejo B y se pulverizado con ayuda del
cianuro, el cual en la reacción tradicional no se pistilo. Después se agregó el polvo obtenido en
consume y requiere ser tratado para su un matraz Erlenmeyer de 125 ml y se añadió 4
disposición final. La tiamina, también llamada mL de agua destilada; se prosiguió a agitar el
vitamina B1, es un metabolito normal y no matraz hasta disolver lo más posible al polvo y
requiere de ningún tratamiento para su se filtró por gravedad dentro de un frasco de
disposición final. Adicionalmente, ya que la vidrio con tapa. Al residuo en el papel filtro, se
reacción se lleva a cabo a temperatura enjuago una vez con agua 1.0 ml y una vez con
ambiente en lugar de un reflujo, se disminuye 1.0 mL de NaOH al 10%. Al filtrado dentro de su
su impacto en las fuentes de energía. (Beyer & recipiente de vidrio, se le añadió 8 mL de etanol
Walter, 1997) al 95% y se agitó vigorosamente procurando
mezclar todo; también, 3 mL de hidróxido de
Se conoce a la catálisis como un proceso sodio al 10%, procurando mezclarlo lo más
que ayuda a aumentar la velocidad en que una posible; por último, se agregó 3 mL de
benzaldehído se mezcló muy bien por Tabla 2 Determinación de la cantidad de benzoe teórica al hacer
reaccionar 0.0494 mol de benzaldehído en un medio alcalino catalizado
aproximadamente 8 min. Se tapó la boca del con clorhidrato de tiamina.
envase de vidrio con papel parafil y la tapa de
recuperar (g)
sustancia de
estequiomét
Cantidad de
Cantidad de
Masa molar
él mismo; se cubrió por completo con papel
rica para la
formación
sustancia
(mol:mol)
de benzil
de benzil
obtenida
Relación
presente
teórica a
Masa de
Rubros
(g/mol)
benzil
benzil
(mol)
(mol)
canela para evitar el contacto con la luz y se
dejó reposar por tres noches. Al observar la
presencia de cristales, se destapó al envase.
Tras dos noches más, se obtuvieron los
Benzaldehído
cristales en un medio semilíquido; se colocaron 0.0494 2:1 0.0247 212.24 5.25
en un embudo Büchner sobre un papel filtro y
se filtró al vacío realizando cuatro lavados de
7.0 mL de agua y cuatro lavados de 7.0 mL de
etanol alternando cada lavado. Finalmente se Tabla 3 Rendimiento porcentual de la reacción. Se obtuvo un
rendimiento de 47.9790%
realizó un último par de lavados, 5 ml de agua y
5 ml de etanol de 5 mL. Rubros Datos numéricos
RESULTADOS Y DISCUSIÓN Masa de benzaldehído obtenido (g) 2.5189
Masa de benzaldehído teórica (g) 5.25
Debido a que el clorhidrato de tiamina solo
Rendimiento porcentual (%) 47.9790
funciona como catalizador, tanto el hidróxido de
sodio y el metanol funcionan como medio de
reacción, no son considerados para determinar En cuanto al rendimiento obtenido, todas
el rendimiento de la reacción. La Tabla 1 indica las referencias indican un rendimiento bastante
la cantidad de sustancia expresada en mol de bajo. Primeramente, se encontró que un
benzaldehído. Debido a que realmente solo hay rendimiento del 48% (Pachova, 2013); mientras
un reactivo, no es necesario estimar el reactivo que otro documento indica un rendimiento un
limitante, solamente la cantidad teórica de tanto menor siendo del 30% (Lampan & Chriz,
producto a obtener, tal como se muestra en la 1982). Un rendimiento de 47.9790% puede
Tabla 2. Por último, se comparó los 2.5189 g deberse a la utilización de proporciones
obtenidos tras la síntesis, los lavados y el estequiométricas que favorecieron la obtención
secado de los cristales (Imagen 1) tal como se del producto y es prácticamente igual al
muestra en la Tabla 3. El Mecanismo de consultado en una fuente, por lo que se puede
reacción se detalla como Anexo al final. afirmar que fue una síntesis satisfactoria
teniendo en cuenta la naturaleza reversible de
la reacción.
Tabla 1 Determinación de la cantidad de sustancia, expresada
en mol, de benzaldehído presente para la reacción. Existen diferentes tipos de benzoin, los
Cantidad cuales son cetonas α-hidroxilados, los cuales
Masa
Masa de
Rubros
Volume Densida
pesad
molar
sustancia
son propiamente formados a través de la
n (ml) d (g/ml) (g/mol
a (g)
)
presente condensación benzoica. Existen formas
n (mol)
Benzaldehíd generales para la condensación benzoica; la
5 1.05 5.25 106.12 0.0494
o más antigua se fundamente en la utilización de
anión cianuro como medio para formar una
cianohidrina capaz de producir las
subsecuentes modificaciones a la molécula
para propiciar la reacción. (Rodríguez Yunta &
Gómez Contreras, 2008) Por otra parte, se
puede utilizar una sal de tiazolio para atacar el
carbono carbonilo y servir como un conector
entre las dos moléculas de benzaldehído. De Pachova, T. (2013). Benzoin condensation
hecho, al utilizar la vitamina B1, la mayor catalyzed by thiamine . Ginebra: Université de
participación de la molécula se da en su anillo Genève.
de cinco miembros dispuesto en una forma 1,3
Rodríguez Yunta, M. J., & Gómez Contreras, F.
de nitrógeno y azufre. (March, 1992)
(2008). Curso experimental en Química
Como prueba de identificación se realizó Orgánica. Medrid: Editorial Síntesis.
su determinación de punto de fusión, el cual
Voet, D. & Voet, J. (2004). Bioquímica.
resultó de 132 ˚C, el cual se encuentra muy
Uruguay: Panamericana. Pág. 513.
cerca de lo esperado, ya que las hojas de
seguridad indican un punto de fusión de entre
130 y 135 ˚C. También, se realizó una
cromatografía de capa fina, sin embargo, no se
encontraron datos en la bibliografía con los
mismos solventes ni en placa de sílice, por lo Bibliografía
que no son representativo para determinar la Carey, F. A. (2006). Química orgánica. México: McGraw-
correcta síntesis. Aunque, el punto de fusión es Hill.
buen indicador de la correcta síntesis de Lampan, L., & Chriz, G. M. (1982). Introduction to
benzoe. La Tabla 4 indica la relación de frentes organic lab technique. College Publishing : New
de la cromatografía realizada. York.
March, J. (1992). Advanced Organic Chemistry. New
York: Jonh Wiley & Sons.
CONCLUSIONES
McMurry, J. (2008). Química orgánica. D.F.: Cengage
Learning.
Bibliografía
Pachova, T. (2013). Benzoin condensation catalyzed by
Bender, M. & Brubacher, L. (1977). Catálisis y thiamine . Ginebra: Université de Genève.
acción enzimática. España: Reverté, S.A. Pág.
Rodríguez Yunta, M. J., & Gómez Contreras, F. (2008).
5
Curso experimental en Química Orgánica.
Beyer, H. & Walter, W. (1997). Manual de Medrid: Editorial Síntesis.
química orgánica. Barcelona: Reverté, S.A. Wade, L. (2011). Química orgánica. Volumen 2. México:
Pág. 567-568 Pearson Educación.
Lampan, L., & Chriz, G. M. (1982). Introduction
to organic lab technique. College Publishing:
New York.
Linstromberg, W. (1997). Curso breve de
química orgánica. España: Reverté, S.A. Pág.
219
March, J. (1992). Advanced Organic Chemistry.
New York: Jonh Wiley & Sons.
ANEXO
Mecanismo de la síntesis de benzoin, también conocido como benzoe, a partir de benzaldehído
mediante condensación benzoica utilizando clorohidrato de tiamina, forma comercial de la vitamina B1,
como catalizador. Se observa que el medio alcalino propicia la reacción al desestabilizar el anillo de
tiazol, el anillo de cinco miembros con nitrógeno y azufre dispuestos en una forma “1,3”.
You might also like
- 9 Constantes de EstabilidadDocument14 pages9 Constantes de EstabilidadAleiozNo ratings yet
- Sol Ex P Cq312 19-2Document3 pagesSol Ex P Cq312 19-2Elvis RenzoNo ratings yet
- Informe FQ 7 (1) .Docx Solubilidad y TermodinámicaDocument4 pagesInforme FQ 7 (1) .Docx Solubilidad y TermodinámicaAighself100% (1)
- Curso de HPLC Ecuacion de Van DeemterDocument32 pagesCurso de HPLC Ecuacion de Van Deemteralextm89No ratings yet
- Mapa Conceptual de Las Herramientas Que Pueden Ser Utilizadas Como Material Didáctico para La Enseñanza en El Área de La Química.Document1 pageMapa Conceptual de Las Herramientas Que Pueden Ser Utilizadas Como Material Didáctico para La Enseñanza en El Área de La Química.urielNo ratings yet
- Determinación Ksp Ca(OH)2Document3 pagesDeterminación Ksp Ca(OH)2Edwin Guerrero CRNo ratings yet
- Informe 0, Bioquímica.Document6 pagesInforme 0, Bioquímica.Fernanda RodriguezNo ratings yet
- Absorb An CIADocument22 pagesAbsorb An CIANayeli Romero VirruetaNo ratings yet
- Complexometria 1Document3 pagesComplexometria 1Jenny QuingaNo ratings yet
- Tarea 3Document1 pageTarea 3Andrea MuñozNo ratings yet
- Carbonatos y Fosfatos Informe 0956956Document7 pagesCarbonatos y Fosfatos Informe 0956956Jose_Warrner_H_7234No ratings yet
- Técnicas analíticas de separación. Electroforesis CapilarDocument2 pagesTécnicas analíticas de separación. Electroforesis CapilarDani MateoNo ratings yet
- Potenciometria InformeDocument12 pagesPotenciometria InformeDiego WettigNo ratings yet
- Superconductor BiBa2Cu3O7Document6 pagesSuperconductor BiBa2Cu3O7Alejandra Balaguera TorresNo ratings yet
- Redox titulaciones potenciométricasDocument11 pagesRedox titulaciones potenciométricasVanessa SánchezNo ratings yet
- Informe Final de Sintesis Quimica OrganicaDocument4 pagesInforme Final de Sintesis Quimica OrganicaMaría Paula RincónNo ratings yet
- Química orgánica III: Estructuras de butirofenona y 4-bromo butironitriloDocument2 pagesQuímica orgánica III: Estructuras de butirofenona y 4-bromo butironitrilosara mercadoNo ratings yet
- Electrogravimetria y ColumbimetríaDocument5 pagesElectrogravimetria y Columbimetría05-FB-HU-EDISON PEREZ PAUCARNo ratings yet
- LABORATORIO 1 Cromatografia de Exclusión BQ IDocument2 pagesLABORATORIO 1 Cromatografia de Exclusión BQ IJaviera CaneloNo ratings yet
- Nitración Del Ácido SalicílicoDocument4 pagesNitración Del Ácido SalicílicoNitgma DcNo ratings yet
- G01 - Informe X (Extraccion)Document3 pagesG01 - Informe X (Extraccion)Victor Aristizabal100% (1)
- AnaliticaDocument1 pageAnaliticaSayuriNo ratings yet
- Cuantificación de compuestos por cromatografíaDocument30 pagesCuantificación de compuestos por cromatografíaIng Ronald Portales0% (1)
- Simetria de Moleculas Simples - Propiedades Vibracionales y Orbitales MolecularesDocument15 pagesSimetria de Moleculas Simples - Propiedades Vibracionales y Orbitales MolecularesJACKELINE SALGADO PALACIONo ratings yet
- Ejercicios Segundo Parcial Química Analítica-1Document2 pagesEjercicios Segundo Parcial Química Analítica-1Fidel TorresNo ratings yet
- Creando entrada Gaussian H2O2Document6 pagesCreando entrada Gaussian H2O2Maria NavasNo ratings yet
- Capítulo 4 Medición de La Capacidad de Intercambio CatiónicoDocument50 pagesCapítulo 4 Medición de La Capacidad de Intercambio CatiónicoDouglas Sánchez100% (1)
- Informe FotocolorimetriaDocument8 pagesInforme FotocolorimetriahemilyNo ratings yet
- Análisis de Una Mezcla de Carbonato y BicarbonatoDocument4 pagesAnálisis de Una Mezcla de Carbonato y BicarbonatoValentina CardenasNo ratings yet
- Informe de Lab Oratorio de Analisis Instrumental Cromatografia de Gases 2Document5 pagesInforme de Lab Oratorio de Analisis Instrumental Cromatografia de Gases 2Oscar Armando Perez BenitezNo ratings yet
- Un Experimento Colorimétrico de Cinética QuímicaDocument2 pagesUn Experimento Colorimétrico de Cinética Químicajulian David PatiñoNo ratings yet
- TP 1 y 2 Preparacion y Normalizacion de HCL y Mezclas AlcalinasDocument5 pagesTP 1 y 2 Preparacion y Normalizacion de HCL y Mezclas AlcalinasLuis PeredoNo ratings yet
- P3. Determinación de La Constante de Disociación de Un Indicador Ácido-BaseDocument6 pagesP3. Determinación de La Constante de Disociación de Un Indicador Ácido-BaseSasha CastellanosNo ratings yet
- Catalisis Como Pilar Fundamental en Quimica VerdeDocument13 pagesCatalisis Como Pilar Fundamental en Quimica Verdeleonard1613LSNo ratings yet
- Cloruros FinalDocument11 pagesCloruros FinalFabiola Del Pilar CuroNo ratings yet
- Compuestos de OrganopaladioDocument51 pagesCompuestos de OrganopaladioEder Yair Nolasco TerrónNo ratings yet
- Determinación de Cloruros InfDocument5 pagesDeterminación de Cloruros InfDaniel AlexanderNo ratings yet
- Pre 3 FQ2Document8 pagesPre 3 FQ2Lesli RamirezNo ratings yet
- Informe ChalconasDocument3 pagesInforme ChalconasAndrés OrtizNo ratings yet
- Practica 3 Separacion e Identificacion de Aminoacidos Por Cromatografia en Capa FinaDocument14 pagesPractica 3 Separacion e Identificacion de Aminoacidos Por Cromatografia en Capa FinaDiego MartinezNo ratings yet
- Práctica 2 BenzoínaDocument9 pagesPráctica 2 BenzoínaIrene NdnxnNo ratings yet
- Laboratorio Kps 2016Document5 pagesLaboratorio Kps 2016Madelyn Garrido VillarrealNo ratings yet
- Practica No. 4-Guía-Análisis de Mezclas Por EspectrofotometríaDocument4 pagesPractica No. 4-Guía-Análisis de Mezclas Por EspectrofotometríaDaniel AlfonsoNo ratings yet
- Articulo Difraccion Cu PDFDocument4 pagesArticulo Difraccion Cu PDFLucía HernándezNo ratings yet
- Problemario 2 Capítulo 7 y 12Document3 pagesProblemario 2 Capítulo 7 y 12Karim 'SolizNo ratings yet
- Sintesis AsimetricaDocument9 pagesSintesis AsimetricaJosselyn MaldonadoNo ratings yet
- Electrodo de Membrana Líquida para CalcioDocument2 pagesElectrodo de Membrana Líquida para CalcioDianaa Isabella Fernandez0% (1)
- La AcetanilidaDocument5 pagesLa Acetanilidadilmer salcedo0% (1)
- Practica #IV Identificación, Cuantificación Del Grupo de Las XantinasDocument19 pagesPractica #IV Identificación, Cuantificación Del Grupo de Las XantinasRoberto Esponda VelásquezNo ratings yet
- Síntesis de isómeros cis y trans de cloruro de diclorobis(etilendiamina) cobalto(IIIDocument11 pagesSíntesis de isómeros cis y trans de cloruro de diclorobis(etilendiamina) cobalto(IIIWENDY NATHALIA ROJAS ARCENo ratings yet
- Teoria de DebyeDocument3 pagesTeoria de DebyeJulio David Garcia0% (1)
- Practica #4 Sintesis Del YodoformoDocument3 pagesPractica #4 Sintesis Del YodoformoGabriel ArturoNo ratings yet
- Solucion Leccion 6Document15 pagesSolucion Leccion 6DanielNo ratings yet
- ImformeDocument5 pagesImformeAnonymous MVMOeliIRzNo ratings yet
- CRISTALOGRAFIADocument3 pagesCRISTALOGRAFIAGloria SolarteNo ratings yet
- Informe 1 - Benzocaina - RetrosintesisDocument10 pagesInforme 1 - Benzocaina - RetrosintesisCamilo SerranoNo ratings yet
- Obtención de Benzoína A Partir de BenzaldehídoDocument11 pagesObtención de Benzoína A Partir de BenzaldehídoAlanna CruzNo ratings yet
- Obtención de Benzoina a partir de BenzaldehídoDocument3 pagesObtención de Benzoina a partir de BenzaldehídoIrvin AdunaNo ratings yet
- PracticaNo. 4 LQOIIDocument10 pagesPracticaNo. 4 LQOIIXimenaNo ratings yet
- Práctica β - naftíl metílicoDocument6 pagesPráctica β - naftíl metílicoJosé OchoaNo ratings yet
- Practica 1 RamirezDocument2 pagesPractica 1 RamirezLuis IslasNo ratings yet
- Mendez Practica 6Document3 pagesMendez Practica 6Luis IslasNo ratings yet
- Monoslide SPDocument9 pagesMonoslide SPLuis IslasNo ratings yet
- Extracción de Identificación de Cafeína en SodasDocument5 pagesExtracción de Identificación de Cafeína en SodasLuis IslasNo ratings yet
- UntitledDocument107 pagesUntitledapi-113270435No ratings yet
- Guia Nacional de Cadena de CustodiaDocument42 pagesGuia Nacional de Cadena de Custodiaisvero75% (4)
- Sobre La CafeínaDocument130 pagesSobre La CafeínaLuis IslasNo ratings yet
- EstereoquímicaDocument36 pagesEstereoquímicaLuis IslasNo ratings yet
- PrácticaDocument2 pagesPrácticaLuis IslasNo ratings yet
- HALOGENUROSDEALQUILO PPTDocument138 pagesHALOGENUROSDEALQUILO PPTJesus Francisco DuarteNo ratings yet
- BQI-Lab Práctica 13Document3 pagesBQI-Lab Práctica 13Luis IslasNo ratings yet
- BQI-Lab Práctica 12Document4 pagesBQI-Lab Práctica 12Luis IslasNo ratings yet
- Microbiología I 3Document8 pagesMicrobiología I 3Luis IslasNo ratings yet
- BQI-Lab Práctica 13Document3 pagesBQI-Lab Práctica 13Luis IslasNo ratings yet
- BQI-Lab Práctica 13Document3 pagesBQI-Lab Práctica 13Luis IslasNo ratings yet
- Microbiología IDocument5 pagesMicrobiología ILuis IslasNo ratings yet
- BQI-Lab Práctica 12Document4 pagesBQI-Lab Práctica 12Luis IslasNo ratings yet
- Microbiología IDocument4 pagesMicrobiología ILuis IslasNo ratings yet
- Microbiología IDocument5 pagesMicrobiología ILuis IslasNo ratings yet
- Los Conceptos Lacanianos en La Enseñanza de La PsicopatologíaDocument3 pagesLos Conceptos Lacanianos en La Enseñanza de La PsicopatologíaJonatan CasteloNo ratings yet
- Las Técnicas de Trabajo de La PorcelanaDocument44 pagesLas Técnicas de Trabajo de La PorcelanaCarlos Mendoza67% (6)
- Prácticas EncoderDocument6 pagesPrácticas EncoderJonathan Fernando Amaguaña SimbañaNo ratings yet
- Piel sensible: cuidados y productos indicadosDocument5 pagesPiel sensible: cuidados y productos indicadosJenifer IsabelNo ratings yet
- Contrato Compraventa Bienes MueblesDocument3 pagesContrato Compraventa Bienes MueblesArizbeth VázquezNo ratings yet
- 23 - Marcos 8 1-21 Evidencias Que Exigen Una RespuestaDocument4 pages23 - Marcos 8 1-21 Evidencias Que Exigen Una RespuestaAndresAlbaNo ratings yet
- Ortografía 1. CorrecciónDocument2 pagesOrtografía 1. Correccióngespadas075No ratings yet
- Ética psicólogo casosDocument2 pagesÉtica psicólogo casosTronningunNo ratings yet
- Repaso de Sistema de ContabilidadDocument3 pagesRepaso de Sistema de ContabilidadYolanda PeñaNo ratings yet
- Guia Anestesia EutanasiaDocument34 pagesGuia Anestesia EutanasiaAdballahbenAsshadNo ratings yet
- Tecnicas de Relajacion para Sexto de PrimariaDocument5 pagesTecnicas de Relajacion para Sexto de PrimariaShirley VelezNo ratings yet
- Secuencia de FuncionesDocument22 pagesSecuencia de FuncionesProf. Silvia MartinezNo ratings yet
- Planeación - S4 IntegradoDocument7 pagesPlaneación - S4 IntegradoCar GonzálezNo ratings yet
- Taller 4Document3 pagesTaller 4Jessica Marin0% (1)
- Byung Chul HanDocument3 pagesByung Chul HanStella RegisNo ratings yet
- DipnoosDocument4 pagesDipnoossobijezixiNo ratings yet
- Tarea # 5 Tejido Vegetal y AnimalDocument6 pagesTarea # 5 Tejido Vegetal y AnimalAbel SantosNo ratings yet
- Informe de Gestion Salud Mental 2018Document13 pagesInforme de Gestion Salud Mental 2018carlos alberto coronado zapataNo ratings yet
- Guia de AP 9 Religion 3 PeriodoDocument8 pagesGuia de AP 9 Religion 3 PeriodoXtian LopezNo ratings yet
- Las Emociones en El DiscursoDocument21 pagesLas Emociones en El DiscursoMaría Villamizar Salas100% (1)
- Biografia Jose BonaparteDocument2 pagesBiografia Jose BonaparteLuchi GianoliniNo ratings yet
- Resumenes I y N-2Document12 pagesResumenes I y N-2Luvianka GradoNo ratings yet
- Pie de CuestasDocument3 pagesPie de CuestasCarne De pezNo ratings yet
- Obtencion de PigmentosDocument5 pagesObtencion de PigmentosCARLOS DANIEL VARAS CALANINo ratings yet
- Brucelosis y TriquinosisDocument8 pagesBrucelosis y TriquinosisFelipe Ignacio Alveal VásquezNo ratings yet
- Medidas de Dispersion #3Document17 pagesMedidas de Dispersion #3Diana Elena Sanchez RosalesNo ratings yet
- Jacques-Alain Miller - Una Nueva Modalidad Del SíntomaDocument13 pagesJacques-Alain Miller - Una Nueva Modalidad Del SíntomafabioazeredoNo ratings yet
- 1-Nuestro SimboloDocument11 pages1-Nuestro SimboloJP Vega GarciaNo ratings yet
- Directorio TelefonicoDocument2 pagesDirectorio TelefonicoAnayeli De Horta RodríguezNo ratings yet