Professional Documents
Culture Documents
Introduccion A Las Enzimas
Uploaded by
Manuel Alejandro PeñafielOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Introduccion A Las Enzimas
Uploaded by
Manuel Alejandro PeñafielCopyright:
Available Formats
Introduccin a las enzimas. Unidades de actividad.
La cintica de Henri-Michaelis-Menten. Determinacin de parmetros.
Temario
Aspectos moleculares de las reacciones enzimticas: sustrato, centro activo, enzimas
como protenas complejas, grupos prostticos, coenzimas. Medida de la actividad enzimtica:
definicin de unidades y mtodos de medida.
Cintica de las reacciones enzimticas: velocidad inicial de reaccin (v 0), dependencia
de la velocidad inicial con la concentracin de enzima y sustrato. Ecuacin de Michaelis-
Menten. Representaciones grficas. Nmero de recambio, k cat. Constante efectiva kcat/Km. La
constante de Michaelis (kM): supuestos fundamentales, ecuacin y significado fsico de los
distintos parmetros cinticos. Transformaciones de la ecuacin de Michelis-Menten;
representaciones grficas.
Preguntas conceptuales
1. Cules son los aspectos caractersticos de las reacciones enzimticas? Qu propiedades
presentan las enzimas que las diferencian de otros catalizadores?
2. Es cierto que todas las enzimas conocidas son de naturaleza proteica?
3. Cul es la diferencia entre el complejo activado y el complejo enzima-sustrato?
4.Qu tipo de interacciones se ejercen entre la enzima y el sustrato para formar el complejo
ES?
5. Qu es la constante de Michaelis? Porque es importante medirla?
6. Definan Ks y kcat.
7. Para una reaccin monosustrato A B, defina las condiciones en que kM=Ks. Describa
condiciones en las cuales esto no sea cierto.
8. Cul es la aproximacin del estado estacionario y bajo que condiciones es vlido?
9. Cul es el orden de reaccin, con respecto al sustrato, de una reaccin enzimtica
monosustrato?
10. Bajo qu condiciones podemos asegurar que medimos velocidades iniciales? Puede
medirse velocidad inicial fuera de estas condiciones?
11. Cmo vara la velocidad inicial para [S]<<k M y para [S]>>k M? Qu utilidad tiene trabajar
en estas condiciones?
12. Cul es el valor estimado de la concentracin fisiolgica de sustratos? Justifique.
13. Mencione un parmetro que mida las siguientes caracteristicas de una enzima: i.
especificidad ii. Eficiencia de la catlisis iii. Afinidad por el sustrato
Problemas
1. Se estudi la actividad de la enzima D-gliceraldehdo 3-fosfato desdhidogenasa de un
organismo mesfilo y de otro hipertermfilo. Los resultados de tal estudio se muestran en
el siguiente grfico
Podra explicar el comportamiento diferencial de ambas enzimas en funcin de la
temperatura? Por qu la actividad de la enzima mesfila es mayor a 20 grados que la
actividad de la hipertermfila?
2. Explique claramente el significado de los siguientes parmetros.
a. kcat
b. Km
c. Kcat/Km
3 Esquematice la energa de activacin para una reaccin enzimtica
E+S ES E+P
Cuando se cumplen las siguientes condiciones:S>>>Km y S<<<Km.
4 En un experimento se modific qumicamente un sustrato para modificar las constantes de
unin del mismo en una enzima especfica. A continuacin se mencionan las constantes que
se modificaron selectivamente:
a. G de unin del sustrato
b. G de unin del sustrato y del estado de transicin (ES* 2)
c. G de unin del estado de transicin
Para evaluar el efecto de tal procedimiento se midieron kcat, Km y kcat/km. Explique como se
modificarn estos parmetros para cada uno de los casos expuestos.
5 La quimotripsina es una endopeptidasa que reconoce a aminocidos aromticos (Phe, Tyr y
Trp). Se estudiaron distintos parmetros cinticos de la quimotripsina en funcin de distintos
sustratos. A continuacin se muestran los resultados:
Sustrato Kcat(s-1) Km(mM) Kcat/Km (s-1 M-1)
Pep-Tyr-NH2 0.17 32 5
Pep-Tyr-Gly-NH2 0.64 23 28
Pep-Tyr-Ala-NH2 7.5 17 440
Pep-Phe-NH2 0.06 31 2
Pep-Phe-Gly-NH2 0.14 15 11
Pep-Phe-Ala-NH2 2.8 25 114
Qu conclusiones puede sacar de tal estudio?
6 Se desea medir la actividad de una enzima tipo esterasa que acta sobre butirato de etilo.
Una forma de seguir el curso de la reaccin es por medida del consumo de NaOH necesario
para mantener el pH constante a 8.5. Cmo definiran entonces una unidad arbitraria de
actividad para esta enzima? Propongan otra forma de medir la actividad y definan otra unidad
de actividad.
7 Se quiere medir la actividad de la enzima hexoquinasa, que cataliza la reaccin:
Mg+2
Glucosa + ATP glucosa-6-P + ADP
hexoquinasa
El mtodo utilizado consiste en medir la formacin de glucosa-6-P a travs de su oxidacin
instantnea, segn la siguiente reaccin:
G-6-P deshidrogenasa
Glc-6-P + NADP+ 6-P-gluconato + NADPH + H+
Como NADPH muestra absorcin de luz UVa 340nm (340=6.3x106 cm2/mol), se puede
seguir entonces el curso de la reaccin por espectrofotometra UV. Se prepar una mezcla de
reaccin con concentraciones saturantes de todos los sustratos. La reaccin se inici con
agregado de hexoquinasa directamente en una cuveta de cuarzo (1 cm de paso de luz). Se
obtuvieron los siguientes datos:
Tiempo (min) 0 1 2 3 4 5
A340 0.054 0.177 0.302 0.422 0.548 0.670
a. Cul fue la velocidad inicial de reaccin?
b. Calculen las unidades internacionales (UI) de hexoquinasa que hay en 1 ml de mezcla de
reaccin.
c. Definan otra unidad arbitraria de actividad enzimtica de hexoquinasa y calculen segn
ella las unidades de enzima presentes en 1 ml de mezcla de reaccin.
8 La creatina quinasa cataliza la siguiente reaccin:
creatina + ATP Creatina-P + ADP kM (creatina): 1.6x10 -2 M
+2
Mg
a. De acuerdo al valor de la constante de equilibrio de la reaccin, a pH 8.0 y 25 C, un 87%
de la creatina se encuentra como creatina-P. Si a la mezcla de esta reaccin se agrega la
enzima (sin cambiar las otras condiciones), podran decir qu porcentaje de creatina-P habr
cuando se alcance el equilibrio?
b. Si luego de alcanzado el equilibrio se agrega creatina-P radioactiva ( 32P), se incorporar
32
P en el ATP?
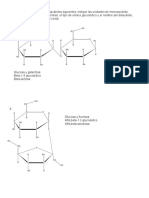
9 La enzima -galactosidasa cataliza la hidrlisis de -galactsidos (derivados de galactosa
en configuracin beta). La reaccin natural catalizada es:
-D-galactopiranosil (1-4) -D-glucopiranosa D-glucopiranosa + D-
galactopiranosa
Dado que resulta un tanto complicado seguir el curso de la reaccin a travs de la deteccin
de sustratos o productos de la reaccin natural, se reemplaza la sacarosa por un sustrato
artificial, el o-nitrofenil--D-galactopiransido (ONPG, PM = 318 g/mol). La hidrlisis de ONPG
produce D-galactosa y o-nitrofenol (ONP). ONP absorbe luz a 420 nm, en solucin alcalina.
El ensayo de actividad de -galactosidasa se realiza en buffer fosfato de potasio 50
mM pH 6.6 que contiene Mn+2 0.1 mM (cofactor). La reaccin se lleva a cabo a 37 C y se
inicia con el agregado de la muestra con enzima. La produccin de ONP se determina
colorimtricamente; se toman 0.7 ml de la mezcla de reaccin y se descargan sobre 0.35 ml
de Na2CO3 1M (Para qu?). Luego de 10 min se puede medir A420. La ley de Lambert-Beer es
vlida para [ONP entre 0.02 y 0.3 mM en el tubo de colorimetra. El coeficiente de
absortividad de ONP a 420 nm es 4500 M-1cm-1.
Se define la Unidad enzimtica de -galactosidasa: 1 UG como la cantidad de enzima
que produce un cambio de absorbancia a 420 nm en el tubo de colorimetra de 0.1 por minuto,
cuando la reaccin se lleva a cabo a 37 C y [ONPG = 1.5 mg/ml, al comienzo de la reaccin.
Para determinar la actividad de una preparacin de -galactosidasa, se hicieron los
siguientes ensayos:
Primer prueba: volumen de reaccin = 10 ml, [ONPG = 1.5 mg/ml. Se inici la
reaccin con 10 l de preparacin enzimtica. A los pocos segundos, la primer muestra de la
mezcla de reaccin tom coloracin amarilla muy intensa cuando se la agreg sobre Na 2CO3
1M (es decir A420 fue > 1.0).
Segunda prueba: volumen de reaccin = 5 ml, [ONPG = 1.5 mg/ml. Se diluy la
preparacin enzimtica 1/10 en buffer de reaccin, y se inici la reaccin con 2 l de la
dilucin. Los resultados fueron:
t (min) 0 1 2 3 4 5
A420 0.059 0.370 0.690 0.828 0.895 0.930
Tercer prueba: volumen de reaccin = 5 ml, [ONPG = 1.5 mg/ml Se diluy la
preparacin enzimtica 1/100 en buffer de reaccin, y se inici la reaccin con 5 l de la
dilucin. Entonces, se obtuvo:
t (min) 0 1 2 3 5 6 8 10
A420 0.062 0.138 0.222 0.291 0.380 0.423 0.451 0.462
a. Porqu se hicieron estas tres determinaciones de actividad sobre la misma muestra?
b. Cul es la actividad de la preparacin enzimtica?
c. Cuntas UG se usaron entonces para la prueba 3?
10 Se ha medido la actividad de una preparacin de invertasa en 10 ml totales de una mezcla
de reaccin con sacarosa 0.1 M y buffer acetato 0.02 M, pH 4.77 (k M = 0.061M). Al cabo de 20
minutos se han hidrolizado 18 moles de sustrato. Cmo explican que hasta ese momento la
velocidad de reaccin se haya mantenido constante, a pesar que se consumi sustrato?
Justifiquen su respuesta con datos cuantitativos.
11 Se quiere medir los parmetros cinticos de la enzima invertasa de un extracto de levadura
comercial. Esta enzima cataliza la siguiente reaccin:
sacarosa + H20 glucosa + fructosa
Para ello se realiz el experimento diagramado a continuacin:
Mezcla de reaccin 1 2 3
Buffer HAc-NaAc 0.02 M , pH 4.77 2 ml 2 ml 2 ml
Sacarosa 0.5 M - - 2 ml
Sacarosa 0.05 M 2 ml 4 ml -
Extracto enzimtico 0.4 ml 0.4 ml 0.4 ml
H20 5.6 ml 3.6 ml 5.6 ml
Las tres mezclas de reaccin se incubaron a 20 C
min (1) (2) (3) tomndose muestras de 1 ml a 2, 5, 7 y 10 min de iniciada
2 1.6 2.0 3.9 la incubacin. Sobre las muestras se determin la
5 3.7 4.5 9.0 cantidad de moles de sacarosa transformada en 10 ml de
7 5.5 6.3 12.6 mezcla de reaccin. Los resultados figuran en la tabla a la
10 5.5 9.0 18.2 izquierda.
a. Calculen vmx y kM a partir de un grfico 1/v 0 en funcin de 1/[S].
b. Calculen las unidades de invertasa contenidas en los 0.4 ml de extracto enzimtico, de
acuerdo a una unidad de actividad enzimtica que deben definir previamente.
12 Los siguientes datos se midieron para la reaccin S P catalizada enzimticamente:
[S] (M) v0 (nmoles/l x min)
6.25x10-6 15.00
7.50x10-5 56.25
1.00x10-4 60.00
1.00x10-3 74.90
1.00x10-2 75.00
a. Determinar vmx y kM.
b. Cul sera v0 si [S] = 2.5x10 -5 M? Y para [S] = 5.0x10 -5 M? Y si en cambio [S] = 2.5x10 -5
M pero la concentracin de enzima es el doble de la original?
c. Cul es la proporcin de enzima libre cuando [S] es 1.0x10 -2 M? Y cuando [S] es 6.25x10 -
6
M?
e- La velocidad dada en la tabla se determin midiendo la concentracin de producto
acumulado en un perodo de 10 min. Es vlida la suposicin de que estos valores de v
representan las velocidades iniciales en todo el rango de [S] utilizado?
13. La siguiente tabla muestra los resultados obtenidos al determinar K M y vmax para 3
isoenzimas. En todos los casos se utilizaron las mismas condiciones de reaccin (pH, T,
fuerza inica). En todos los casos el volumen final de la reaccin fue de 10 ml y se agreg
enzima hasta una concentracin final de 1x10 -11 M.
Isoenzima KM (mM) vmax (mol/min)
A 2 4
B 0.5 0.8
C 0.1 0.35
a. En base a estos datos, cul isoenzima tiene mayor afinidad por el sustrato? Justifiquen.
b. Cul de las tres isoenzimas tiene mayor nmero de recambio?. Fundamenten.
14 Una enzima microbiana se uso en un extenso trabajo de mutagnesis dirigida con el objeto
de modificar sus propiedades cinticas. A continuacin se muestran los distintos reemplazos
ensayados y las modificaciones en kcat y en Km. La columna Mutante indica el aminocido
original, su posicin y el aminocido que lo reemplaza.
Mutante Kcat (s-1) Km(microM)
Nativa 310 137
His58Ala 9.8 134
His58Tyr 5.4 139
Glu72Ala 300 235
Glu72Leu 302 278
Glu72Asp 310 102
Gly34Qln - -
Thr98Ala 310 135
a. En base a estos datos, explique detalladamente el rol de cada uno de los
aminocidos mutados en la cintica y funcin de la enzima.
b. Que posicin mutara y que aminocido elegira para aumentar significativamente la
Km de la enzima.
Justifique adecuadamente todas sus respuestas.
Ejercicios Adicionales
1 Para una reaccin catalizada por una enzima micaeliana:
a. Dibujen cmo vara la velocidad de la reaccin en funcin del tiempo (que datos
necesitara saber para contestar esta pregunta?)
b. Hagan lo mismo para la velocidad inicial en funcin de la concentracin de sustrato.
Ahora, grafiquen velocidad inicial versus concentracin de enzima.
2 Se estudi el efecto de la concentracin de sustrato sobre la velocidad de una reaccin
enzimtica. Se midieron las velocidades iniciales a distintas concentraciones de sustrato y
concentracin constante de enzima, en un volumen total de reaccin de 10 ml. Se obtuvieron
los siguientes resultados:
Sustrato (M) v0 (mol/min)
5.0x10-2 0.25
5.0x10-3 0.25
5.0x10-4 0.25
5.0x10-5 0.20
5.0x10-6 0.071
5.0x10-7 0.0096
Utilizando clculos numricos (NO GRFICOS), digan:
a. Cules son los valores de vmx y kM?
b. Cules son las velocidades iniciales para [S]=1.0x10 -6 M y 1.0x10 -1 M?
c. Calculen la cantidad total de producto formado durante los primeros 5 minutos para
[S]=2.0x10 -3 M. Pueden hacer el mismo clculo para [S]=2.0x10 -6 M? Porqu?
c. Supongan que la concentracin de enzima en cada mezcla de reaccin se incrementa 4
veces. Cul ser el nuevo valor de kM? y el de vmx? Cul ser ahora el valor de v0 para
[S]=5.0x10 -6 M?
3 El kM de cierta enzima por su sustrato es 1.0x10 -5 M. La reaccin sigue la cintica de
Michaelis-Menten. Para una determinada concentracin de enzima la velocidad inicial de
reaccin fue 37 moles/min, para una concentracin de sustrato de 0.1 M. Sin embargo, a
una concentracin de sustrato 0.01 M la velocidad inicial de reaccin es tambin 37
moles/min. Usando clculos numricos, demuestren porqu esta reduccin de 10 veces en
la concentracin de sutrato no tiene efecto sobre la velocidad inicial de reaccin.
4 Se quiere poner a punto un protocolo para estudiar la cintica de la enzima lactato
deshidrogenasa. Esta enzima cataliza la reaccin
Lactato + NAD Piruvato + NADH
A 340nm la nica especie qumica capaz de absorber luz es el NADH, de ah que su
incremento en el tiempo pueda ser tomado como proporcional a la disminucin de Lactato. El
coeficiente de absortividad molar para el NADH es 6220 M-1 cm-1. Para este estudio se utiliza
una solucin comercial de enzima que contiene 3 UI/ml de enzima. La mezcla de reaccin
contiene:
1ml de solucin de enzima:
5 ml de solucin de sustrato
4 ml de buffer
A distintos tiempos de reaccin se toman distintas alcuotas de la mezcla de reaccin. Sobre
estas se mide su absorbancia a 340nm.
a. Si se utiliza una solucin 1/100 de la enzima, prediga entre que tiempos, mnimo y
mximo, podra medir la absorbancia de la solucin (tenga en cuenta que las
mediciones optimas de absorbancia se toman entre 0.2-0.8)
b. Que concentracin de sustrato sera necesaria para que la velocidad estimada en el
punto anterior sea una velocidad inicial? Cul es la concentracin en la solucin stock
de sustrato empleada para hacer la mezcla de reaccin?
c. Calcule la velocidad mxima de dicha enzima en la mezcla de reaccin.
5
La cintica de la enzima carboxipeptidasa se estudi usando como sustrato un pptido del
cual, por accin de la enzima, se libera el aminocido triptofano. La cintica de la enzima se
estudio para distintas concentraciones de pptido a 25 C y ph = 7.5. Los datos de tal estudio
se representaron en un grafico como se muestra a continuacin:
45
40
35
1/v0 (mM s)
30
-1
25 datos
y=b0+b1x
20 All curves:
a. Coefficients: Calcule
b[0]11.8062776299 Vmax y Km
15 b[1]0.0755095039
r0.9976517593
para la
enzima
b. 10 Calcule las
0 100 200 300 400 500
-1
1/[s] M
concentraciones de sustrato para las cuales se obtiene una velocidad igual a 0.90,
0.50 y 0.20 de Vmax
c. Calcule 2 relaciones de concentraciones para la cual la velocidad inicial se duplica
You might also like
- Seminario 5Document4 pagesSeminario 5Mar ValenciaNo ratings yet
- Taller Parcial 1Document5 pagesTaller Parcial 1William Camilo Díaz GonzálezNo ratings yet
- Ejercicios de Cinetica EnzimaticaDocument28 pagesEjercicios de Cinetica EnzimaticaJose Orbegoso LopezNo ratings yet
- Ejercicios Cinética EnzimáticaDocument6 pagesEjercicios Cinética EnzimáticaSambita MaryNo ratings yet
- Practica Nº2Document5 pagesPractica Nº2xchinodanyNo ratings yet
- Problemas Introduccion 2010Document4 pagesProblemas Introduccion 2010Marcela V. Pellegrini0% (1)
- Coloquio 5Document13 pagesColoquio 5Alex AlustizaNo ratings yet
- Práctica 2Document7 pagesPráctica 2ppchuy344No ratings yet
- Problemas Introduccion 2010Document4 pagesProblemas Introduccion 2010weikeNo ratings yet
- Práctica #4 Determinación Del Efecto (S) Sobre La FA - Cálculo de KM y VmaxDocument3 pagesPráctica #4 Determinación Del Efecto (S) Sobre La FA - Cálculo de KM y VmaxDayanna MendozaNo ratings yet
- Practico 4 ImprimirDocument8 pagesPractico 4 ImprimirDa GeißerNo ratings yet
- Guia 2017 Enzimologia Quimica Biologica 24 de AbrilDocument19 pagesGuia 2017 Enzimologia Quimica Biologica 24 de AbrilGuapomonNo ratings yet
- TPDocument4 pagesTPAlfonso PepeNo ratings yet
- Enzimas Bio ListoDocument17 pagesEnzimas Bio ListoIgnacio ArFuNo ratings yet
- Taller 2 Problemas de Enzimologia - Curso 22-23Document19 pagesTaller 2 Problemas de Enzimologia - Curso 22-23AprenediendoaConLaMata. comNo ratings yet
- Tp04 Bq1 Unaj 2022Document4 pagesTp04 Bq1 Unaj 2022René PonceNo ratings yet
- Actividad de Clase Inmovilización de EnzimasDocument11 pagesActividad de Clase Inmovilización de EnzimasEdwin TulcánNo ratings yet
- Guia de Problemas de Enzimologia y Cinetica EnzimaticaDocument27 pagesGuia de Problemas de Enzimologia y Cinetica EnzimaticabbvgftrNo ratings yet
- Cinética Enzimática Jesaya Rios.mDocument12 pagesCinética Enzimática Jesaya Rios.mJesaya RiosNo ratings yet
- Prob. Catalisis EnzimáticaDocument1 pageProb. Catalisis EnzimáticaJeffry Daza CorzoNo ratings yet
- Practico 4Document5 pagesPractico 4Grisel RodriguezNo ratings yet
- Informe Final Tirosinasa - Fosfatasa PDFDocument21 pagesInforme Final Tirosinasa - Fosfatasa PDFcamilo432100% (1)
- Taller 2. Catálisis EnzimáticaDocument2 pagesTaller 2. Catálisis EnzimáticaANA MARIA ARANGO SEPULVEDANo ratings yet
- Taller de EnzimasDocument5 pagesTaller de EnzimasKevin ParraNo ratings yet
- Rxns EnzDocument7 pagesRxns EnzLuis Gustavo Nolasco LeónNo ratings yet
- Enzimas e InhibiciónDocument73 pagesEnzimas e InhibiciónHéctor GalvánNo ratings yet
- Problemas Enzimas 2Document3 pagesProblemas Enzimas 2Kamila KbelloNo ratings yet
- TP N 7 Operon Lac Giudici AbrilDocument8 pagesTP N 7 Operon Lac Giudici AbrilAbril GiudiciNo ratings yet
- Práctica 11 - TransaminaciónDocument5 pagesPráctica 11 - Transaminaciónmprosario8No ratings yet
- Cinética Enzimática de La Glucosa-OxidasaDocument13 pagesCinética Enzimática de La Glucosa-OxidasaDavid HenríquezNo ratings yet
- Ejercicios Cinetica EnzimaticaDocument4 pagesEjercicios Cinetica EnzimaticaAlejandra PeñaNo ratings yet
- Relacion de Problemas EnzimologiaDocument5 pagesRelacion de Problemas EnzimologiaCarmen Rincón100% (1)
- Practica 4Document12 pagesPractica 4Lorena Herrera Tejeda0% (1)
- Clase Enzimas 2Document85 pagesClase Enzimas 2Rodrigo Amaru Bruna VásquezNo ratings yet
- Cuantificacion de La Actividad Enzimatica y Determinacion de La Actividad Especifica de La Fosfatasa Acida de Higado de PolloDocument10 pagesCuantificacion de La Actividad Enzimatica y Determinacion de La Actividad Especifica de La Fosfatasa Acida de Higado de PolloFranco Javier Huaccha CáceresNo ratings yet
- Metabolismo de CarbohidratosDocument2 pagesMetabolismo de Carbohidratosjavier san juan mercadoNo ratings yet
- Biomoléculas IDocument6 pagesBiomoléculas IJuanma AlfaroNo ratings yet
- Reporte-FOSFATASA (Deleted)Document11 pagesReporte-FOSFATASA (Deleted)Ale NoguezNo ratings yet
- Segundo Parcial 2019Document9 pagesSegundo Parcial 2019Jorge AmatoNo ratings yet
- Informe Cinetica EnzimaticaDocument10 pagesInforme Cinetica EnzimaticaMarcelo CucasNo ratings yet
- S5 - Bioq 1 UNAJ 2021Document5 pagesS5 - Bioq 1 UNAJ 2021René PonceNo ratings yet
- Informe Nº1 Lab. Enzimología - Mesa 1Document8 pagesInforme Nº1 Lab. Enzimología - Mesa 1Miguel Angel Quispe HuamanNo ratings yet
- Guía 4 EnzimasDocument2 pagesGuía 4 EnzimasAntonia Madrid100% (1)
- Actividad Enzimatica de Fosfatasa Acida en SueroDocument8 pagesActividad Enzimatica de Fosfatasa Acida en SueroMaziel Pamela Cusi CasanovaNo ratings yet
- Ejercicios para TallerDocument3 pagesEjercicios para TallerVenezuelaNo ratings yet
- Efecto de La Temperatura en La Velocidad de Reacción & Determinación de Parámetros de Cinética EnzimáticaDocument13 pagesEfecto de La Temperatura en La Velocidad de Reacción & Determinación de Parámetros de Cinética EnzimáticaLuis A. InurretaNo ratings yet
- Qb-Lab 5-Cinética Enzimática IiDocument4 pagesQb-Lab 5-Cinética Enzimática IiCañizares NestorNo ratings yet
- CatalasaDocument7 pagesCatalasaPiero Juarez100% (1)
- Giraldo Borrero MosqueraDocument7 pagesGiraldo Borrero MosqueraJUAN DANIEL GIRALDO MUÑOZNo ratings yet
- Practica FinalDocument3 pagesPractica FinalMILENKA YOMAR MONTEALEGRE SARZURINo ratings yet
- Lectura Sesion 2. EnzimasDocument8 pagesLectura Sesion 2. EnzimasCamila MoralesNo ratings yet
- Enzimas - Marco Godoy, Magdalena Ibañez, Francisca SaavedraDocument16 pagesEnzimas - Marco Godoy, Magdalena Ibañez, Francisca SaavedraValentina CastroNo ratings yet
- Cinetica Enzimatica Ejercicios ResueltosDocument26 pagesCinetica Enzimatica Ejercicios Resueltospvv1963100% (1)
- Modelamiento y casos especiales de la cinética química heterogéneaFrom EverandModelamiento y casos especiales de la cinética química heterogéneaRating: 3 out of 5 stars3/5 (1)
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadFrom EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadNo ratings yet
- Isomeros y EstereoquimicaDocument3 pagesIsomeros y EstereoquimicaManuel Alejandro PeñafielNo ratings yet
- CG MS PDFDocument8 pagesCG MS PDFManuel Alejandro PeñafielNo ratings yet
- Aceites EsencialesDocument28 pagesAceites EsencialesJulio Ge E100% (4)
- Normas APA Sexta Edición PDFDocument21 pagesNormas APA Sexta Edición PDFBuffon BravoNo ratings yet
- Ese SilencioDocument6 pagesEse SilencioVíctor JiménezNo ratings yet
- Flavonoides y Parametros de Agitacion en BiomineriaDocument3 pagesFlavonoides y Parametros de Agitacion en BiomineriaManuel Alejandro PeñafielNo ratings yet
- Foro Cambio Climatico Por La AgriculturaDocument1 pageForo Cambio Climatico Por La AgriculturaManuel Alejandro PeñafielNo ratings yet
- Fundamentosdegestionempresarialunidaduno1 100317005229 Phpapp02Document15 pagesFundamentosdegestionempresarialunidaduno1 100317005229 Phpapp02Ambroxol MetroxolNo ratings yet
- Acuerdo 061 Reforma Libro Vi Tulsma - R.o.316 04 de Mayo 2015Document80 pagesAcuerdo 061 Reforma Libro Vi Tulsma - R.o.316 04 de Mayo 2015Priss PaucarNo ratings yet
- Preguntas Entrevista TrabajoDocument1 pagePreguntas Entrevista TrabajoManuel Alejandro PeñafielNo ratings yet
- Transformada de LaplaceDocument18 pagesTransformada de Laplacefredy málagaNo ratings yet
- Código Tributario Ultima ModificacionDocument107 pagesCódigo Tributario Ultima ModificacionPatriciaPelaezNo ratings yet
- Microbiologia Industrial LibroDocument108 pagesMicrobiologia Industrial LibroAlejandro Canaza Jorges0% (1)
- MaterialDocument46 pagesMaterialManuel Alejandro PeñafielNo ratings yet
- Plan Del Buen VivirDocument399 pagesPlan Del Buen VivirManuel Alejandro PeñafielNo ratings yet
- Ejemplo EstadisticaDocument2 pagesEjemplo EstadisticaManuel Alejandro PeñafielNo ratings yet
- Manejo Del Recurso SueloDocument2 pagesManejo Del Recurso SueloManuel Alejandro PeñafielNo ratings yet
- Fmam IDocument20 pagesFmam IManuel Alejandro PeñafielNo ratings yet
- 6 Ideas para La Busqueda de TrabajoDocument1 page6 Ideas para La Busqueda de TrabajoManuel Alejandro PeñafielNo ratings yet
- Diseño de Procesos AlgoritmosDocument24 pagesDiseño de Procesos AlgoritmosManuel Alejandro PeñafielNo ratings yet
- FUNBIODocument10 pagesFUNBIOManuel Alejandro PeñafielNo ratings yet
- Balance 1Document118 pagesBalance 1Manuel Alejandro PeñafielNo ratings yet
- TejasDocument5 pagesTejasManuel Alejandro PeñafielNo ratings yet
- Tablas Mecanica de FluidosDocument4 pagesTablas Mecanica de FluidosManuel Alejandro PeñafielNo ratings yet
- Pasos para Fabricar Cerveza CaseraDocument7 pagesPasos para Fabricar Cerveza CaseraManuel Alejandro PeñafielNo ratings yet
- Apuntes Sobre Desarrollo ComunitarioDocument83 pagesApuntes Sobre Desarrollo ComunitarioChristian Francisco García CruzNo ratings yet
- Apuntes-Mecanica de Fluidos 2011Document101 pagesApuntes-Mecanica de Fluidos 2011Julio Miguel Fernández PradoNo ratings yet
- Laboratroio. Nucleoproteinas. MetodologíaDocument13 pagesLaboratroio. Nucleoproteinas. MetodologíaIrene FengNo ratings yet
- Biologia Celular Unidad 4Document29 pagesBiologia Celular Unidad 4Betty CosmeNo ratings yet
- 30-07-2021 Cofactores Enzimaticos-Ing. QuimicaDocument13 pages30-07-2021 Cofactores Enzimaticos-Ing. QuimicaLeoncio Hilario UmiyauriNo ratings yet
- Catabolismo de Lípidos 1 - LipólisisDocument3 pagesCatabolismo de Lípidos 1 - LipólisisLis ReyNo ratings yet
- Tema 1 - IntroduccionDocument4 pagesTema 1 - IntroduccionepepNo ratings yet
- Activación de Linfocitos TDocument3 pagesActivación de Linfocitos TOctavio ZmNo ratings yet
- Informe 4 - Pruebas Generales de Aminoacidos y ProteinasDocument18 pagesInforme 4 - Pruebas Generales de Aminoacidos y ProteinasLaura CaicedoNo ratings yet
- Guía de Problemas N°1 - Bioquímica IIDocument8 pagesGuía de Problemas N°1 - Bioquímica IIANA LAURANo ratings yet
- CineticaDocument26 pagesCineticaserigleromNo ratings yet
- Cromatina BacterianaDocument2 pagesCromatina Bacterianamexico_and_you4729No ratings yet
- Radicales Libres y Especies Reactivas de OxigenoDocument9 pagesRadicales Libres y Especies Reactivas de OxigenoMonica MendozaNo ratings yet
- Macronutrientes y MicronutrientesDocument8 pagesMacronutrientes y MicronutrientesFRANCISCO ANTONIO PEÃ'A EPULEO50% (2)
- Taller EnzimasDocument8 pagesTaller Enzimasjhonatan AlonsoNo ratings yet
- Taller 5Document4 pagesTaller 5DANNERI LEZAMA GALLEGOSNo ratings yet
- Ejercicios Semana 11Document6 pagesEjercicios Semana 11DAYRIN MILEYDI LINARES AGUIRRENo ratings yet
- Nucleótidos y NucleósidosDocument12 pagesNucleótidos y NucleósidosXimena AlonsoNo ratings yet
- Nutrient EsDocument7 pagesNutrient EsLuzhesita Marix Martinez RiosNo ratings yet
- 3transporte de Electrones y Fosforilacion OxidativaDocument18 pages3transporte de Electrones y Fosforilacion OxidativaSanti GarciaNo ratings yet
- TERPENOSDocument11 pagesTERPENOSMar MelgarejoNo ratings yet
- Tema 2 Aminoacidos y Proteinas PDFDocument8 pagesTema 2 Aminoacidos y Proteinas PDFKaizerNo ratings yet
- Cadena Transportadora de ElectronesDocument9 pagesCadena Transportadora de ElectronesVinicio VillafuerteNo ratings yet
- Informe de QuimicaDocument7 pagesInforme de QuimicaModesto CopiasNo ratings yet
- Trabajo de Investigacion de Microbiologia y Bioquimica Industrial - Grupo 2 - V-CDocument13 pagesTrabajo de Investigacion de Microbiologia y Bioquimica Industrial - Grupo 2 - V-CMeilin PachecoNo ratings yet
- Telomeros y TelomerasasDocument4 pagesTelomeros y TelomerasasLuz Vanessa ParejoNo ratings yet
- Resumen: Glucólisis, Ciclo Del Ácido Cítrico, Fosforilación Oxidativa y Cadena Respiratoria.Document8 pagesResumen: Glucólisis, Ciclo Del Ácido Cítrico, Fosforilación Oxidativa y Cadena Respiratoria.Axel RamírezNo ratings yet
- Control Genético de La Síntesis ProteicaDocument21 pagesControl Genético de La Síntesis ProteicaAlma MirandaNo ratings yet
- Resumen Cap 9 Bioquimica BaynesDocument7 pagesResumen Cap 9 Bioquimica BaynesBrithny Amelí Santisteban CameyNo ratings yet
- 4 Niveles de Organización y Biomoléculas 2020 - 20Document34 pages4 Niveles de Organización y Biomoléculas 2020 - 20selene lima lastraNo ratings yet
- Metabolismo de NucleótidosDocument52 pagesMetabolismo de NucleótidosNellys Suarez BanquethNo ratings yet