Professional Documents
Culture Documents
Cinética Química
Uploaded by
Michael Camacho PortugalOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Cinética Química
Uploaded by
Michael Camacho PortugalCopyright:
Available Formats
ESCUELA MILITAR DE INGENIERIA
QUIMICA
CINETICA QUIMICA
CINTICA QUMICA
COMPETECIA
Determinar la velocidad de reaccin y orden de reaccin.
FUNDAMENTO TEORICO
La cintica qumica se ocupa principalmente del estudio del efecto que tiene los
cambios de concentracin y temperatura sobre la velocidad de las reacciones qumicas.
LA VELOCIDAD DE REACCION
La cintica qumica se ocupa de la determinacin de la velocidad de las reacciones
qumicas, entonces esta corresponde a la relacin de la concentracin del reactivo que
se consume en un tiempo determinado o de la concentracin del producto que se forma
en la unidad del tiempo.
En la siguiente reaccin se tiene al reactivo (A) y producto (B): A B
Interpretacin para el producto:
B [ B2 ] [ B1 ]
=
; Entonces:
t
t 2t 1
v reaccion =v conla que aparece el producto
v=
Interpretacin para el reactivo:
[ B]
t ; porque:
Unidad:
[ ][
t 2 >t 1
v reaccion =v conla que se cosume el reactivo
[ A ]
A [ A ]2 [ A 1 ]
v=
=
;
Entonces:
; porque:
t
t
t 2t 1
mol
L
mol
mol
;
;
s
Ls Lmin
[ B 2 ]> [ B ]1
[ A 2 ] <[ A ]1
t 2 >t 1
La velocidad de las reacciones qumicas esta grandemente afectadas por los cambios
en la concentracin de los reaccionantes, por los cambios de temperatura y por la
presencia de catalizadores.
EFECTO DE CONCENTRACION SOBRE LA VELOCIDAD DE REACCION
Para entender el efecto de la concentracin sobre la velocidad de reaccin nos
basamos en la experiencia del fsico alemn LudwuingWilhelmi (1812 1864) quien
estudio la hidrolisis de la sacarosa a partir de la siguiente reaccin.
H 2 0+ C12 H 22 O11 C 6 H 12 O6 +C 6 H 12 O6
Sacarosa
glucosa
fructosa
1-1
ESCUELA MILITAR DE INGENIERIA
QUIMICA
CINETICA QUIMICA
[ S ]
Demostr que: v = t =K [ S ] , para un proceso infinitesimal:
v=
[S]
=K [ S ]
t
Donde S es la concentracin de la sacarosa.
Adems determino el valor de K (constante de velocidad): K = 0,004 min-1
LEY DE ACCION DE MASAS Y LA EXPRESION DE LA VELOCIDAD.
Para la reaccin se aplica la ley de Guldberg y Waage (1867) los cuales indican que la
velocidad de la reaccin qumica es proporcional a las concentraciones de las
sustancias reaccionantes.
Sea la ecuacin general:
a A+b B+c C+. . .. . . productos
De acuerdo a la ley de accin de masas:
[ A]
x
y
z
v1
=K [ A ] [ B ] [ C ] ..
[Reactante]
t
Donde x, y, z cada variable puede asumir el valor de cero, entero positivo negativo,
fracciones.
x+ y+ z : define el orden de reaccin
x+ y+ z=1 : Reaccin de primer orden.
x+ y+ z=2 : Reaccin de segundo orden.
x+ y+ z=0 : Reaccin de orden cero.
REACCIONES DE PRIMER ORDEN:
De la reaccin general: a A+b B+c C+. . .. . . productos
De la ley de accin de masas:
v1
[reactante]
[ A]
x
y
z
=K [ A ] [ B ] [ C ] ..
t
Para una reaccin de primer orden: x=1, y=0, z=0
[A]
1
0
0 [A]
1
=K
[
A
]
[
B
]
[
C
]
= K 1 [ A ]
1
Reemplazando:
t
t
Para un proceso infinitesimal:
d [ R]
d [R ]
=K 1 [ R]
=K 1 dt
dt
[ R]
Aplicando la integral correspondiente se tiene:
2-1
ln
[R]
[R ]0
=K 1 (t 1t 2 )
ESCUELA MILITAR DE INGENIERIA
QUIMICA
CINETICA QUIMICA
Donde R concentracin del reactivo a tiempo t.
REACCIONES DE SEGUNDO ORDEN:
De la reaccin general: a A+b B+c C+. . .. . . productos
La velocidad de desaparicin de A ser:
Como la reaccin de segundo orden:
[A]
x
y
z
=K n [ A ] [ B ] [ C ] .
t
x+ y+ z=2
[A]
[A]
2
=K 2 [ A][B]
=K 2 [ A ]
t
t
Reemplazando:
d [ A]
2
=K 2 [ A ]
dt
Para un proceso infinitesimal:
Aplicando mtodos de clculo se obtiene la frmula:
1
1
=K 2(tt 0 )
[ A ] [ A ]0
EQUIPO Y MATERIAL
5 tubos de ensayo.
1 pipeta de 10 ml.
1 pipeta de 5 ml.
1 gradilla.
1 propipeta.
REACTIVOS
Bicarbonato de sodio.
Carbonato
Acido ntrico
Acido
Actico
Fenolftaleina.
CALCULOS:
Concentraciones:
Tubo De Ensayo 1
Tubo De Ensayo 2
V 1 C 1=V 2 C2
V1
=5ml
NaH co 3 C 2=
V1
V 1C1
V2
V 1C1
V2
V2 =
C1 =0.1 NaH CO 3 C 2=0
V 2 =0
=4ml
NaH CO 3 C 2=
1 ml NaH CO3 C 2=
3-1
C1 = 0.1
4 ml 0.1
1 ml
ESCUELA MILITAR DE INGENIERIA
QUIMICA
CINETICA QUIMICA
Tubo De Ensayo 3
V1
Tubo De Ensayo 4
V 1C1
NaH
CO
C
=
3
2
=3ml
V2
V1
V 2 =2ml
NaH CO 3 C 2=
C1 =0.1
V 1C1
NaH
CO
C
=
3
2
=2ml
V2
V 2 =3ml H
3 ml 0.1
2ml
C2 =
c 3=0.15 M
2 ml 0.1
3 ml
C1 =0.1 C 4=0.07 M
Determinacin Del Orden De Reaccin
R(M)
t (s)
0,1
1,34
0,08
1,25
0,06
1.17
0,04
1,05
0,02
0,8
Calcular Las Constantes De La Rapidez A Partir
1)
K0
Tubo De Ensayo 5
(0,080,1)
(1,251,34 )
V C
V 1=1 mlNaH CO 3 C 2= 1 1
V2
=
V2 =
2ml
H 2 O C2 =
C1 =
1 ml 0.1
4 ml
0.1 4 - 1
NaH (O 4 )
t
M
-0,22 S
=-
ESCUELA MILITAR DE INGENIERIA
QUIMICA
CINETICA QUIMICA
2).
K0
=-
(NaHC O 3 )
(0,060,08)
M
==-0,25
S
(1.171,25)
t
3).
K0
=-
(0,040,06)
(NaHC O 4)
M
==-0,16
S
(1,051.17)
t
4).
K0
(NaHC O 3 )
(0,020,04)
M
==- (0,81,05) =-0,08 S
t
Excepto
K1
K2
K3
K4
Por lo que corresponde a una reaccin de orden cero.
Si no verifica con orden cero hacer los clculos para:
Primer Orden;
K1
ln
Segundo Orden;
=-
K2
(NaHC O 3) F
(NaHC O 3 )o
=0,43
t F t o
1
1
(NaHC O 3) F ( NaHC O3) o
=
=0,534
t F t o
GRAFICA:
grafica
1.5
1
0.8
REACCIONES
0.5
0
0.5 1 1.5 2 2.5 3 3.5 4 4.5 5 5.5
numero de tubos
CUESTIONARIO
5-1
ESCUELA MILITAR DE INGENIERIA
QUIMICA
CINETICA QUIMICA
1. De que factores depende la velocidad de reaccin?
La velocidad de las reacciones qumicas depende de cuatro factores: el estado de
divisin de los reactivos, la concentracin de los reactivos, la temperatura y la adicin
de catalizadores.
2. Cmo influye la concentracin en la velocidad de reaccin qumica?
La velocidad de reaccin no es constante. Al principio, cuando la concentracin de
reactivos es mayor, tambin es mayor la probabilidad de que se den choques entre las
molculas de reactivo, y la velocidad es mayor. a medida que la reaccin avanza, al ir
disminuyendo la concentracin de los reactivos, disminuye la probabilidad de choques y
con ella la velocidad de la reaccin. La medida de la velocidad de reaccin implica la
medida de la concentracin de uno de los reactivos o productos a lo largo del tiempo,
esto es, para medir la velocidad de una reaccin necesitamos medir, bien la cantidad de
reactivo que desaparece por unidad de tiempo, bien la cantidad de producto que
aparece por unidad de tiempo. La velocidad de reaccin se mide en unidades de
concentracin/tiempo, esto es, en moles/s.
3. En el ensayo al combinar bicarbonato de sodio con cido actico porque la
fenolftalena cambia de color?
Por el principio de Lechatelier de que debe mantener el equilibrio qumico en la reaccin
4. En el ensayo al combinar bicarbonato de sodio por que se form burbujas de gas?
El acero tiene un volumen constante y el casco de un barco tiene un volumen
vaco.
5. Cierta reaccin A y B es de primer orden y la constante de velocidad es 3.30x10 s. Si
la concentracin de A es 0.030 mol/L y la de B es cero Determine las concentraciones
al cabo de 200 min?
La concentracin de es 0.202 M, y la de B es de 0.098 M
6. Un 35.5 % de cierta reaccin de primer orden se lleva a cabo en 4,90 min. A 25C
Cul es la constante de velocidad en min??
La constante de velocidad expresada en minutos es de K= 0,0896 min-1
7. Para cierta reaccin de primer orden, el tiempo de vida media es de 100s. Calcular el
tiempo min necesario para que se consuman 87,5% de la sustancia.
El tiempo para que se consuma la sustancia es de 5 min.
Datos:
1
1 0,693
=100 [ s ] t =
t 2
2
K1
87,5 100 [ s ] =
0,693
0,693
K 1=
K 1=6,93 103 [ s1 ]
K1
100 [ s ]
log ( 0.125 )=log ( 1 )
K 1t
2.303log ( 1 )log ( 0.125 )
t=
2,303
6,93 103 [ s1 ]
6-1
ESCUELA MILITAR DE INGENIERIA
t=130,31
QUIMICA
CINETICA QUIMICA
[ s ]1 [ min ]
60 [ s ]
t=2 ,17 [ min ]
8.- La constante de rapidez para la reaccin de segundo orden :
N O 2( g ) N O( g) +O2 ( g)
Es de 0,54 /M.sa 300C Cunto tiempo es segundos tomara para que la concentracin
N O2
de
disminuya desde 0,62 M hasta 0,28 M?
Datos:
K 2=0,54 / MsN O 2
T =300 0,62 M 0,28 M
1
1
= + K 2t
[ ]f [ ]0
Despejando el tiempo..
1
1
1
t=
0,54 [ 0,28 ] f [ 0,62 ] 0
t =3 , 6 [ s ]
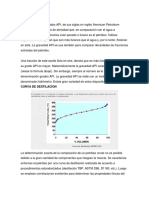
9.- Determinar con ayuda de los datos que aparecen en la tabla si la reaccin es de
orden cero o de primer orden .Calcular la constante de velocidad
PARA: n=O
REACCION A
B
Tiempo (min)
(B)
0,00
0,0000
5,00
0,0160
7,00
0,0224
11,00
0,0352
7-1
ESCUELA MILITAR DE INGENIERIA
QUIMICA
CINETICA QUIMICA
150
f(x) = 0.41x + 99.8
R = 1
100
n=0
50
0
10
20
30
40
50
60
70
TIEMPO (s)
[ B ] f =[ B ] 0+ K 2t
Y= A+ BX
r=1 ;
A=0 ; B= 0,0032
PARA : n=1
REACCION A
Tiempo (min)
ln(B)
0,00
00
5,00
-4,135
7,00
-3,799
11,00
-3,347
150
f(x) = 0.41x + 99.8
R = 1
100
n=1
50
0
10
20
30
40
TIEMPO (s)
8-1
50
60
70
ESCUELA MILITAR DE INGENIERIA
QUIMICA
CINETICA QUIMICA
ln [ B ] f =ln [ B ] 0 + K 1t
Y= A+ BX
r=0,994 ;
A=- 4,74 ; B= 0,129
LA REACCIN ES DE ORDEN O YA QUE SU GRAFICA ES UNA RECTA Y AL
MISMO TIEMPO SU CORRELACIN ES DE 1 DE ESTE MODO LA CONSTANTE DE
VELOCIDAD ES DE K=0 ,0032
10.-Determinar con ayuda de los datos de la tabla si la reaccin es de orden cero o
primer orden Calcular la constante de velocidad.
PARA : n=0
REACCION
Tiempo (min)
(A)
(B)
0,00
0,01000
0,00000
9,82
0,00965
0,00035
59,60
0,00803
0,00197
REACCION A
Tiempo (min)
(A)
0,00
0,01000
9,82
0,00965
59,60
0,00803
9-1
ESCUELA MILITAR DE INGENIERIA
QUIMICA
CINETICA QUIMICA
150
f(x) = 0.41x + 99.8
R = 1
100
n=1
50
0
10
20
30
40
50
60
70
TIEMPO (s)
[ A ] f =[ A ]0 K 2t
Y= A+ BX
r= 0 ,999831
3
A= 9 , 987 x 10
; B=
PARA : n=1
REACCION A
Tiempo (min)
ln(A)
0,00
-4,605
9,82
-4,641
59,60
-4,825
ln [ B ] f =ln [ B ] 0 + K 1t
Y= A+ BX
r=1 ;
A=- 4,605 ; B= 0,0037
PARA : n=2
REACCION A
Tiempo (min)
1/(A)
0,00
100
9,82
10 -103,63
1
59,60
124,53
3 , 289 x 105
ESCUELA MILITAR DE INGENIERIA
QUIMICA
CINETICA QUIMICA
140
120
f(x) = 0.41x + 99.8
R = 1
100
80
n=2
60
40
20
0
10
20
30
40
50
60
70
TIEMPO (s)
1
1
=
+ K t
[ A ] f [ A ]0 2
Y= A+ BX
r= 0,9997 ;
A= 99,801 ; B= 0,414
LA REACCIN ES DE ORDEN 1 YA QUE SU GRAFICA ES UNA RECTA Y AL MISMO
TIEMPO SU CORRELACIN ES DE 1 DE ESTE MODO LA CONSTANTE DE
VELOCIDAD ES DE 0,0037
K=0 ,0037
CONCLUSIONES
La velocidad de reaccin depende de la concentracin de los reactivos y de la
temperatura ya que a medida que estos aumentan, se incrementa el nmero de
colisiones, ya que las partculas se movern ms rpido y por ello ser mayor la
velocidad de reaccin.
BIBLIOGRAFA
[1] Tema 3: Cintica qumica.pdf
http://centros4.pntic.mec.es/~sierra8/aquimica/cinetica.pdf - Consultado el 23 de mayo
[2] Conceptos bsicos de cintica qumica, Juan J. Baeza.
http://www.uv.es/~baeza/cqtema3.html - Consultado el 22 de Mayo de 2012
[3] WHITTEN, K.W, Qumica General, Tercera Edicin, Mc Graw-Hill. Pg. 492.
11 - 1
ESCUELA MILITAR DE INGENIERIA
QUIMICA
CINETICA QUIMICA
12 - 1
You might also like
- Mecánica Celeste Clásica: ApuntesDocument295 pagesMecánica Celeste Clásica: ApuntesJames Duarte� GalvisNo ratings yet
- Introducción A La SoldaduraDocument43 pagesIntroducción A La SoldaduraRene Caldera50% (2)
- INFORME Corrosion MetalicaDocument16 pagesINFORME Corrosion MetalicaMarco IanNo ratings yet
- 4 EjercicioDocument3 pages4 EjercicioDayana VillarroelNo ratings yet
- 1 Procesamiento Minerales AuriferosDocument22 pages1 Procesamiento Minerales AuriferoseduardoNo ratings yet
- Neo 25 - 2005Document42 pagesNeo 25 - 2005Raúl RangelNo ratings yet
- Refineria Onsan CoreaDocument17 pagesRefineria Onsan CoreaLizeth Tania Huayllani MamaniNo ratings yet
- 02 Apuntes Prospeccion Geofisica Prof T Teixido PDFDocument59 pages02 Apuntes Prospeccion Geofisica Prof T Teixido PDFcris cruz75% (4)
- Cinética de Las ReaccionesDocument4 pagesCinética de Las ReaccionesMichael Camacho PortugalNo ratings yet
- Campo Patujusal - Pjo 1hDocument15 pagesCampo Patujusal - Pjo 1hMichael Camacho PortugalNo ratings yet
- Tipos de CombustiblesDocument7 pagesTipos de CombustiblesMichael Camacho PortugalNo ratings yet
- PlataDocument4 pagesPlataMichael Camacho PortugalNo ratings yet
- PetroleraDocument4 pagesPetroleraMichael Camacho PortugalNo ratings yet
- PetroleraDocument4 pagesPetroleraMichael Camacho PortugalNo ratings yet
- Mecanismo de ProduccionDocument3 pagesMecanismo de ProduccionMichael Camacho PortugalNo ratings yet
- Balance de MateriaDocument9 pagesBalance de MateriaMichael Camacho PortugalNo ratings yet
- Algunos ColgadoresDocument2 pagesAlgunos ColgadoresMichael Camacho PortugalNo ratings yet
- REFINACIONDocument4 pagesREFINACIONMichael Camacho PortugalNo ratings yet
- Codigo de Procedimiento Penal MilitarDocument41 pagesCodigo de Procedimiento Penal MilitarDaniel Severiche MurilloNo ratings yet
- Campo Patujusal - Pjo 1hDocument15 pagesCampo Patujusal - Pjo 1hMichael Camacho PortugalNo ratings yet
- Flotabilidad y Estabilidad 2Document2 pagesFlotabilidad y Estabilidad 2Michael Camacho PortugalNo ratings yet
- Laboratorio de ResistenciaDocument4 pagesLaboratorio de ResistenciaMichael Camacho PortugalNo ratings yet
- Laboratorio de ResistenciaDocument22 pagesLaboratorio de ResistenciaMichael Camacho PortugalNo ratings yet
- PETRÓLEODocument5 pagesPETRÓLEOMichael Camacho PortugalNo ratings yet
- Gravedad Ap1Document4 pagesGravedad Ap1Michael Camacho PortugalNo ratings yet
- Tipos de Percepcion RemotaDocument4 pagesTipos de Percepcion RemotaMichael Camacho PortugalNo ratings yet
- Tipos de Percepcion RemotaDocument4 pagesTipos de Percepcion RemotaMichael Camacho PortugalNo ratings yet
- TriásicoDocument3 pagesTriásicoMichael Camacho PortugalNo ratings yet
- Practica 1Document6 pagesPractica 1Keily BastardoNo ratings yet
- Espo Frakincg EspañolDocument2 pagesEspo Frakincg EspañolMichael Camacho PortugalNo ratings yet
- Tipos de Percepcion RemotaDocument4 pagesTipos de Percepcion RemotaMichael Camacho PortugalNo ratings yet
- Propiedades de Aldehídos y CetonasDocument6 pagesPropiedades de Aldehídos y CetonasMichael Camacho PortugalNo ratings yet
- Taladro de PerforaciónDocument5 pagesTaladro de PerforaciónMichael Camacho PortugalNo ratings yet
- Propiedades de Aldehídos y CetonasDocument6 pagesPropiedades de Aldehídos y CetonasMichael Camacho PortugalNo ratings yet
- Tipos de CombustiblesDocument7 pagesTipos de CombustiblesMichael Camacho PortugalNo ratings yet
- Gravedad Ap1Document4 pagesGravedad Ap1Michael Camacho PortugalNo ratings yet
- NARANJADocument4 pagesNARANJAMichael Camacho PortugalNo ratings yet
- Práctica Calificada - T1: Química OrgánicaDocument5 pagesPráctica Calificada - T1: Química OrgánicaMANUEL SALAZARNo ratings yet
- BraquistócronaDocument9 pagesBraquistócronaMaya Belen BalderasNo ratings yet
- Bombas CentrífugasDocument3 pagesBombas CentrífugasMELANY TATIANA APONTE SANDOVALNo ratings yet
- 114934tema6 CMN Marzo 2021 (16343)Document23 pages114934tema6 CMN Marzo 2021 (16343)Laura Salvatierra MonfortNo ratings yet
- Practica #03 04 05 - Factores Que Afectan La Actividad EnzimaticaDocument10 pagesPractica #03 04 05 - Factores Que Afectan La Actividad EnzimaticaVerónica SuárezNo ratings yet
- Principio de ArquímedesDocument14 pagesPrincipio de ArquímedesfelliolNo ratings yet
- Clase3. Estabilización y Compactacion de SuelosDocument23 pagesClase3. Estabilización y Compactacion de Suelosgabriel eduardo carmona joly estudianteNo ratings yet
- MINERALES Y GASES ESSENCIALES PARA EL CUERPO HUMANODocument2 pagesMINERALES Y GASES ESSENCIALES PARA EL CUERPO HUMANOAngel sosaNo ratings yet
- Segundo Listado de Actividades Altamente RiesgosasDocument8 pagesSegundo Listado de Actividades Altamente RiesgosasPako HidalgoNo ratings yet
- Calculo Equilibrio Flash y Vaporizaicion DiferencialDocument49 pagesCalculo Equilibrio Flash y Vaporizaicion DiferencialRicardo Gomez GalindoNo ratings yet
- Formula EmpíricaDocument10 pagesFormula EmpíricakeylaNo ratings yet
- HS - Hipoclorito de CalcioDocument10 pagesHS - Hipoclorito de Calcioalfonso jaramilloNo ratings yet
- Hoja Trabajo - Compuestos OrgánicosDocument4 pagesHoja Trabajo - Compuestos OrgánicospatriciaNo ratings yet
- Articulo Científico SOFIA MEDALLADocument16 pagesArticulo Científico SOFIA MEDALLASofia Medalla GutierrezNo ratings yet
- UntitledDocument7 pagesUntitledAndrea GalindoNo ratings yet
- Características de TetrazolesDocument3 pagesCaracterísticas de TetrazolesAly CruzNo ratings yet
- Problemas Mov. OscilatorioDocument2 pagesProblemas Mov. OscilatorioJavier MedinaNo ratings yet
- Wuolah Test AnalíticaDocument10 pagesWuolah Test AnalíticaFatimaNo ratings yet
- Triptico NanotecnologiaDocument2 pagesTriptico NanotecnologiaBrianna JulcaNo ratings yet
- Programa Mecanica de FluidosDocument2 pagesPrograma Mecanica de FluidosKeven Andres OspinaNo ratings yet
- Almacenamiento de Energía Grupo 2Document31 pagesAlmacenamiento de Energía Grupo 2LUIS RISCONo ratings yet
- Propiedades y métodos de medición de nanopartículasDocument9 pagesPropiedades y métodos de medición de nanopartículasJhon SaavedraNo ratings yet