Professional Documents
Culture Documents
0607DM2 PDF
Uploaded by
Foudil LaouiciOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
0607DM2 PDF
Uploaded by
Foudil LaouiciCopyright:
Available Formats
TS1
DM n2
Exercice n1 Suivi temporel dune transformation chimique par manomtrie.
Le monoxyde de carbone CO forme avec le fer un compos de formule Fe(CO)5 appel
pentacarbonylfer. 200 C, dans l'obscurit, le pentacarbonylfer gazeux se dcompose lentement en fer
solide et monoxyde de carbone gazeux.
Donne : Les gaz sont assimils des gaz parfaits avec R = 8,314 J.K-1.mol-1
1. Ecrire lquation de la raction de dcomposition.
2. On enferme une quantit n0 = 2,0 mmol de pentacarbonylfer dans un volume V = 250 mL,
pralablement vid, puis on chauffe = 200 C. On enregistre la pression totale P(t) dans
l'enceinte en fonction du temps.
a) Etablir le tableau davancement du systme.
b) Grce lquation du gaz parfait, exprimer la quantit totale de matire gazeuse ngaz en
fonction de la pression totale P dans l'enceinte.
c) Relier lavancement x(t) la pression totale P(t).
3. L'on note que pour t = 20 min, P = 105,0 kPa. Dterminer la composition du mlange ractionnel
cet instant.
Exercice n2 Cintique de la synthse de l'iodure dhydrogne.
On se propose d'tudier la cintique de la raction suivante :
H2(g) + I2(g) = 2 HI(g)
Dans ce but, on porte la temprature = 350 C quatre ballons de 1,00 L : A, B, C, D renfermant chacun
n0(I2) = 0,50 mmol de diiode et n0(H2) = 5,0 mmol de dihydrogne. Les ballons sont maintenus cette
temprature durant des dures t diffrentes, puis ils sont brutalement refroidis. Le diiode restant dans
chaque ballon est d'abord dissous dans une solution d'iodure de potassium (qui prend une couleur jaune),
puis il est dos par une solution de thiosulfate de sodium, 2 Na+(aq) + S2032-(aq), de concentration
C2 = 0,050 mol.L-'
La fin du titrage est indique par la dcoloration de la solution de diiode. Soit VE le volume de la solution
de thiosulfate ncessaire pour obtenir la dcoloration. On obtient les rsultats suivants :
Ballon
t (min)
50
100
150
200
VE (mL)
16,6
13,7
11,4
9,4
nI2(t) (mmol)
On donne les couples rdox suivants : I2 (aq) / I- (aq) ; S4O6 2-(aq) / S2O3 2-(aq)
1. Justifier le protocole exprimental utilis pour tudier le droulement temporel de la synthse de
l'iodure d'hydrogne HI.
2. Ecrire l'quation de la raction support du titrage.
3. Dfinir lquivalence et complter la troisime ligne du tableau prcdent.
4.
a) tablir le tableau d'avancement de la synthse de l'iodure d'hydrogne HI.
b) Exprimer l'avancement x(t) en fonction de nI2(t).
DM2
Page 1 sur 3
TS1
DM n2
c) Tracer la courbe x = f(t) En dduire la composition du mlange ractionnel pour t = 75 min.
Exercice n3. Cintique de la saponification du formiate dthyle.
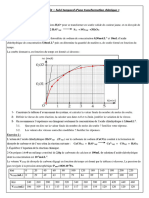
On tudie la cintique de lhydrolyse basique dun ester, le mthanoate dthyle, par la mesure de la
conductance du mlange de mthanoate dthyle et dhydroxyde de sodium en fonction du temps.
Protocole exprimental.
On verse dans un bcher une solution dhydroxyde de sodium de concentration C0 = 10,0 mmol.L-1.
On plonge la cellule conductimtrique dans la solution et on met en marche l'agitation.
On mesure la conductance initiale G(0) la date t = 0. On ajoute alors rapidement le mthanoate
d'thyle, en quantit gale celle de la soude initiale.
On mesure la conductance G(t) de la solution en fonction du temps. Les mesures sont reportes dans le
tableau (1).
0
t (min)
G (ms)
12
15
45
2,16 1,97 1,84 1,75 1,68
Avancement
x (mmol)
fin de raction
1,20
0
(tableau 1)
Donnes :
L'quation de la raction tudie est :
HCO2C2H5 + HO- = HCO2 + C2H5OH
un instant t la conductance du mlange est donne par la relation :
G (t ) = k . Na+ Na + + HO HO + HCO HCO2
2
avec k la constante de cellule, k = 0,010 m et la conductivit molaire ionique.
Les conductivits molaires ioniques de quelques ions 25 C sont donnes dans le
tableau ci-dessous :
Ion
+
Na(aq)
HO(aq)
(S.m.mol-1)
5,0.10-3
19,9.10-3
HCO(aq)
5,46.10-3
Remarques :
Le volume de mthanoate de mthyle est ngligeable devant le volume V d'hydroxyde de
sodium.
Le volume du mlange est V = 200 mL et la concentration C0 = 10,0 mmol.L-1
Soit n0 la quantit de matire initiale d'ions hydroxyde et d'ions sodium et n0 la quantit de matire
initiale de mthanoate d'thyle.
1. On considre la solution d'hydroxyde de sodium de volume V l'instant t = 0.
1.1. Donner les quantits des ions dans cette solution cet instant.
1.2. Montrer que la conductance G(0) peut s'crire :
DM2
Page 2 sur 3
TS1
DM n2
k
G (0) = n0 Na + + HO
V
1.3. En utilisant les units conventionnelles du systme international, calculer la valeur de G(0).
2. On note x(t), l'avancement de la raction un instant t. tablir un tableau d'avancement en indiquant
les quantits de matire en fonction de n0 et x(t).
3. On tudie la conductance de la solution en fonction du temps.
3.1.Montrer que la conductance du mlange un instant t en fonction des quantits de matire
initiales et de l'avancement x peut s'crire :
G (t ) =
k
. + n0 + HO ( n0 x ) + HCO x (1)
2
V Na
3.2.On veut montrer que la mesure de la conductance G(t) permet connatre l'avancement x(t) en
tablissant une relation simple entre G(t) et x(t).
3.2.1.
Simplifier l'expression (1) pour montrer qu'on peut crire x(t) sous la forme :
x(t) = a.G(t) + b , a et b tant des constantes qui contiennent les conductivits molaires
ioniques et les quantit matire initiales no.
DM2
3.2.2.
Calculer les valeurs de a et b et tableau (1) sachant que la transformation est totale.
3.2.3.
Tracer la courbe x(t). En dduire la composition du mlange la date t = 10 min.
Page 3 sur 3
You might also like
- Ob S2-Cin-ChimiqueDocument3 pagesOb S2-Cin-ChimiqueManar Bahi100% (2)
- Serie 1 E Et 2 E (Cinétique Chimique) PDFDocument9 pagesSerie 1 E Et 2 E (Cinétique Chimique) PDFbouaounNo ratings yet
- Série D'exercices N°2 - Sciences Physiques Spectre Atomique - Bac Sciences Exp (2010-2011) MR Hannachi ChokriDocument5 pagesSérie D'exercices N°2 - Sciences Physiques Spectre Atomique - Bac Sciences Exp (2010-2011) MR Hannachi ChokriTawfiq Weld EL Arbi0% (1)
- Sciences Physiques - Cinetique Chimique-Gazzah MahmoudDocument3 pagesSciences Physiques - Cinetique Chimique-Gazzah MahmoudMahmoud GazzahNo ratings yet
- TD08 Filtrage-Lineaire 2023Document8 pagesTD08 Filtrage-Lineaire 2023dawoud.kenzariNo ratings yet
- Série+d'Exercices+ +Physique+Dipole+RC+ +Bac+Mathématiques+ (2012 2013) +Mr+AfdalDocument7 pagesSérie+d'Exercices+ +Physique+Dipole+RC+ +Bac+Mathématiques+ (2012 2013) +Mr+AfdalWiem BenchahbounNo ratings yet
- 2012 2013DM5 PDFDocument25 pages2012 2013DM5 PDFbadreNo ratings yet
- TPCorrCeFe 4Document2 pagesTPCorrCeFe 4Amelie Pinchon100% (1)
- $RFCGXUMDocument2 pages$RFCGXUMChikov ÆmineNo ratings yet
- Annales Du Bac - 1995-2005Document30 pagesAnnales Du Bac - 1995-2005Japhet BAOUNDOULANo ratings yet
- Decroissance RadioactiveDocument4 pagesDecroissance RadioactiveYmelk RuthNo ratings yet
- Dipole RL Prof - Sbiro (WWW - Pc1.ma)Document5 pagesDipole RL Prof - Sbiro (WWW - Pc1.ma)lahcen essNo ratings yet
- Examen National Physique Chimie Sciences Maths 2018 Normale Sujet PDFDocument8 pagesExamen National Physique Chimie Sciences Maths 2018 Normale Sujet PDFel ghazi benrrabhiNo ratings yet
- OndesDocument5 pagesOndesMohamed HammouchNo ratings yet
- Exercice 1 (7 Points) Étude Cinétique de La Réaction de L'éthanoate D'éthyle Avec L'hydroxyde de SodiumDocument9 pagesExercice 1 (7 Points) Étude Cinétique de La Réaction de L'éthanoate D'éthyle Avec L'hydroxyde de SodiumAli A RammalNo ratings yet
- DS2 Physique Classes MPSI-PCSI-TSI My YoussefDocument5 pagesDS2 Physique Classes MPSI-PCSI-TSI My Youssefcopie masterNo ratings yet
- TP 3 Acide Base PDFDocument8 pagesTP 3 Acide Base PDFadsvgnmNo ratings yet
- 4e DS1 2010 2011Document4 pages4e DS1 2010 2011fethi10% (1)
- Redox ExoDocument10 pagesRedox ExoAbdo AiaicheNo ratings yet
- Smb-2013 Rattrapage-Sujet +corrigéDocument31 pagesSmb-2013 Rattrapage-Sujet +corrigéGuiliassNo ratings yet
- 08 Fiche Suites Series FctsDocument5 pages08 Fiche Suites Series Fctsayoub elNo ratings yet
- PH SolutionDocument5 pagesPH SolutionBelgasem AsselNo ratings yet
- Noyau, Énergie Et MasseDocument6 pagesNoyau, Énergie Et MassetarazoterachidNo ratings yet
- Corrige ENI GEIPI Physique 2009Document8 pagesCorrige ENI GEIPI Physique 2009la physique selon le programme FrançaisNo ratings yet
- Exercice (Induction - Auto Induction) PDFDocument6 pagesExercice (Induction - Auto Induction) PDFhonoka flowerNo ratings yet
- Série D'exercices N°2 - Sciences Physiques LA BOBINE ET LE DIPOLE RL - Bac Sciences Exp (2015-2016) MR Daghsni Sahbi PDFDocument5 pagesSérie D'exercices N°2 - Sciences Physiques LA BOBINE ET LE DIPOLE RL - Bac Sciences Exp (2015-2016) MR Daghsni Sahbi PDFMahmoud Essahbi Sahbi DaghsniNo ratings yet
- Tdec 2Document2 pagesTdec 2zied houaneb100% (1)
- Devoir de Contrôle N°2 Lycée Pilote - Sciences Physiques - Bac Technique (2012-2013) MR Imed RADHOUANIDocument6 pagesDevoir de Contrôle N°2 Lycée Pilote - Sciences Physiques - Bac Technique (2012-2013) MR Imed RADHOUANIKhalil Bkekri0% (1)
- Cinétique Chimique App PDFDocument6 pagesCinétique Chimique App PDFAzizElheni100% (1)
- Cours ConductimetrieDocument8 pagesCours Conductimetrienico21du13No ratings yet
- Devoir 2Document2 pagesDevoir 2HAMADA1972100% (1)
- DM16 1112 - Dosage PH Metrique Es PDFDocument6 pagesDM16 1112 - Dosage PH Metrique Es PDFEmma LovaNo ratings yet
- Exercice 4 Réactions Destérification Et Dhydrolyse LAHLALI PDFDocument5 pagesExercice 4 Réactions Destérification Et Dhydrolyse LAHLALI PDFBouba KhedherNo ratings yet
- ChimieDocument5 pagesChimieEssamiNo ratings yet
- Exmeca 0910 G M8M9Document7 pagesExmeca 0910 G M8M9Hamza NadirNo ratings yet
- DS 2001 11 13Document2 pagesDS 2001 11 13الغزيزال الحسن EL GHZIZAL Hassane0% (1)
- Sa. Dev3 TS3 13-14 PDFDocument10 pagesSa. Dev3 TS3 13-14 PDFaittaliNo ratings yet
- Serie 06Document2 pagesSerie 06Omar LANGEUR100% (1)
- Rappel - ThermoDocument18 pagesRappel - ThermoEmmanuel smith TaïgaNo ratings yet
- Corrige DM5 PDFDocument15 pagesCorrige DM5 PDFBrandy OdonnellNo ratings yet
- Mecanique Serie 3Document2 pagesMecanique Serie 3maryem sousitaNo ratings yet
- TD29 Filtrage Passe-Bas, Isolation Composante Continue-CorrigeDocument3 pagesTD29 Filtrage Passe-Bas, Isolation Composante Continue-CorrigeLahcen ElamraouiNo ratings yet
- (Simili) (Blanc Math 2022) (Boif)Document8 pages(Simili) (Blanc Math 2022) (Boif)badrelassali666No ratings yet
- Série Dexercices Sur Les Piles de Type DaniellDocument7 pagesSérie Dexercices Sur Les Piles de Type DaniellchadaNo ratings yet
- Extrait Statique CNC 2011 CorrectionDocument7 pagesExtrait Statique CNC 2011 CorrectionAdnane100% (1)
- Série D'exercices - Sciences Physiques - Equilibre Chimique - Bac Technique (2017-2018) MR Gammoudi SoufienDocument2 pagesSérie D'exercices - Sciences Physiques - Equilibre Chimique - Bac Technique (2017-2018) MR Gammoudi SoufienInass LayachNo ratings yet
- Cinétique Chimique2 PDFDocument11 pagesCinétique Chimique2 PDFmostafa90raoufNo ratings yet
- Correction TD2 - Calculs de PH (Exos 4,5,6,7,8) V2Document9 pagesCorrection TD2 - Calculs de PH (Exos 4,5,6,7,8) V2Amir NadeauNo ratings yet
- TP1 Méca2 CycloïdeDocument2 pagesTP1 Méca2 CycloïdeErwanNo ratings yet
- Théorie de Champ TD 3Document2 pagesThéorie de Champ TD 3Motive -Tech100% (1)
- Diffraction Dispersion BMDocument4 pagesDiffraction Dispersion BMAyman Benamer100% (1)
- Série D'exercices - Physique Filtre - Bac Technique (2012-2013) MR Trayia NabilDocument2 pagesSérie D'exercices - Physique Filtre - Bac Technique (2012-2013) MR Trayia NabilLam LamNo ratings yet
- Examen 2er Semestre Mai 2017version Finale Enone Et CorrigeeDocument8 pagesExamen 2er Semestre Mai 2017version Finale Enone Et CorrigeeAziz JridiNo ratings yet
- DEVOIR SURVEILLE N°3, Classe de 1°SDocument4 pagesDEVOIR SURVEILLE N°3, Classe de 1°Sالغزيزال الحسن EL GHZIZAL HassaneNo ratings yet
- Exercice Corrigée Detrmination de LDocument3 pagesExercice Corrigée Detrmination de LBoussetta ZouhaierNo ratings yet
- Série Cinétique Chimique 2bac: P T P T RDocument9 pagesSérie Cinétique Chimique 2bac: P T P T Rrkibi.khadija2006No ratings yet
- SerieDocument7 pagesSeriemehdi benmassoudNo ratings yet
- Ex-1Document2 pagesEx-1soulaimaneelaouni220No ratings yet
- Capture D'écran . 2023-11-16 À 19.24.58Document14 pagesCapture D'écran . 2023-11-16 À 19.24.58azeddineelghazoui637No ratings yet
- Série N°3 Avec Correction Chimie Série Cinétique 2007 2008 (Tlili Touhami)Document14 pagesSérie N°3 Avec Correction Chimie Série Cinétique 2007 2008 (Tlili Touhami)Ltaief Chayma100% (2)
- 2012 DS1 Acide Base PDFDocument2 pages2012 DS1 Acide Base PDFFoudil LaouiciNo ratings yet
- Acide Benzoique PDFDocument3 pagesAcide Benzoique PDFFoudil LaouiciNo ratings yet
- 2005 AmSud Correction Exo3 Cinetique Sapo 6 5ptsDocument3 pages2005 AmSud Correction Exo3 Cinetique Sapo 6 5ptsFoudil LaouiciNo ratings yet
- ElectriquesDocument4 pagesElectriquesFoudil LaouiciNo ratings yet
- Cadre - Référence PDFDocument36 pagesCadre - Référence PDFFoudil LaouiciNo ratings yet
- BC 1 Equilibre PDFDocument10 pagesBC 1 Equilibre PDFFoudil LaouiciNo ratings yet
- 2003 Pondichery Correction Exo1 Esterification 6ptsDocument2 pages2003 Pondichery Correction Exo1 Esterification 6ptsFoudil LaouiciNo ratings yet
- 2003 Pondichery Sujet Exo1 Esterification 6ptsDocument3 pages2003 Pondichery Sujet Exo1 Esterification 6ptsFoudil LaouiciNo ratings yet
- 2003 Pondichery Correction Exo1 Esterification 6ptsDocument2 pages2003 Pondichery Correction Exo1 Esterification 6ptsFoudil LaouiciNo ratings yet
- Acide Base PDFDocument26 pagesAcide Base PDFFoudil Laouici100% (1)
- Avancement 2Document2 pagesAvancement 2Foudil LaouiciNo ratings yet
- Acide Benzoique PDFDocument3 pagesAcide Benzoique PDFFoudil LaouiciNo ratings yet
- 2003 09 National Correction Exo2 Banane 6 5ptsDocument2 pages2003 09 National Correction Exo2 Banane 6 5ptsFoudil LaouiciNo ratings yet
- ph2 1RC-coursDocument9 pagesph2 1RC-coursFoudil LaouiciNo ratings yet
- 9-Quantite MatiereDocument1 page9-Quantite MatiereFoudil LaouiciNo ratings yet
- 2 PDFDocument1 page2 PDFFoudil LaouiciNo ratings yet
- 4 5 Trajectoire Satellites PDFDocument1 page4 5 Trajectoire Satellites PDFFoudil LaouiciNo ratings yet
- Acide Benzoique PDFDocument3 pagesAcide Benzoique PDFFoudil LaouiciNo ratings yet
- Acide Benzoique PDFDocument3 pagesAcide Benzoique PDFFoudil LaouiciNo ratings yet
- SM Devoir 2 P 1Document1 pageSM Devoir 2 P 1Foudil LaouiciNo ratings yet
- Acide Benzoique PDFDocument3 pagesAcide Benzoique PDFFoudil LaouiciNo ratings yet
- GEIPI Physique-Chimie 2011 PDFDocument9 pagesGEIPI Physique-Chimie 2011 PDFFoudil LaouiciNo ratings yet
- Chimie TC Cours 03 Synthese Des Especes ChimiquesDocument1 pageChimie TC Cours 03 Synthese Des Especes ChimiquesFoudil LaouiciNo ratings yet
- Chimie TC Cours 03 Synthese Des Especes ChimiquesDocument1 pageChimie TC Cours 03 Synthese Des Especes ChimiquesFoudil LaouiciNo ratings yet
- 2.réaction TotaleDocument5 pages2.réaction TotaleFoudil LaouiciNo ratings yet
- 5716 5534Document96 pages5716 5534Foudil LaouiciNo ratings yet
- Etat D'équilibre D'un Système ChimiqueDocument5 pagesEtat D'équilibre D'un Système ChimiqueFoudil LaouiciNo ratings yet
- Etat D'équilibre D'un Système ChimiqueDocument5 pagesEtat D'équilibre D'un Système ChimiqueFoudil LaouiciNo ratings yet
- Etat D'équilibre D'un Système ChimiqueDocument5 pagesEtat D'équilibre D'un Système ChimiqueFoudil LaouiciNo ratings yet
- Polissage Electrolytique de L Inox PDFDocument2 pagesPolissage Electrolytique de L Inox PDFKhouloud GharbiNo ratings yet
- Dimensionnement D'un Rechauffe - IDRISSI JANATI Zineb - 2521 PDFDocument39 pagesDimensionnement D'un Rechauffe - IDRISSI JANATI Zineb - 2521 PDFOumaima Guerouh100% (1)
- TD2 CorrectionDocument3 pagesTD2 Correctionmm72c48gbg0% (1)
- Acide PhosphoriqueDocument10 pagesAcide PhosphoriqueSimo HoussaineNo ratings yet
- GénéralitésDocument15 pagesGénéralitésJohn FistonNo ratings yet
- Industrie PétrolièreDocument14 pagesIndustrie Pétrolièrehamza.tazi.00No ratings yet
- VMZ Soudo-BrasageDocument16 pagesVMZ Soudo-BrasagebetounnNo ratings yet
- Traitement Des Eaux UseesDocument16 pagesTraitement Des Eaux UseesSOFNo ratings yet
- Devoir Surveillé 8 Durée 1 Heure - CopieDocument3 pagesDevoir Surveillé 8 Durée 1 Heure - CopieAEKO SENSEINo ratings yet
- Etude de La Métallurgie Du SoudageDocument93 pagesEtude de La Métallurgie Du SoudageOUSSAMA BEN OMARNo ratings yet
- Os Chimie Corrige ch5Document21 pagesOs Chimie Corrige ch5Amellie Gendron100% (7)
- 7 Les PilesDocument4 pages7 Les PilesDalmareen CusubNo ratings yet
- CHARRON - Web 234 2471Document12 pagesCHARRON - Web 234 2471Mohammed MAAROUFNo ratings yet
- Kemija: Izpitna Pola 1Document16 pagesKemija: Izpitna Pola 1anejNo ratings yet
- Solution-TD3 Électrochimie SMC5Document18 pagesSolution-TD3 Électrochimie SMC5mouhssine.sallamiNo ratings yet
- Extraction Poison MinérauxDocument27 pagesExtraction Poison Minérauxhanibekakra2003No ratings yet
- Activité 1 - La Configuration Électronique Des AtomesDocument2 pagesActivité 1 - La Configuration Électronique Des AtomesAndré MadeiraNo ratings yet
- Laminage À ChaudDocument24 pagesLaminage À ChaudjabraneNo ratings yet
- TP No07 Dosage Des Ions ChloruresDocument3 pagesTP No07 Dosage Des Ions Chlorureschérifa boulechfarNo ratings yet
- Chap 1 Les Nanotubes de CarboneDocument63 pagesChap 1 Les Nanotubes de CarboneNadia Ait AhmedNo ratings yet
- Ph-Solution Aqueuse-Autoprotolyse de L'eau-TsDocument2 pagesPh-Solution Aqueuse-Autoprotolyse de L'eau-TsSeydina WadeNo ratings yet
- Étamage ChimiqueDocument1 pageÉtamage ChimiqueOualidNo ratings yet
- Compte Rendu TP Electro Chimie 2Document3 pagesCompte Rendu TP Electro Chimie 2yasserNo ratings yet
- Prevention Des AccidentsmajeursliesalentreposagedengraiscontenanDocument36 pagesPrevention Des AccidentsmajeursliesalentreposagedengraiscontenanAkramKassisNo ratings yet
- 3-Classifications D'aciers:: L'acier Pour Béton Armé (Ou Béton Précontraint)Document6 pages3-Classifications D'aciers:: L'acier Pour Béton Armé (Ou Béton Précontraint)Baali LoubnaNo ratings yet
- Support de Cours Pollution&phytoremediation PDFDocument41 pagesSupport de Cours Pollution&phytoremediation PDFFrancklin TokimitondrasoaNo ratings yet
- Série C3 Liaisons Chimiques 2nde S WWW - Axloutoth.snDocument2 pagesSérie C3 Liaisons Chimiques 2nde S WWW - Axloutoth.snDaouda FallNo ratings yet
- Cahier Share 210917234607 PDFDocument81 pagesCahier Share 210917234607 PDFNSANGOUNo ratings yet
- 7 Al CR ZN 2018 2Document54 pages7 Al CR ZN 2018 2SamiNo ratings yet
- Métallurgie Des MétauxDocument11 pagesMétallurgie Des MétauxLoulou rifiaNo ratings yet