Professional Documents
Culture Documents
Informe de Electroquiimca
Uploaded by
judith churaCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Informe de Electroquiimca
Uploaded by
judith churaCopyright:
Available Formats
INDICE
1. Resumen...03
2. Introduccin..04
ELECTROQUIMICA
201
6
3. Principios tericos05
4. Detalles experimentales.....09
5. Tabulacin de datos y resultados experimentales..14
6. Ejemplos de clculos...18
7. Anlisis y discusiones de resultados.20
8. Conclusiones y recomendaciones....21
9. Bibliografa.22
10. Anexos...23
1. RESUMEN
En el siguiente informe acadmico se dar a conocer la experiencia realizada
en la cuarta prctica de laboratorio, perteneciente al tema de electroqumica,
la cual tuvo como objetivo el estudio de la ecuacin de Nernst aplicada a la
+2
celda galvnica
agua.
2+/ Cu /Cu
Zn/Zn
y la ley de Faraday para la electrolisis del
ELECTROQUIMICA
201
6
Las condiciones del laboratorio en la que se trabaj fueron presin de 756
mmhg , 23C de temperatura y a un 96% de humedad relativa.
En la ecuacin de Nernst se halla que el potencial de una celda est en
funcin de su concentracin y temperatura en base a esta teora mediante el
dispositivo de las celdas galvnicas se obtuvieron los siguientes potenciales:
+2
+2
1.67 v ( [ Zn ]=0.1 M y [ Cu ]=0.1 M ) , 1.61 v ( [ Zn+2 ]=0.1 M y [ Cu +2 ]=0.01 M )
1.55 v ( [ Zn+2 ] =0.1 M y [ Cu+2 ] =0.1 M ) ; y el error en cada caso fue de -51.81%,50.46% y -48.60% respectivamente.
Para el caso de la celda electroltica se obtuvo 10 masas experimentales de
donde se hall el porcentaje de error promedio los cual fue: 30.05% ( 6 Voltios)
y 9.06% (8 voltios).
De lo anterior se puede concluir que en una celda galvnica a menos
concentracin de una de las soluciones el potencial ser menor y en el caso de
la celda electroltica a ms amperaje la masa obtenida ser mayor. Tambin se
recomienda corroborar el buen funcionamiento de los equipos a utilizar.
Los detalles experimentales de estos resultados de manera concisa, as como
el anlisis de los resultados obtenidos, respecto al margen de error de los
experimentos, adems de las conclusiones y las recomendaciones respectivas
que permitan la obtencin de mejores resultados as como la reduccin del
porcentaje de error.
2. INTRODUCCIN
La electroqumica es el estudio de las reacciones qumicas que producen
efectos elctricos y de los fenmenos qumicos causados por la accin de las
corrientes o voltajes.
Es por ello, que el campo de la electroqumica ha sido dividido en dos grandes
secciones. La primera de ellas es la Electrlisis, la cual se refiere a las
reacciones qumicas que se producen por accin de una corriente elctrica. La
ELECTROQUIMICA
201
6
otra seccin se refiere a aquellas reacciones qumicas que generan una
corriente elctrica, ste proceso se lleva a cabo en una celda o pila galvnica.
La descomposicin electroltica es la base de un gran nmero de procesos de
extraccin y fabricacin muy importantes en la industria moderna. La sosa
custica (un producto qumico importante para la fabricacin de papel, rayn y
pelcula fotogrfica) se produce por la electrlisis de una disolucin de sal
comn en agua. La reaccin produce cloro y sodio.
El sodio reacciona a su vez con el agua de la pila electroltica produciendo sosa
custica. El cloro obtenido se utiliza en la fabricacin de pasta de madera y
papel. Una aplicacin industrial importante de la electrlisis es el horno
elctrico, que se utiliza para fabricar aluminio, magnesio y sodio. En este horno,
se calienta una carga de sales metlicas hasta que se funde y se ioniza. A
continuacin, se deposita el metal electrolticamente.
Los mtodos electrolticos se utilizan tambin para refinar el plomo, el estao,
el cobre, el oro y la plata. La ventaja de extraer o refinar metales por procesos
electrolticos es que el metal depositado es de gran pureza. La galvanotecnia,
otra aplicacin industrial electroltica, se usa para depositar pelculas de
metales preciosos en metales base.
Tambin se utiliza para depositar metales y aleaciones en piezas metlicas que
precisen un recubrimiento resistente y duradero. La electroqumica ha
avanzado recientemente desarrollando nuevas tcnicas para colocar capas de
material sobre los electrodos, aumentando as su eficacia y resistencia. Tras el
descubrimiento de ciertos polmeros que conducen la electricidad, es posible
fabricar electrodos de polmeros.
3. PRINCIPIOS TERICOS
Electroqumica:
Es la rama de la qumica que estudia la transformacin entre la energa
elctrica y la energa qumica.
El objetivo de la electroqumica es estudiar las reacciones qumicas
producidas por efecto de la corriente elctrica (electrolisis) y la produccin
4
ELECTROQUIMICA
201
6
de energa elctrica mediante trasformaciones qumicas llamadas
comnmente galvnicas o pilas.
Los procesos electroqumicos son reacciones redox (oxidacin-reduccin)
donde la energa liberada por una reaccin espontnea se convierte en
electricidad, o donde la energa elctrica se aprovecha para inducir una
reaccin qumica no espontanea.
Celdas galvnicas:
Las Celdas galvnicas, son un dispositivo en el que la transferencia de
electrones, (de la semireaccin de oxidacin a la semireaccin de
reduccin), se produce a travs de un circuito externo en vez de ocurrir
directamente entre los reactivos; de esta manera el flujo de electrones
(corriente elctrica) puede ser utilizado.
FIGURA N 01 : Estructura de las celdas galvnicas
FUENTE: http://corinto.pucp.edu.pe/quimicageneral/contenido/42celdas-galvanicas-o-celdas-voltaicas.html
En la semicelda andica ocurren las oxidaciones, mientras que en la semicelda
catdica ocurren las reducciones. El electrodo andico, conduce los electrones que
son liberados en la reaccin de oxidacin, hacia los conductores metlicos. Estos
conductores elctricos conducen los electrones y los llevan hasta el electrodo
catdico; los electrones entran as a la semicelda catdica producindose en ella la
reduccin.
ELECTROQUIMICA
201
6
FIGURA N02: Ejemplo de celdas galvnicas
FUENTE: http://corinto.pucp.edu.pe/quimicageneral/contenido/42-celdas-galvanicaso-celdas-voltaicas.html
++2 e
nodo(oxidacin)Zn(s ) Zn2 (ac)
Cu(s )
++2 e
Ctodo(reduccin)Cu 2(ac )
La pila galvnica, consta de una lmina de zinc metlico, Zn (electrodo andico),
sumergida en una disolucin de sulfato de zinc, ZnSO 4 , 1 M (solucin andica) y
una lmina de cobre metlico, Cu (electrodo catdico), sumergido en una disolucin de
sulfato de cobre, CuSO 4 , 1 M (solucin catdica).
El funcionamiento de la celda se basa en el principio de que la oxidacin de Zn a
+
Zn2 (ac) y la reduccin de
+
Cu 2(ac)
a Cu se puede llevar a cabo simultneamente,
pero en recipientes separados por un puente salino, con la transferencia de electrones,
e , a travs de un alambre conductor metlico externo.
Las lminas de zinc y cobre son electrodos.
Los electrodos son la superficie de contacto entre el conductor metlico y la solucin
de semicelda (andica o catdica). Si el electrodo no participan de la reaccin redox
(ni se oxida ni se reduce), se le llama electrodo inerte o pasivo. Cuando participa de la
reaccin redox, como es este caso, se denomina electrodo activo.
ELECTROQUIMICA
201
6
Puente salino
El puente salino es por lo general un tubo en u invertido lleno de una solucin inerte de
cloruro de sodio o de potasio.
Un puente salino se compone de un tubo en forma de "U" que contiene una solucin
muy concentrada de un electrlito.
Ejemplo:
NaN O 3 (ac ), N H 4 N O3( ac) , NaCl (ac) , KN O 3 (ac), entre otros) cuyos iones no
reaccionan con los otros iones de la celda ni con el material de los electrodos.
El electrlito se suele incorporar en un gel para que la solucin de electrlito no
escurra cuando se invierte el tubo en U.
FIGURA N 03:Ejemplo de celdas galvnicas
FUENTE:http://corinto.pucp.edu.pe/quimicageneral/contenido/42-celdas-galvanicas-o-celdasvoltaicas.html
A medida que se produce la oxidacin y la reduccin de los electrodos, los iones del
puente salino emigran para neutralizar la carga en los compartimientos de la celda.
Los aniones emigran hacia el nodo y los cationes hacia el ctodo.
De hecho, no se producir un flujo medible de electrones a travs del circuito externo,
a menos que se proporcione un medio para que los iones emigren a travs de la
solucin de un compartimiento al otro, con lo que el circuito se completa.
ELECTROQUIMICA
201
6
LEYES DE FARADAY
PRIMERA LEY
La masa depositada o liberada de una sustancia en un electroltico es directamente
proporcional a la cantidad de electricidad que pasa por la solucin.
m=
1 Eqg I t
..(1)
96500
m=masa depositada o liberada
I =Intensidad ( A)
t=tiempo(s )
Eqg=Equivalente gramo de la sustaciadepositada o liberada
Segunda ley:
Cuando una misma intensidad de corriente fluye por dos o ms celdas electrolticas,
la masa depositada o liberada es proporcional a su peso equivalente
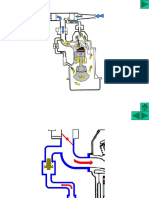
FIGURA N 04:Electrolisis
FUENTE :http://es.slideshare.net/ELIASNAVARRETE/electrlisis-13386529
ELECTROQUIMICA
201
6
Ecuacin de nernst
Nernts encontr que el potencial de una celda no solo est en funcin del electrodo y
del electroltico, sino tambin de su concentracin y temperatura para obtener el
voltaje de una celda galvnica en condiciones diferentes a las normales, se utilizara la
ecuacin de nernst.
.. (2)
E= potencial o voltaje de la celda ( f . e . m. )
E = potencial normal del par dado .
F=numero de faraday 96500.
n=numero de electrones que se gana o pierde .
ELECTROQUIMICA
4. DETALLES EXPERIMENTALES
MATERIALES
CARACTERSTICAS
IMAGEN
1.1) Fiolas
500 ml
2) Bagueta
Min 30 Max 60
vidrio
3) Tubo en U
2 Cm diametro
4) Vaso
precipitado
Dos vasos de 100ml y 500ml
3.- 4.-
5.-
5) Pipeta
Graduado 10ml
7.-
10
2.-
6.-
201
6
ELECTROQUIMICA
6) Conexiones
elecetricas
Rojo y negro ( con gancho)
7) Laminas
Cu-Zn
8) Tubo Vidrio
Salida lateral
Orificio parte inferior
8.-
9.-
9) Electrodo
metlico
Son llamados electros de
referencia
REACTIVOS
CARACTERSTICAS
1) ZnSO4
0,1 M
2) CuSo4
3) KCl
11
0,1 M
Blanco
IMAGEN
201
6
ELECTROQUIMICA
4) NaOH
4N
EQUIPOS
CARACTERISTICAS
Fuente
Corriente
Fuente de corriente continua
regulable voltaje y amperio
Multimetro
Elctrica de 1 hornilla
Variac
Transformador variable
de
201
6
IMAGEN
1.-
2.-
3.-
Fuente: http://es.slideshare.net/helenvega94/fisicoquimica-materiales-delaboratorio
Procedimiento
Experiencia 1: Capacidad calorfica del calormetro
Pasos:
a. Se arma el equipo de frasco termo
Figura N01:Armado de frasco trmico
12
Fuente: Elaboracin propia
ELECTROQUIMICA
201
6
b. Colocar 150ml de agua de cao en el termo a temperatura de 23,5c
Figura
N02:Calentamiento
del
agua
Fuente: Elaboracin propia
c. Colocar 150 ml de agua de cao a temperatura de 39,4c
Figura N03:Vaceado del agua en la pera
Fuente: Elaboracin propia
d. Dejar caer el agua de la pera a la terma , y mover constantemente hasta
que tenga una temperatura constante
Ex
periencia 2: Determinacin del calor de
neutralizacin entre soluciones
Pasos:
13
Figura N04: Titulacin
Fuente: Elaboracin propia
ELECTROQUIMICA
201
6
a. Determine las concentraciones exactas de ambas soluciones, valorando
la base de biftalato de potasio y el cido con la base. Calcule las
concentraciones corregidas.
b. Calcule los volmenes de las soluciones de hidrxido y de cido
necesarios para producir la neutralizacin, tales que sumados de 300 ml.
Figura N05:Resultado de la titulacin
Fuente: Elaboracin propia
c. Secar por completo el frasco termo y colocar en ste, el volumen de
base calculado, y en la pera el volumen de cido. Mida las temperaturas
exactas de ambas soluciones, deje caer el cido sobre la base, y mida la
temperatura
14
ELECTROQUIMICA
201
6
Figura N06: Traslado del cido sobre la base
Fuente: Elaboracin propia
5. TABULACIN DE DATOS Y RESULTADOS
EXPERIMENTALES
i.
TABLAS DE DATOS EXPERIMENTALES
TABLA N01: VALORES EXPERIMENTALES DE CELDAS GALVANICAS
CELDA GALVNICA
VOLTAJE EXPERIMENTAL (V)
[ Zn+2 ]=0.1 M . y [ Cu+2 ]=0.1 M
1.71
[ Zn+2 ]=0.1 M . y [ Cu+2 ]=0.01 M .
1.60
[ Zn+2 ]=0.1 M . y [ Cu +2 ]=0.001 M
1.55
1.69
PROMEDIO =1.67
1.62
PROMEDIO=1.61
1.54
PROMEDIO=1.54
FUENTE: ELABORACION PROPIA
TABLA N02: VALORES EXPERIMENTALES DE CELDAS ELECTROLITICA
TEMPERATURA (K)
INTENSIDAD
(A)
295
6
8
TIEMPO (s)
VOLUMEN (ml)
15
18.52
17.79
40.98
34.71
61.45
52.42
78.16
69.44
1.62
1.61
1.55
ELECTROQUIMICA
201
6
10
97.95
86.78
12
119.35
103.59
14
142.02
120.28
16
161.82
137.48
18
177.72
154.3
20
203.0
171.06
FUENTE: ELABORACION PROPIA
ii.
TABLAS DE DATOS TEORICOS
TABLA N03: VALORES TEORICOS DE CELDAS MEDIANTE LA ECUACION DE NERTS
Para
[ Zn+2 ]=0.1 M . y [ Cu+2 ]=0.1 M
molK
8.31 J /
(298 K )
molK
96500 J /
E=1.100
Para
[ Zn+2 ]=0.1 M . y [ Cu+2 ]=0.01 M .
molK
8.31 J /
(298 K )
molK
96500 J /
E=1.100
Para
16
1.100V
[ Zn+2 ]=0.1 M . y [ Cu+2 ]=0.001 M
1.070V
ELECTROQUIMICA
201
6
molK
8.31 J /
(298 K )
molK
96500 J /
E=1.10
1.045V
FUENTE: ELABORACION PROPIA
TABLA N04: VALORES EXPERIMENTALES DE CELDAS ELECTROLITICA
TEMPERATURA (K)
INTENSIDAD
VOLUMEN (ml)
295
(A)
0.6
0.9
MASA TEORICA (g)
6
MASA TEORICA (g)
6
115.194 10
165.9810
254.896 106
323.844 106
382.219106
489.074 106
486.155 106
647.875 106
10
609.249 106
809.657 106
12
742.357 10
14
966.495 10
883.364 10
1122.212 10
16
1006.520106
1282.688106
18
1105.418 106
1439.619106
20
1262.66 106
1595.989106
FUENTE: ELABORACION PROPIA
iii.
TABLAS DE CALCULOS
TABLA N05: %DE ERROR
Valores
Tericos
1.100
17
Valores
Experimental
es
1.67
Para
[ Zn+2 ]=0.1 M . y [ Cu +2 ]=0.1 M
ELECTROQUIMICA
201
6
+2
+2
1.1001.67
]=0.01818(defecto)
M.
error[ Zn
= ]=0.1 M . y[ Cu
100=51.
1.100
1.0701.61
%error=
100=50.467(defecto)
1.100
Para
1.070
1.61
Para
1.045
1.54
FUENTE: ELABORACION PROPIA
iv.
TABLAS DE RESULTADOS
18
[ Zn+2 ]=0.1 M . y [ Cu +2 ]=0.001 M
%error=
1.0451.54
100=47.368( defecto)
1.045
ELECTROQUIMICA
201
6
TABLA N07: RESULTADOS DELA LEY DE FARADAY
RESULTADOS DE CELDA GALVANICA ELECTROLTICA A 0.6 A
Valores Tericos
Valores Experimentales
% de error
6
1262.66 10
1595.98910
1647.64 10
1647.64 10
FUENTE: ELABORACION PROPIA
6. EJEMPLOS DE CLCULOS
Clculos con la ecuacin de Nernst
Sabemos que:
Ecuacin de Nernst
T = 25C=298K
19
-20.4 %(defecto)
-3.24 %(defecto)
ELECTROQUIMICA
R = 8.314 Jmol/K
n=2
F = 96500 C
Ecuacion Qumica
+ 2e
+2e
Potenciales
Para
[ Zn+2 ]=0.1 M . y [ Cu+2 ]=0.1 M
molK
8.31 J /
(298 K )
molK
96500 J /
E=1.100
Terico
=1.100v
(V)
Experimental
=1.67v
(V)
Porcentaje de error:
error =
1.1001.67
100=51. 818(defecto)
1.100
Clculos con la ley de faraday
Sea:
20
201
6
ELECTROQUIMICA
Dnde:
M = masa de sustancia
= peso equivalente de sustancia
R= amperios
t = tiempo en seg.
P=presion
R=Constantes de gases ideales
-Para nuestra experiencia:
t = 18.52seg.
T=295k
164.764 10
-Teorico:
Dnde:
21
g de Hidrogeno
201
6
ELECTROQUIMICA
201
6
M = masa de sustancia
PE. = peso equivalente de sustancia
I = amperios
t = tiempo en seg.
t = 18.52 seg.
de hidrogeno
Calculo de porcentaje de error
7. ANLISIS Y DISCUSIONES DE RESULTADOS
22
En la experiencia de la ecuacin de Nerst se obtuvo los potenciales tericos
utilizando las ecuaciones de Nerst, al compararlos con los potenciales
experimentales obtuvimos errores muy grandes, as como: -51.818 por defecto,
esto se debi travs a la falta de precisin del voltmetro, a las concentraciones
exactas de los sulfatos y tambin que elijamos bien las lminas de zinc y de
ELECTROQUIMICA
201
6
cobre; cabe recalcar que el voltmetro estaba defectuoso, no marcaba un
voltaje correcto.
En el experimento de la ley de Faraday (celda electroltica) obtuvimos un error
nfimo
por defecto, el cual nos indica que hubo precisin en la hora
del desarrollo de la experiencia.
8. CONCLUSIONES Y RECOMENDACIONES
a) CONCLUSIONES
La celda galvnica est basada en la oxidacin - reduccin donde se
produce un cambio en los nmeros de oxidacin de las sustancias. Los
electrones tienen que fluir por el circuito externo desde el electrodo
23
ELECTROQUIMICA
201
6
negativo al positivo. En el electrodo negativo tiene lugar la oxidacin y la
reduccin se verifica en el electrodo positivo. Al sumar las reacciones de
oxidacin y reduccin, resulta la celda electroqumica.
El uso del puente salino es muy importante pues concentra dos
soluciones evitando la mezcla eliminando el potencial de unin.
La diferencial de potencial varia con la concentracin , es decir mientras
ms diluida es la solucin , el potencial decrecer
b) RECOMENDACIONES
Lavar con agua desionizada los electrodos y lijar esto permite una mejor
lectura en el multmetro
En el proceso de la celda electroltica hay que tener cuidado de conectar
los cables positivo y negativo de la fuente en sus respectivos lugares ya
que de producirse este error el experimento estara completamente
errado.
9. BIBLIOGRAFA
LIBROS:
Raymond
Chang
&
Kenneth
Goldsby.,
qumica,
McGraw-
Hill/INTERAMERICANA EDITORES, S.A. DE C.V., China- 2013.
(CAPITULO 18-Pag. 815-850)
24
ELECTROQUIMICA
201
6
Wilman Benites M., Qumica-5- teora y problemas. Electroqumica,
Moshera S.R.L, Peru-2005. (Pag.01-91)
SITIOS WEB:
http://corinto.pucp.edu.pe/quimicageneral/unidades-q2/unidad-4electroquimica.html (accedida mayo 30,2016 - la teora de
electroqumica).
Wikipedia, https://es.wikipedia.org/wiki/Electroqu%C3%ADmica,
(accedida mayo 30,2016-(celda electroqumica)
OTROS:
Gua de prcticas de laboratorio de fisicoqumica, departamento
acadmico de fisicoqumica, reeditado en abril del 2016. (Frmula de la
ecuacin de nerst. Pg. 30).
10.
CUESTIONARIO
1. A qu se denomina electrolitos, mencione tres ejemplos.
Un electrlito es una sustancia que se descompone en iones (partculas
cargadas de electricidad) cuando se disuelve en los lquidos del cuerpo o el
agua, permitiendo que la energa elctrica pase a travs de ellos. Algunos de
los ejemplos de electrolitos son el sodio, el potasio, el cloruro y el calcio. La
25
ELECTROQUIMICA
201
6
responsabilidad principal de los electrolitos en los seres vivos es llevar
nutrientes hacia las clulas y sacar los desechos fuera de estas.
Los electrlitos pueden ser dbiles o fuertes, segn estn parcial o totalmente
ionizados o disociados en medio acuoso. Un electrolito fuerte es toda sustancia
que al disolverse en agua lo hace completamente y provoca exclusivamente la
formacin de iones con una reaccin de disolucin prcticamente irreversible.
Un electrolito dbil es una sustancia que al disolverse en agua lo hace
parcialmente y produce iones parcialmente, con reacciones de tipo reversible.
Los electrolitos generalmente existen como cidos, bases o sales.
Un electrlito se describe como concentrado si tiene una alta concentracin de
iones; o diluido, si tiene una baja concentracin. Si tiene una alta proporcin del
soluto disuelto se disocia en iones, la solucin es fuerte; si la mayor parte del
soluto permanece no ionizado la solucin es dbil.
Los electrlitos juegan un papel importante en los seres vivos. Ayudan a
mantener el fluido adecuado y el balance cido-base dentro del cuerpo.
Algunos de los cationes biolgicos ms importantes son Na+, K+, Ca^2+ y Mg.
Adems del Cl-, el O^2- y el S^2-, los aniones ms importantes son los aniones
poliatmicos. Un in poliatmico es un in que contiene ms de un tomo.
Ejemplos de iones poliatmicos son, el in bicarbonato (HCO3-), que es un
anin compuesto de cinco tomos, al igual que el ion sulfato (SO4^2-); el catin
amonio (NH4+) compuesto por cinco tomos, etc.
Ejemplos:
-Cloruro de sodio fundido (NaCl).
- cido ntrico.
- Cloruro mercurioso (HgCl2)
2. Qu es la FEM? Mencione algunas aplicaciones.
26
ELECTROQUIMICA
201
6
La fuerza electromotriz (FEM) es toda causa capaz de mantener una
diferencia de potencial entre dos puntos de un circuito abierto o de producir
una corriente elctrica en un circuito cerrado. Es una caracterstica de cada
generador elctrico. Con carcter general puede explicarse por la
existencia de un campo electromotor cuya circulacin, ds, define la
fuerza electromotriz del generador.
La f.e.m. se mide en voltios, al igual que el potencial elctrico.
Existen diferentes dispositivos capaces de suministrar energa elctrica,
entre los que podemos citar:
Pilas o bateras. Son las fuentes de FEM ms conocidas del gran pblico.
Generan energa elctrica por medios qumicos. Las ms comunes y
corrientes son las de carbn-zinc y las alcalinas, que cuando se agotan no
admiten recarga. Las hay tambin de nquel-cadmio (NiCd), de nquel e
hidruro metlico (Ni-MH) y de in de litio (Li-ion), recargables. En los
automviles se utilizan bateras de plomo-cido, que emplean como
electrodos placas de plomo y como electrolito cido sulfrico mezclado con
agua destilada.
Mquinas electromagnticas. Generan energa elctrica utilizando
medios magnticos y mecnicos. Es el caso de las dinamos y generadores
pequeos utilizados en vehculos automotores, plantas elctricas porttiles
y otros usos diversos, as como los de gran tamao empleado en las
centrales hidrulicas, trmicas y atmicas, que suministran energa
elctrica a industrias y ciudades.
Celdas fotovoltaicas o fotoelctricas. Llamadas tambin celdas solares,
transforman en energa elctrica la luz natural del Sol o la de una fuente de
luz artificial que incida sobre stas. Su principal componente es el silicio
(Si). Uno de los empleos ms generalizados en todo el mundo de las celdas
27
ELECTROQUIMICA
201
6
voltaicas es en el encendido automtico de las luces del alumbrado pblico
en las ciudades.
Efecto piezoelctrico. Propiedad de algunos materiales como el cristal de
cuarzo de generar una pequea diferencia de potencial cuando se ejerce
presin sobre ellos. Una de las aplicaciones prcticas de esa propiedad es
captar el sonido grabado en los antiguos discos de vinilo por medio de una
aguja de zafiro, que al deslizarse por los surcos del disco en movimiento
convierten
sus
variaciones
de
vaivn
en
corriente
elctrica
de
audiofrecuencia de muy baja tensin o voltaje, que se puede amplificar y or
a un nivel mucho ms alto.
3. Explique de que forma se pueden predecir los productos en un
proceso electroltico.
En un proceso electroltico se puede predecir los resultados mediante las
ecuaciones de reaccin. Adems que si se tienen todos los datos
necesarios (intensidad de corriente, tiempo) el clculo se hace simple.
Por ejemplo para la solucin de hidrxido de sodio se sabe que se forman
los iones H+ y O-2, una vez que empiece a pasar corriente elctrica el H +
(positivo) se dirigir al ctodo y el O-2 (negativo) ira hacia el nodo.
Originando gas hidrogeno en el ctodo y gas oxigeno en el nodo.
28
You might also like
- Fuerzas de PorteDocument1 pageFuerzas de Portejudith churaNo ratings yet
- Suavizado Mat y ObsDocument3 pagesSuavizado Mat y Obsjudith churaNo ratings yet
- La Evaluacion InternaDocument81 pagesLa Evaluacion Internajudith churaNo ratings yet
- La Cadena de SuministroDocument20 pagesLa Cadena de Suministrojudith chura100% (1)
- Sistema de LubricacionDocument10 pagesSistema de Lubricacionjudith churaNo ratings yet
- TesisDocument10 pagesTesisjudith churaNo ratings yet
- ANALIZARDocument11 pagesANALIZARjudith churaNo ratings yet
- S1.1 Metodos de UbicacionDocument51 pagesS1.1 Metodos de UbicacionJesus BartoloNo ratings yet
- CadsumDocument23 pagesCadsumHP_PaulNo ratings yet
- Aplicación Practica Del Programa de PersonalDocument10 pagesAplicación Practica Del Programa de Personaljudith churaNo ratings yet
- Lavadora TupesaDocument5 pagesLavadora Tupesajudith churaNo ratings yet
- NeumaticoDocument10 pagesNeumaticojudith churaNo ratings yet
- 6 SigmaDocument8 pages6 Sigmajudith churaNo ratings yet
- Página Tiempo Traducción OracionesDocument1 pagePágina Tiempo Traducción Oracionesjudith churaNo ratings yet
- Aplicación Practica Del Programa de PersonalDocument10 pagesAplicación Practica Del Programa de Personaljudith churaNo ratings yet
- Vapores Aceite PCVDocument7 pagesVapores Aceite PCVjudith churaNo ratings yet
- Materiales Observaciones ANTIESTATICODocument3 pagesMateriales Observaciones ANTIESTATICOjudith churaNo ratings yet
- De Que HablamosDocument21 pagesDe Que Hablamosjudith churaNo ratings yet
- F-1 Proceso de Toma de DecisionesDocument40 pagesF-1 Proceso de Toma de Decisionesjudith churaNo ratings yet
- Caja de Cambio-ChuraDocument21 pagesCaja de Cambio-Churajudith churaNo ratings yet
- Gestion de Operaciones PDFDocument205 pagesGestion de Operaciones PDFjudith churaNo ratings yet
- A2 Electricidad Basica PDFDocument123 pagesA2 Electricidad Basica PDFyersonNo ratings yet
- Labo 4Document15 pagesLabo 4judith churaNo ratings yet
- Mecanica JoseDocument9 pagesMecanica Josejudith churaNo ratings yet
- Suavizado Mat y ObsDocument3 pagesSuavizado Mat y Obsjudith churaNo ratings yet
- Emisiones ContaminantesDocument20 pagesEmisiones ContaminantesMauricio GarciaNo ratings yet
- Hilos TexturizadosDocument1 pageHilos Texturizadosjudith churaNo ratings yet
- Clúster TexmodDocument1 pageClúster Texmodjudith churaNo ratings yet
- CraftDocument2 pagesCraftjudith churaNo ratings yet
- Analisis de Propiedades en Tintoreria y AcabadosDocument9 pagesAnalisis de Propiedades en Tintoreria y Acabadosjudith churaNo ratings yet
- Entrenamiento en HHSS Con Niños y Adolescentes IDocument58 pagesEntrenamiento en HHSS Con Niños y Adolescentes IRosa María Pérez MarínNo ratings yet
- Español Semana 12Document2 pagesEspañol Semana 12Daniela TumbacoNo ratings yet
- La Enseñanza Del Ingles en La Escuela Publica Venezolana (Abril, 2015Document244 pagesLa Enseñanza Del Ingles en La Escuela Publica Venezolana (Abril, 2015José Antonio Torres100% (3)
- Caja de Cambios GRS 900 ScaniaDocument36 pagesCaja de Cambios GRS 900 ScaniaGodolfredo Beellido Turpo94% (16)
- Check list diario inspección arnes línea anclajeDocument1 pageCheck list diario inspección arnes línea anclajeAnderson Alejandro Benites ZelayaNo ratings yet
- Fase5 - Trabajo Colaborativo - Grupo - 403010 - 9Document12 pagesFase5 - Trabajo Colaborativo - Grupo - 403010 - 9Mafe LizarazoNo ratings yet
- IG Manual Velas PDFDocument9 pagesIG Manual Velas PDFAnonymous ZLUrYLS7MNo ratings yet
- Informe Creditex Io 2 1Document17 pagesInforme Creditex Io 2 1Norma ItoNo ratings yet
- Silvana RomeroDocument14 pagesSilvana RomeroMercedes Milagros Ramirez ChavezNo ratings yet
- Intervalos de Sustitución de La Correa de Distribución: Nota ImportanteDocument3 pagesIntervalos de Sustitución de La Correa de Distribución: Nota Importanteirvingalexru7664No ratings yet
- AECOC Impresión - GS1 - 128Document29 pagesAECOC Impresión - GS1 - 128Bender VigoNo ratings yet
- Impacto tecnología productividad humanaDocument7 pagesImpacto tecnología productividad humanaFLORENCIA TOSSONo ratings yet
- ENXTV-X4 Data Sheet SP110120 PDFDocument3 pagesENXTV-X4 Data Sheet SP110120 PDFcleverman1No ratings yet
- Cinetica de Monod en AlimentosDocument31 pagesCinetica de Monod en Alimentosluis100% (1)
- PoderDocument3 pagesPodersssNo ratings yet
- Material y Metodos AmbientalDocument5 pagesMaterial y Metodos AmbientalJuanPercyMonzonDavilaNo ratings yet
- PC 2 DificultadesDocument15 pagesPC 2 DificultadesGlenisiita RoqueNo ratings yet
- Ejercicios 4 - Resueltos Perdida Deposito-TanqueDocument12 pagesEjercicios 4 - Resueltos Perdida Deposito-TanqueJORGE LORENZO CHUQUIMIA CALDERONNo ratings yet
- Tipos de Suelos en El EcuadorDocument29 pagesTipos de Suelos en El EcuadorFreddy XavierNo ratings yet
- 01 Análisis de Los Principios Doctrinales de La Seguridad Social y Su Aplicación en BoliviaDocument1 page01 Análisis de Los Principios Doctrinales de La Seguridad Social y Su Aplicación en BoliviaVladimir Astete RomeroNo ratings yet
- Marketing - Di MecoDocument145 pagesMarketing - Di Mecojose roque mostacero ramosNo ratings yet
- Estructura Del Proyecto Revisión SistemáticaDocument6 pagesEstructura Del Proyecto Revisión SistemáticaElizabeth TacillaNo ratings yet
- DUSSEL E. 1492. El Encubrimiento Del Otro (Fragmento)Document15 pagesDUSSEL E. 1492. El Encubrimiento Del Otro (Fragmento)Daniela Bolaños RomeroNo ratings yet
- Planificacion Mayo y Junio Cuarto BasicoDocument4 pagesPlanificacion Mayo y Junio Cuarto BasicoMariela GarridoNo ratings yet
- Mutombo Con SuizaDocument9 pagesMutombo Con SuizaCarolina BareiroNo ratings yet
- TUTORIAL para Fabricación Casera de BRIQUETAS para La Chimenea - Fernando Pagés LledóDocument2 pagesTUTORIAL para Fabricación Casera de BRIQUETAS para La Chimenea - Fernando Pagés LledólalyrieNo ratings yet
- Diplomado en Convivencia y Mediacion EscoclarDocument4 pagesDiplomado en Convivencia y Mediacion EscoclarRicardo Araneda NuñezNo ratings yet
- Juego ficción y ToM niños dificultades socialesDocument15 pagesJuego ficción y ToM niños dificultades socialesLorena Lincopán ViverosNo ratings yet
- Evaluación Módulo 1Document3 pagesEvaluación Módulo 1serginho paulistaNo ratings yet
- Plan estratégico para microempresa THEA INDUSTRIALDocument5 pagesPlan estratégico para microempresa THEA INDUSTRIALAna MendozaNo ratings yet