Professional Documents
Culture Documents
ACT 1 Curva de Valoración Complejométrica (FORO)
Uploaded by
CR DiezOriginal Description:
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
ACT 1 Curva de Valoración Complejométrica (FORO)
Uploaded by
CR DiezCopyright:
Available Formats
Curva de valoracin complejomtrica
En las valoraciones con EDTA interesa calcular la concentracin del ion metlico en
funcin de la cantidad de valorante aadido expresado como como log (pMe) en tanto se
aaden volmenes crecientes del patrn de EDTA.Na2.
Antes del punto de equivalencia existe un exceso del catin y tras el punto de equivalencia
el exceso es de EDTA. Son dos los factores que afectan a la forma de las curvas de
valoracin con EDTA: la constante de formacin condicional del complejo formado y el pH
del medio de valoracin.
Momentos que tipifican a todas las curvas de valoracin.
1. Punto inicial: Cuando an no se ha aadido volumen alguno de solucin valorante
(EDTA.Na2).
2. Puntos intermedios: Cuando la cantidad aadida deEDTA.Na2 no es suficiente
para completar la reaccin de formacin del complejo y hay exceso del ion
metlico que se valora.
3. Punto de equivalencia: Cuando las cantidades de sustancias de ambos
reaccionantes (EDTA.Na2 e ion metlico) se igualan y se alcanza el equilibrio.
4. Puntos posteriores al punto de equivalencia: Una vez alcanzado el punto de
equivalencia
cualquier
adicin
de
solucin
patrn
del reactivo
acomplejante (EDTA.Na2) queda en exceso.
EDTA.- Es un cido Etildiaminotetraactico, que es una sustancia utilizada como agente
quelante que puede crear complejos con un metal que tenga una estructura de
coordinacin octadrica. Coordina a metales pesados de forma reversible por cuatro
posiciones acetato y dos amino, lo que lo convierte en un ligando hexadentado, y el ms
importante de los ligandos quelatos.
Traza una curva de titulacin de una solucin de 50 ml. De Ca 0.01 M con EDTA 0.01 M a
pH=10 utilizando como indicador eriocromo negro T.
Titulacion
ml
agregados
0
25
50
75
pCa
12
2
2.47
6.27
9.93
10
9.93
pCa
6.27
6
4
2
2.47
0
0
10
20
30
40
50
60
70
80
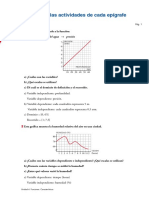
Localiza en la grfica el punto de equivalencia e indica que sucede con respecto a las
concentraciones del analito y del titulante, antes y despus del punto.
Antes del punto de equilibrio.
Se tiene un exceso de Ca en la disolucin, por lo que la concentracin del ion metlico libre
ser igual a la concentracin de Ca o que Na ha reaccionado.
Punto de equivalencia.
Nos muestra que la cantidad de valorante es la misma que la del ion metlico [Mn+] = [L].
Segn nuestros datos, tenemos que EDTA equivale a 0.01 M y Ca equivale a 0.01 M
tambin. Los cationes del EDTA reaccionan 1 a 1, suponemos que el punto de equilibrio se
encuentra en 50 ml de EDTA. Utilizamos indicador ericromo negro T y el punto de la curva
de titulacin se encuentra en 50 ml de EDTA y 6.27 de pCa.
Despus del punto de equivalencia.
Todos os iones de Ca han reaccionado y existe un exceso del valorante.
You might also like
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSFrom EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSRating: 4.5 out of 5 stars4.5/5 (7)
- Bourdieu Pensar RelacionalmenteDocument10 pagesBourdieu Pensar Relacionalmentespax379986No ratings yet
- ComplejometríaDocument7 pagesComplejometríarodrigojuliNo ratings yet
- 9788476539637Document444 pages9788476539637Wagner Mamani Molina100% (1)
- Complexometría I. Preparación y Valoración de Una Solución de EdtaDocument8 pagesComplexometría I. Preparación y Valoración de Una Solución de EdtaJenny Rodriguez AguirreNo ratings yet
- Limpieza en TBADocument50 pagesLimpieza en TBAneobem100% (1)
- Acido AceticoDocument14 pagesAcido AceticoReyes OdraNo ratings yet
- ACT 1 Curva de Valoración Complejométrica (FORO)Document4 pagesACT 1 Curva de Valoración Complejométrica (FORO)CR DiezNo ratings yet
- Volumetria de Formación de ComplejosDocument11 pagesVolumetria de Formación de ComplejosreyD1992No ratings yet
- QUIMICA ANALITICA Complejos de EDTA Con Iones Metalicos y Curvas de Titulación Con EDTADocument16 pagesQUIMICA ANALITICA Complejos de EDTA Con Iones Metalicos y Curvas de Titulación Con EDTALhyza Vm100% (1)
- Comple Jo Metric ADocument16 pagesComple Jo Metric APaola InsuastyNo ratings yet
- Tema 5 Análisis Volumétrico Esq 2016Document12 pagesTema 5 Análisis Volumétrico Esq 2016Jessica ortega VillegasNo ratings yet
- ComplejometriaDocument14 pagesComplejometriaGladys ChoqueNo ratings yet
- PrevioDocument3 pagesPrevioRobertReyes100% (1)
- Complexometria Parte I - Preparación y Valoración de Una Solución de EdtaDocument9 pagesComplexometria Parte I - Preparación y Valoración de Una Solución de EdtaJuan OyagataNo ratings yet
- 2-QUIMICA ANALITICA Complejos de EDTA Con Iones Metalicos y Curvas de Titulación Con EDTADocument12 pages2-QUIMICA ANALITICA Complejos de EDTA Con Iones Metalicos y Curvas de Titulación Con EDTALhyza Vm100% (1)
- Qa ComplejometriaDocument20 pagesQa ComplejometriaFreddy MembreñoNo ratings yet
- Volumetría Acido Base PDFDocument6 pagesVolumetría Acido Base PDFNorma NedianiNo ratings yet
- Informe Teorico de Complejos ANQ-400Document8 pagesInforme Teorico de Complejos ANQ-400Hilda MCHNo ratings yet
- Requisitos para Los Análisis VolumétricosDocument5 pagesRequisitos para Los Análisis VolumétricosRaul_negro6567% (3)
- Valoracion de Acido Devil Base FuerteDocument4 pagesValoracion de Acido Devil Base FuerteimmaninNo ratings yet
- Volumetria ComplejosDocument45 pagesVolumetria ComplejosRomina Espinoza GonzalezNo ratings yet
- Construcción y Uso Del Diagrama de McCabeDocument4 pagesConstrucción y Uso Del Diagrama de McCabeDianitaa RodriguezNo ratings yet
- PotenciometriaDocument9 pagesPotenciometriaGermán Guerra FernándezNo ratings yet
- Determinación Complejométrica de CalcioDocument2 pagesDeterminación Complejométrica de Calciolaura zabalaNo ratings yet
- Laboratorio de Acido BaseDocument9 pagesLaboratorio de Acido BaseJose Gabriel Caamaño100% (1)
- 9 InfoDocument11 pages9 InfoyumniNo ratings yet
- Laboratorio Remoto - Ácidos y BasesDocument13 pagesLaboratorio Remoto - Ácidos y BasesLeonel NoyaNo ratings yet
- Conceptos Teoricos PDFDocument69 pagesConceptos Teoricos PDFLeonardo Fabian LamasNo ratings yet
- COMPLEJOMETRÍADocument3 pagesCOMPLEJOMETRÍAAlejandra CorsiNo ratings yet
- Conferencia 2Document10 pagesConferencia 2Denis Lopez MartinezNo ratings yet
- Métodos Gráficos de Análisis de Curvas VolumétricasDocument5 pagesMétodos Gráficos de Análisis de Curvas VolumétricasAndreaFigueroaNo ratings yet
- Acido AceticoDocument10 pagesAcido Aceticopaula murciaNo ratings yet
- AnalisisDocument13 pagesAnalisisGray D L LeoNo ratings yet
- TitulaciónDocument6 pagesTitulaciónPaola LNNo ratings yet
- Fundamentos TeoricosDocument12 pagesFundamentos TeoricosFrancis MNo ratings yet
- Pract 11. - Titulación PotenciométricaDocument5 pagesPract 11. - Titulación PotenciométricaEstephany28No ratings yet
- Titulación de ComplejosDocument15 pagesTitulación de ComplejosGarissa MorenoNo ratings yet
- Lab 3 PotenciometriaDocument12 pagesLab 3 PotenciometriaLizeth PabonNo ratings yet
- Clase 4 Volumetriar QAC 1s 2020 AudioDocument42 pagesClase 4 Volumetriar QAC 1s 2020 AudioCamila BascuNo ratings yet
- Practica #12Document5 pagesPractica #12Luis Rolando Alvarez ChavezNo ratings yet
- PAUL SAAVEDRA CARRASCO - Elaborar Un Resumen de La Semana 06Document3 pagesPAUL SAAVEDRA CARRASCO - Elaborar Un Resumen de La Semana 06Paul MartinNo ratings yet
- Problemas Resueltos REDOXDocument7 pagesProblemas Resueltos REDOXRebeca Madriz MarinNo ratings yet
- Lab1 Conductimetria Valoracion Acido-BaseDocument20 pagesLab1 Conductimetria Valoracion Acido-BaseJacqueNo ratings yet
- Determinación Del Contenido de Calcio y Magnesio en Una Muestra ProblemaDocument6 pagesDeterminación Del Contenido de Calcio y Magnesio en Una Muestra ProblemaDavid Colorado Vega67% (3)
- Practica Determinación Aditivo en Refrescos de ColaDocument4 pagesPractica Determinación Aditivo en Refrescos de ColaEdwin Guerrero CRNo ratings yet
- PotenciometriaDocument10 pagesPotenciometriatroy6959No ratings yet
- Apunte Potenciometría y Método GranDocument4 pagesApunte Potenciometría y Método GranJulio Rodríguez CancinoNo ratings yet
- Pérez Cruz David Emmanuel - Cuestionario Previo - ComplejosDocument5 pagesPérez Cruz David Emmanuel - Cuestionario Previo - ComplejosDAVID EMMANUEL PEREZ CRUZNo ratings yet
- Informe Número 5 (Aplicación Del Método Volumétrico para Determinar La Composición de Soluciones Acuosas Con Mezclas de Carbonatos)Document7 pagesInforme Número 5 (Aplicación Del Método Volumétrico para Determinar La Composición de Soluciones Acuosas Con Mezclas de Carbonatos)Yefrei SierraNo ratings yet
- Volumetría de Formación de ComplejosDocument8 pagesVolumetría de Formación de ComplejosEduardo VelasquezNo ratings yet
- Lab 8Document9 pagesLab 8Kevin FloresNo ratings yet
- Acidez TesDocument11 pagesAcidez TesCarlos CajaleonNo ratings yet
- Introducción Titulacion Acidos BasesDocument5 pagesIntroducción Titulacion Acidos BasesBetty SantiagoNo ratings yet
- 10 Curvasdevaloracionacido-Base 14305Document8 pages10 Curvasdevaloracionacido-Base 14305LiZz Lara0% (1)
- Analisis Quimico - Treceava SemanaDocument23 pagesAnalisis Quimico - Treceava SemanaKeny PaezNo ratings yet
- Valoracion Poteciometrica Redox GerberDocument20 pagesValoracion Poteciometrica Redox GerberkatherinNo ratings yet
- Unidad 7 ComplejometriaDocument8 pagesUnidad 7 ComplejometriaPamela Hilari TiconaNo ratings yet
- Constante de AcidezDocument18 pagesConstante de AcidezMilagros Osorio Tábraj100% (1)
- Volumetría de Formación de ComplejosDocument8 pagesVolumetría de Formación de ComplejosKaren Ramirez QuilindoNo ratings yet
- El CuarzoDocument4 pagesEl CuarzoNILCER VIADIMER CHILON VALDEZNo ratings yet
- Capitulo 10Document10 pagesCapitulo 10Pablo ParedesNo ratings yet
- Presentación 1Document6 pagesPresentación 1guillermoNo ratings yet
- Regla de TresDocument20 pagesRegla de TresNarda Marcela Piminchumo Grau67% (3)
- Bifurcacion-Ejemplos SDII DGTDocument3 pagesBifurcacion-Ejemplos SDII DGTdavidNo ratings yet
- Seminario de Neumática IndustrialDocument74 pagesSeminario de Neumática IndustrialAdalberto LopezNo ratings yet
- CAPII EaDocument89 pagesCAPII EaLuis MendozaNo ratings yet
- Containers Kubernetes and Red Hat OpenShift Administration I DO285Document6 pagesContainers Kubernetes and Red Hat OpenShift Administration I DO285brykymaNo ratings yet
- Solucions Tema 4Document17 pagesSolucions Tema 4Pablo SánchezNo ratings yet
- 1mat07 2020 2Document5 pages1mat07 2020 2Carmen ChavezNo ratings yet
- Brochure Trilogia de Las EstructurasDocument3 pagesBrochure Trilogia de Las EstructurasjoseNo ratings yet
- Formato de Tarea - Resumen Ultrasonido Obstétrico 2o y 3er TrimestreDocument16 pagesFormato de Tarea - Resumen Ultrasonido Obstétrico 2o y 3er TrimestreAlfonso Alejandro Santiago MarcosNo ratings yet
- Teoria Word Material Teorico de WordDocument87 pagesTeoria Word Material Teorico de WordAGOSTINA BRASSEURNo ratings yet
- Actividad 2Document13 pagesActividad 2Jorge Daniel Andrade HermosilloNo ratings yet
- Informe Descomposición Del Peróxido de HidrógenoDocument4 pagesInforme Descomposición Del Peróxido de HidrógenoISABELA SOLARTE CASTILLONo ratings yet
- T2 TermoquímicaDocument19 pagesT2 Termoquímicarokan4000No ratings yet
- Libro Particulas MagnetizablesDocument129 pagesLibro Particulas MagnetizablesOperaciones RL Oilfield SolutionsNo ratings yet
- Guia de Informatica - Karen VelandiaDocument24 pagesGuia de Informatica - Karen VelandiajuliethNo ratings yet
- 02 Microscopía - Apunte 2019Document8 pages02 Microscopía - Apunte 2019gladys alvaresNo ratings yet
- Interes Simple y Descuent (Roxana)Document6 pagesInteres Simple y Descuent (Roxana)Jorge Luis Chumberiza ManzoNo ratings yet
- AFEX Certificado 280453 SCI - N - 6325 - OT 14443Document1 pageAFEX Certificado 280453 SCI - N - 6325 - OT 14443CesarRamirezCNo ratings yet
- Manejo de Nutrición.Document89 pagesManejo de Nutrición.darwin ortegaNo ratings yet
- Biomedicas - Geometria AnaliticaDocument2 pagesBiomedicas - Geometria AnaliticaJair MontalvoNo ratings yet
- Movimientos de TherbligsDocument7 pagesMovimientos de TherbligsAngel Rojas RamirezNo ratings yet
- Practca KerberosDocument6 pagesPractca KerberosEfren Eduardo Villegas ArreagaNo ratings yet
- El Método Científico-Diego A. Perez Pou 20-1638Document2 pagesEl Método Científico-Diego A. Perez Pou 20-1638Priscila ContrerasNo ratings yet