Professional Documents
Culture Documents
Guia N1 Quimica UB
Uploaded by
spotlight_brianCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Guia N1 Quimica UB
Uploaded by
spotlight_brianCopyright:
Available Formats
Guia
N
1
de
Ejercicios
de
Qumica
Profesor
Carrera
Unidad/Sub
Unidad
Contenidos
Brian
Alvarez
V.
Prevencion
de
Riesgos
/
Tecnico
en
Prevencion
de
Riesgos
Quimica
General
Determinacion
de
Peso
Molecular,
Formula
Empirica,
Calculo
de
moles,
moleculas,
gramos
INSTRUCCIONES:
1. Lea
atentamente
la
gua
y
sus
contenidos.
2. Cualquier
duda,
consultar
con
el
profesor
3. Los
ejercicos
estan
basados
especificamente
con
los
contenidos
entregados
en
clases
1-Calcular
el
peso
molecular
de:
a-CHCl3:
R:
119,5
g/mol
b-Al(OH)3
R:
78
g/mol
c-Fe2(SO4)3
R:
400
g/mol
d-C19H38O
R:
282
g/mol
2-Calcular
la
composicin
porcentual
del
Al2O3
R
:
Al
52,94%,
O
47,06%
3-El
anlisis
de
cierto
compuesto
revela
que
su
composicin
porcentual
en
masa
es
85,63%
de
C,
14,37%
de
H.
Cul
es
la
frmula
emprica
del
compuesto?
Si
la
masa
molecular
es
de
28
g/mol,
cul
es
la
frmula
molecular?
R
:
C2H4
4-Determine
la
frmula
emprica
de
un
compuesto
que
contiene
52.9%
de
aluminio
y
47.1%
de
oxgeno.
R:
Al2O3
5-Cul
es
la
frmula
molecular
del
compuesto
siguiente?
frmula
emprica
CH,
masa
molar
78
g/mol.
R:
C6H6
6-Cul
es
la
masa
en
gramos
de
0.257
mol
de
sacarosa,C12H22O11?
R:
87,89
g
7-Calcula
cuntos
moles,
litros
y
numero
de
molculas
hay
en
37
gramos
de
metano
(CH4)
en
CNPT.
R:
2,31
moles,
51,8
litros,
12,04
x
1023
molculas
8-Averigua
cuntas
molculas,
litros
y
moles
hay
en
38
gramos
de
oxgeno
(
O2)
en
CNTP.
R:
1,19
moles,
26,6
litros,
7,15
x
1023
molculas
9-Dnde
hay
ms
gramos:
en
107
molculas
de
amonaco
(NH3)
o
en
1.5
moles
de
agua
(H2O)?
R:
3.01x10-21
g
NH3,
27
g
de
H2O
10-Dnde hay ms partculas: en 3.3 moles de CaCO3 o en 69 gramos de Na?
11-El litio ha sido calificado como el petrleo blanco del siglo XXI por su uso en las bateras
recargables de equipos tecnolgicos (celulares, mp3, notebooks), construccin de automviles
elctricos e incluso en la generacin de energa nuclear. Determine Cuntos moles existen en 289
gramos de Litio (Li)?
R: 41.9 moles de Li
12-Cuntos gramos hay en 2,5 mol de Carbono (C)?
R: 30 g de C
13-El oro es el menos reactivo de todos los metales. Se llama un metal "noble" (un trmino
alquimista) porque no oxida bajo condiciones ordinarias, significando que nunca aherrumbrar y
nunca deslustrar. Determine la cantidad de tomos que estn contenidos en 5 mol de Oro (Au).
R: 3.01x1024 atomos de Au
14-El cobalto es ferromagntico y se parece al hierro y al nquel, en su dureza, resistencia a la
tensin, capacidad de uso en maquinaria, propiedades trmicas y comportamiento
electroqumico. Cuntos mol de cobalto hay en 6,00x109 de tomos de Co?.
R: 9,96x10-15 moles de Co
15-Los compuestos del plomo son txicos y han producido envenenamiento de trabajadores por
su uso inadecuado y por una exposicin excesiva a los mismos. Determine la cantidad de gramos
de Plomo (Pb) que estn contenidos en 6,022x1019 tomos de Plomo.
R: 0.020 g de Pb
16- El azufre se utiliza en la vulcanizacin del caucho, en atomizadores con azufre para combatir
parsitos de las plantas, en la manufactura de fertilizantes artificiales y en ciertos tipos de
cementos y aislantes elctricos, en algunos ungentos y medicinas y en la manufactura de plvora
y fsforos. Los compuestos de azufre se emplean en la manufactura de productos qumicos,
textiles, jabones, fertilizantes, pieles, plsticos, refrigerantes, agentes blanqueadores, drogas,
tintes, pinturas, papel y otros productos. Cuntos mol existen 12 gramos de azufre?
R: 0.375 g de S
17- Calcule la masa de un compuesto si 0,399 moles de l tiene una masa de 140g.
R: 55,86 g del compuesto
18-Cuntas molculas de etano (C2H6) estn presentes en 0,887g de Etano (C2H6)?
R: 1,78x1022 moleculas de C2H6
19- El etanol, CH3CH2OH, posee una densidad de 0,89 g/mL. Calcular el nmero de moles que hay
en 250 mL de etanol.
R: 4.83 moles de Etanol
20.- La Vitamina C es esencial para los humanos. Su frmula global es C6H8O6.
a) Calcular la masa molar (Peso molecular), de la Vitamina C.
b) Para 1,00 g de Vitamina C, calcular:
b1. El nmero de molculas. R: 3,4x1021 moleculas de Vit C
b2. El nmero de moles. R: 0.0056 moles de Vit C
You might also like
- Todas Las Cosas Que Escribí Cuando NingDocument95 pagesTodas Las Cosas Que Escribí Cuando Ningandrea avila perezNo ratings yet
- Empresa NestleDocument19 pagesEmpresa NestleJennifer Lopez HNo ratings yet
- Cuerpo HumanoDocument59 pagesCuerpo HumanoVíctor CatalàNo ratings yet
- No SirveDocument3 pagesNo Sirvespotlight_brianNo ratings yet
- Guia N2 Quimica UB - 2Document3 pagesGuia N2 Quimica UB - 2spotlight_brianNo ratings yet
- Lomo Archivador #1 Ant AdmsDocument1 pageLomo Archivador #1 Ant Admsspotlight_brianNo ratings yet
- 6284, Guía de ProductosDocument28 pages6284, Guía de Productosspotlight_brianNo ratings yet
- Guia Molalidad y Fraccion MolarDocument2 pagesGuia Molalidad y Fraccion Molarspotlight_brian0% (1)
- Guia N2 Quimica UB - 2Document3 pagesGuia N2 Quimica UB - 2spotlight_brian100% (1)
- Gua de Ejercicios DisolucionesDocument2 pagesGua de Ejercicios Disolucionesspotlight_brianNo ratings yet
- Con Senso SaunaDocument5 pagesCon Senso Saunaspotlight_brianNo ratings yet
- 05 AJG05 de 05Document116 pages05 AJG05 de 05Dennis Vicente AyalaNo ratings yet
- Conceptos de QuimicaDocument274 pagesConceptos de QuimicaladyyelitzaNo ratings yet
- Sistemas de tratamiento de agua para laboratoriosDocument6 pagesSistemas de tratamiento de agua para laboratoriosdilberth26No ratings yet
- Entrevista PDFDocument2 pagesEntrevista PDFspotlight_brianNo ratings yet
- Analisis GranulometricoDocument2 pagesAnalisis GranulometricoAnonymous TsKN7XZBNo ratings yet
- Anibal Matamala - Oro No EsDocument17 pagesAnibal Matamala - Oro No Esspotlight_brianNo ratings yet
- Plan de Mantenimiento Prevetntivo en Planta de CaféDocument94 pagesPlan de Mantenimiento Prevetntivo en Planta de CaféManuel MariñasNo ratings yet
- Fechas PresentacionDocument2 pagesFechas Presentacionspotlight_brianNo ratings yet
- PMC User Es PDFDocument51 pagesPMC User Es PDFspotlight_brianNo ratings yet
- Modulo Disoluciones 2 MedioDocument22 pagesModulo Disoluciones 2 Mediospotlight_brianNo ratings yet
- Carta Del Padre TraicionadoDocument1 pageCarta Del Padre Traicionadospotlight_brianNo ratings yet
- Gestión Ambiental, Auditorías y TLCDocument1 pageGestión Ambiental, Auditorías y TLCspotlight_brianNo ratings yet
- Guía de Ejercicios Nomenclatura2Document3 pagesGuía de Ejercicios Nomenclatura2spotlight_brianNo ratings yet
- Netbook en Muy Buen EstadoDocument3 pagesNetbook en Muy Buen Estadospotlight_brianNo ratings yet
- Ofrenda, Ritual y Terapia - Las Mesas Aymaras, Gerardo Fdz. JuárezDocument28 pagesOfrenda, Ritual y Terapia - Las Mesas Aymaras, Gerardo Fdz. JuárezNicolasa16No ratings yet
- Guia N2 Quimica UB - 2Document3 pagesGuia N2 Quimica UB - 2spotlight_brianNo ratings yet
- Decreto-90 1420917434Document16 pagesDecreto-90 1420917434spotlight_brianNo ratings yet
- Cuad Qcagral eDocument7 pagesCuad Qcagral espotlight_brianNo ratings yet
- 603 617 1 PBDocument8 pages603 617 1 PBspotlight_brianNo ratings yet
- Reseña 1-11Document2 pagesReseña 1-11spotlight_brianNo ratings yet
- 2015 Demre Modelo Prueba Ciencias Quimica PDFDocument50 pages2015 Demre Modelo Prueba Ciencias Quimica PDFVictoria Alejandra Ojeda ConchaNo ratings yet
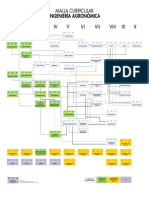
- Malla Curricular Ing Agronómica UNALDocument1 pageMalla Curricular Ing Agronómica UNALkmigeNo ratings yet
- Infografía Sobre El Cuidado Del Agua Ilustrada Moderna Verde y AzulDocument1 pageInfografía Sobre El Cuidado Del Agua Ilustrada Moderna Verde y AzulMelany RoblesNo ratings yet
- CALIBRACIONESDocument24 pagesCALIBRACIONESKene Aguilar ZanabriaNo ratings yet
- FT-SST-046 Formato Analisis de Amenzas y Vulnerabilidad QUINRAFFDocument15 pagesFT-SST-046 Formato Analisis de Amenzas y Vulnerabilidad QUINRAFFDora AmayaNo ratings yet
- Libro MalvicheDocument5 pagesLibro MalvicheAlexAnderAngeloNo ratings yet
- Lección 1 - Ge - GiDocument4 pagesLección 1 - Ge - GiAlejandra MandarinaNo ratings yet
- Unidad 1. Introducción A La Modelación y Simulación-2Document21 pagesUnidad 1. Introducción A La Modelación y Simulación-2Emmanuel Villegas Gutiérrez0% (1)
- El MODELO COGNITIVO DE LA DEPRESION DE BECK Y COLABORADORES PDFDocument14 pagesEl MODELO COGNITIVO DE LA DEPRESION DE BECK Y COLABORADORES PDFRomi Peralta De MarcoNo ratings yet
- Español 2ºDocument11 pagesEspañol 2ºPILAR GONZÁLEZNo ratings yet
- Historia Clínica MédicaDocument6 pagesHistoria Clínica MédicaRigoberto TorresNo ratings yet
- Fragmentos de Memoria. Profesores y luchas de la UTDocument374 pagesFragmentos de Memoria. Profesores y luchas de la UTdaniel garcíaNo ratings yet
- Clorofitas: Estudio de los géneros de la división ChlorophytaDocument10 pagesClorofitas: Estudio de los géneros de la división ChlorophytaANTONY ABEL ARONES MIGUELNo ratings yet
- Prueba de La ChispaDocument6 pagesPrueba de La ChispaEdgar LopezNo ratings yet
- Cáncer de Páncreas y CarcinomaDocument29 pagesCáncer de Páncreas y CarcinomaJuan ArgentNo ratings yet
- GM o Lum 562Document3 pagesGM o Lum 562GabrielaNo ratings yet
- Celulares y PdaDocument22 pagesCelulares y Pdayan100% (4)
- Guía de lectura para el análisis y comprensión de obras literariasDocument89 pagesGuía de lectura para el análisis y comprensión de obras literariasEmilio Sanchez BravoNo ratings yet
- Ensayo CISDocument8 pagesEnsayo CISalis castilloNo ratings yet
- Ensayo Sobre Ética NormativaDocument3 pagesEnsayo Sobre Ética NormativaSthefan Abad TorresNo ratings yet
- Especificaciones Tecnicas EstructurasDocument35 pagesEspecificaciones Tecnicas EstructurasLatex666No ratings yet
- Aplicaciones de La Curva e eDocument47 pagesAplicaciones de La Curva e ecirino fernandezNo ratings yet
- Estructuras de Drenaje SuperficialDocument10 pagesEstructuras de Drenaje SuperficialJersonCruzNo ratings yet
- InvertebradosDocument5 pagesInvertebradosIris BeltranNo ratings yet
- Analisis de Un CuentoDocument5 pagesAnalisis de Un Cuentonilsa yamile meloNo ratings yet
- Monografía Latin 2Document11 pagesMonografía Latin 2Gabriel Andres RaveraNo ratings yet
- Exploración de Vía Biliar 1 2Document49 pagesExploración de Vía Biliar 1 2Emmanuel NuñezNo ratings yet
- Pieza DubujoDocument19 pagesPieza DubujoAlisson NicoleNo ratings yet