Professional Documents
Culture Documents
Seminario 5 - Enzimas 2 - 2015
Uploaded by
Simón WitonCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Seminario 5 - Enzimas 2 - 2015
Uploaded by
Simón WitonCopyright:
Available Formats
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
SEMINARIO 5
Enzimas 2
Regulacin de la actividad enzimtica.
Inhibidores. Enzimas Michaelianas y alostricas
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
Inhibidores de la actividad enzimtica
La actividad de una enzima puede ser disminuida o eliminada completamente por la
accin de ciertas sustancias a las cuales se las conoce con el nombre genrico de
inhibidores enzimticos. Debemos aclarar que en este grupo de sustancias no deben
ser incluidos aquellos agentes que producen simplemente una destruccin irreversible de
la enzima, como podran ser todos aquellos que conducen a su desnaturalizacin, como
por ejemplo los cidos fuertes.
La inhibicin enzimtica es de gran importancia fisiolgica ya que, a veces, la inhibicin
de una sola enzima que forma parte de una cadena de reacciones metablicas puede
inhibir por completo a todo el proceso metablico involucrado y ejercer de esa forma un
efecto profundo y a veces fatal sobre el organismo. De ms est recalcar la importancia
que este fenmeno tiene en farmacologa y toxicologa como as tambin en el desarrollo
de herbicidas e insecticidas. De ah que el estudio del mecanismo de accin de los
inhibidores se haya constituido en una de las ms exploradas de la enzimologa prctica.
Los inhibidores pueden clasificarse en dos grandes grupos:
1) Irreversibles
2) Reversibles
i) competitivos
ii) no competitivos
En el primer caso, los inhibidores irreversibles, la enzima no recobra su actividad por
remocin del inhibidor libre. Esto es debido a que este tipo de inhibidores acta por lo
general modificando irreversiblemente o an destruyendo algunos de los grupos
esenciales del centro activo. En el segundo caso, los inhibidores reversibles, la enzima
recobra su actividad por remocin del inhibidor libre (por ejemplo, por simple dilisis), lo
cual demuestra que hay un equilibrio entre el inhibidor libre y la enzima.
Ejemplos de uno y otro tipo de inhibidores los encontramos entre los llamados reactivos
de tioles. Estas sustancias tienen la particularidad de reaccionar especficamente con
grupos sulfhidrilos (-SH) de las protenas presentes en los grupos laterales
correspondientes a los residuos de cistena. Existen ciertas enzimas que requieren para
actuar que algunos de esos grupos sulfhidrilos estn libres. Es evidente que en esos
casos los reactivos de tioles, al bloquear los grupos sulfhdrilos esenciales de estas
enzimas, pueden actuar como inhibidores.
Entre algunos reactivos de tioles
podemos
mencionar
al
pcloromercuribenzoato y el alquilante
Hg
COO - + ClH
Cl-Hg
COO -
iodoacetato, que ejemplifican a un
inhibidor reversible y a un inhibidor
P-cloromecuribenzoato
irreversible, respectivamente. Ambos
Enzima inactiva
Enzima
reaccionan con los grupos sulfhidrilos
libres de las protenas, pero mientras que el primero lo hace formando un complejo
reversible (mercaptida), el segundo forma un carboximetil-derivado de gran estabilidad,
incapaz de disociarse.
En el primer caso, una vez establecido el equilibrio, si se elimina el pcloromercuribenzoato la reaccin se va a desplazar hacia la izquierda por el principio de
accin de masas, disocindose el complejo enzima-inhibidor en enzima libre e inhibidor.
Si la eliminacin es total, toda la enzima recuperar su forma libre activa.
2
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
En cambio en el segundo caso, una vez formado el carboximetil-derivado, es imposible
disociarlo
dada
su
extraordinaria estabilidad,
por ende, la eliminacin del
exceso del inhibidor ser
ineficaz
para
hacer
recuperar
la
actividad
original.
Otro ejemplo de inhibicin irreversible es el representado por los llamados gases
neurotxicos que se desarrollaron durante la 2 Guerra Mundial, para ser utilizados como
gases de guerra. Son sustancias que reaccionan con el grupo alcohlico del resto lateral
correspondiente a la serina de algunas enzimas que tienen un hidroxilo en el centro activo
y que es necesario para que la enzima presente actividad.
Una enzima de este tipo es la acetilcolinestearasa que interviene en los procesos de
transmisin del impulso nervioso y cuya inhibicin causa, entre otros efectos, parlisis de
los msculos estriados.
acetilcolinestearasa
Acetilcolina + H2O colina + acetato
Una
de
las
primeras
sustancias que se utiliz
con este fin fue el
diisopropilfluorofosfato que
reacciona con la enzima
como se muestra en la
figura.
Se lo utiliz tambin como
insecticida (pertenece al
grupo de organofosforados).
Es muy efectivo pero
sumamente peligroso por su
volatilidad.
Vamos ahora a referirnos exclusivamente a la inhibicin reversible, en la cual el
inhibidor tambin interacta con algn grupo esencial de la enzima, pero hacindolo en
forma reversible. Las distintas formas de interacciones se traducen en varios tipos de
inhibicin perfectamente diferenciables experimentalmente. Los dos tipos ms comunes
son la competitiva y la no competitiva.
En la inhibicin competitiva el inhibidor se combina reversiblemente con la enzima en el
sitio por el cual se debera unir el sustrato, impidiendo por lo tanto la formacin del
complejo activo enzima-sustrato. De ah surge el nombre de competitiva, dado que
efectivamente tanto el inhibidor como el sustrato compiten por el mismo sitio y tratan de
desplazarse mutuamente de la enzima. Las posibles formas de reaccionar del sustrato y
el inhibidor con la enzima pueden presentarse por las ecuaciones:
Por ello este tipo de inhibicin se caracteriza en que puede disminuirse
considerablemente aumentando la concentracin de sustrato, de modo que desplace al
inhibidor.
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
Por ello este tipo de inhibicin se
caracteriza en que puede disminuirse
considerablemente aumentando la
concentracin de sustrato, de modo
que desplace al inhibidor.
En este tipo de inhibidores se
incluyen
sustancias
que
estructuralmente son muy parecidas
al sustrato (llamados anlogos
estructurales) y que, por lo tanto, pueden ocupar el lugar que ocupara el mismo en la
enzima pero no pueden ser atacadas por la misma.
Un ejemplo clsico de este tipo de inhibicin es el de la succinato deshidrogenasa,
enzima que tiene por sustrato el cido succnico. Puede ser inhibida por otras sustancias
estructuralmente parecidas al cido succnico, tales como el cido malnico, el cido
oxlico y el cido glutrico.
cido succnico
cido malnico
cido oxlico
cido glutrico
En la inhibicin no competitiva se postula que el inhibidor se une con la enzima en otro
sitio, que no es aquel por el cual se une el sustrato. Por esa razn la unin del sustrato
con la enzima no es afectada por la presencia del inhibidor y se puede formar entones un
complejo enzima-sustrato-inhibidor. Pero este complejo es catalticamente inactivo y no
puede escindirse en productos de la reaccin y complejo enzima-inhibidor. El inhibidor
presenta afinidad tanto por la enzima libre como por el complejo enzima-sustrato. En este
caso, las posibles formas de reaccionar del sustrato y el inhibidor con la enzima se
representan por las ecuaciones siguientes:
Este tipo de inhibicin se caracteriza
entonces porque no puede ser
revertida por un aumento de la
concentracin de sustrato. El sustrato
no puede desplazar al inhibidor unido
a la enzima.
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
Experimentalmente ambos tipos de inhibicin (competitiva y no competitiva) pueden
distinguirse fundamentalmente mediante la aplicacin del mtodo de Lineweaver-Burk
antes descripto a la reaccin enzimtica con y sin inhibidor, en cuyos respectivos casos
se obtendrn los grficos indicados en las figuras siguientes.
Inhibicin competitiva
Lineweaver-Burk
Michaelis-Menten
Vo
1/Vo
Vmx
Con inhibidor
Sin inhibidor
Con inhibidor
Vmx/2
1/Vmx
Sin inhibidor
Km
10
Km inh
(sustrato)
1/(S)
-1/Km -1/Km inh
Inhibicin NO competitiva
Lineweaver-Burk
Michaelis-Menten
1/Vo
Vo
Vmx
Con inhibidor
Sin inhibidor
Vmx/2
Sin inhibidor
Con inhibidor
1/Vmx inh
Vmx inh
Vmx inh/2
1/Vmx
Km = Km inh
(sustrato)
-1/Km
1/(S)
Como puede apreciarse en los grficos, en el caso de la inhibicin competitiva la Vmx
para una dada cantidad de enzima no se modifica por el agregado de inhibidor porque
agregando una concentracin lo suficientemente grande de sustrato se pude desplazar
completamente al inhibidor. Sin embargo, el Km aumenta porque la presencia del inhibidor
hace que se necesite una mayor cantidad de sustrato para saturar a la enzima que la que
se necesitara si el inhibidor no estuviera presente.
5
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
En contraposicin a lo anterior, en la inhibicin no competitiva, el inhibidor disminuye el
valor de la Vmx ya que el sistema se comporta como si la concentracin de la enzima
hubiera disminuido, dado que la fraccin de enzima unida al inhibidor no tiene actividad
cataltica. Sin embargo, no se modifica la Km ya que la unin del sustrato a la enzima no
est alterada por la simultnea unin del inhibidor.
En resumen:
Tipo de
Inhibicin
reversible
Sitio de unin de la
enzima
En presencia
del inhibidor
Esquema
- La unin del sustrato y
del inhibidor son
mutuamente excluyentes.
- A muy altas
concentraciones de
competitiva sustrato desaparece la
inhibicin.
- el valor de Km
aumenta
- Se mantiene el
valor de Vmx
- Por lo general, el
inhibidor competitivo es
un anlogo estructural del
sustrato.
no
competitiva
- Se une a un lugar
diferente del sitio activo
de la enzima
- Se une a la enzima libre
y tambin al complejo
enzima-sustrato
- El valor de Km
se mantiene
- Disminuye el
valor de Vmx
Enzimas alostricas
Las enzimas a las cuales nos hemos referido hasta este momento, las enzimas
michaelianas, corresponden a lo que se ha dado en llamar enzimas clsicas. Pero
adems existen ciertas enzimas con caractersticas regulatorias que poseen propiedades
que las distinguen de las primeras y que se denominan enzimas alostricas.
Las enzimas alostricas, como las clsicas, reconocen y se asocian en su centro activo a
un sustrato especfico y catalizan su conversin en productos. Pero estas enzimas,
adems, tienen la propiedad de reconocer selectivamente a uno o varios compuestos
distintos del sustrato cuya asociacin reversible con la protena tiene por efecto modificar
su actividad frente al sustrato, ya sea activndolo o inhibindolo, sin participar en nada en
la reaccin en s. Dichos compuestos, que reciben el nombre de efectores o
6
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
moduladores alostricos, interaccionan con la enzima en un sitio distinto y
generalmente distante del centro activo que recibe el nombre de sitio alostrico. Se
acepta que la asociacin del efector alostrico a la protena en el sitio alostrico produce
una alteracin de la configuracin espacial de la enzima (transicin alostrica) que se
transmite al centro activo, modificndolo de tal manera que la actividad de la enzima
aumenta o disminuye segn se trate de un efector o modulador alostrico positivo o
negativo, respectivamente.
Las enzimas alostricas tienen por lo general una estructura proteica ms compleja que la
de las enzimas no regulables o clsicas: estn constituidas por subunidades. Adems,
pueden responder a la accin de ms de un efector alostrico (positivos y/o negativos), en
cuyo caso poseen en su estructura un sitio alostrico distinto para cada uno de ellos.
Desde ese punto de vista, las enzimas alostricas pueden clasificar en tres grandes
grupos:
a) Homotrficas: en las cuales el mismo sustrato puede actual como modulador,
generalmente positivo.
b) Heterotrficas: aquellas que son moduladas positiva o negativamente por
sustancias distintas del sustrato, para cada una de las cuales la enzima posee un
sitio especfico de reconocimiento.
c) Homotrficas-heterotrficas: responden a efectos regulatorios del mismo
sustrato y de sustancias distintas del mismo.
Desde el punto de vista metablico estas enzimas, que generalmente catalizan
reacciones prcticamente irreversibles, se encuentran ubicadas estratgicamente en
ciertos puntos de las vas metablicas, de tal manera que su regulacin coopera en forma
efectiva en la economa general de la clula. As, por ejemplo, las encontramos como
primera enzima de una secuencia de reacciones, de tal manera que su activacin o
inhibicin aumente o disminuya respectivamente la velocidad de toda la va metablica
involucrada de acuerdo a las necesidades de la clula.
Las enzimas alostricas tienen propiedades
cinticas de las diferencian de las enzimas
michaelianas. Si bien exhiben saturacin cuando
la [S] es suficientemente alta, cuando se grafica
V0 en funcin de [S] algunas enzimas alostricas
muestran una curva de tipo sigmoidal, no
hiperblica como las enzimas michaelianas
clsicas. En estas curvas sigmoidales podemos
encontrar tambin un valor de [S] en el cual la V0
V0
Vmx
Vmx
2
K0,5
[S]
7
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
es la mitad de la Vmx, pero no podemos referirnos a este valor como Km, ya que estas
enzimas no siguen la relacin hiperblica de Michaelis Menten. Se la representa entonces
como K0,5 o Km aparente.
Comnmente, el sustrato acta tambin como modulador positivo (homotrficas): la unin
de una molcula de sustrato altera la conformacin de la enzima, incrementando la unin
de subsecuentes molculas de sustrato. Esto explica el cintica sigmoidal observada en el
cambio de V0 con [S] crecientes. Una caracterstica de la cintica sigmoidal es que los
pequeos cambios en la concentracin de un modulador pueden estar asociados con
grandes cambios en la actividad, sobre todo en [S] cercanas a la parte empinada de la
curva. En el caso de las enzimas alostricas heterotrficas, donde los moduladores son
otros metabolitos diferentes al sustrato, es difcil generalizar cmo se modifica la forma de
la curva de saturacin de sustrato. Hablaremos un poco de ello ms adelante.
Modelos para las enzimas alostricas
Se han propuesto algunos modelos para interpretar las interacciones entre la protena, el
sustrato y el o los efectores de las enzimas alostricas. Entre ellos vamos a describir
brevemente los debidos a Monod, Wyman y Changeux (1965) y a Koshland, Nemethy y
Filmes (1966).
El primero de ellos, conocido con el nombre de modelo concertado simtrico (Monod,
Wyman y Changeux), parte del supuesto de que la protena regulatoria (oligmero)
consiste de dos o ms subunidades idnticas (protmeros) que se asocian de tal manera
que la molcula posea por lo menos un eje de simetra. Cada subunidad contiene un sitio
de unin para cada sustrato y efector, mantenindose la simetra de la molcula. Cada
subunidad puede existir en dos estados conformacionales distintos: estados R y T, que
difieren en la posibilidad que poseen de unirse al o los sustratos y los efectores. As la
forma R (relajada) tiene afinidad por el sustrato y por lo tanta alta actividad, mientras
que la forma T (tensa) tiene baja afinidad por el mismo y por ende baja actividad. La
transicin de una conformacin de una subunidad es concertada con la correspondiente
transicin en las subunidades vecinas, de tal manera que todas las subunidades se
encuentren en el mismo estado conformacional simultneamente y la simetra molecular
se mantenga. Es decir, la enzima tiene solo dos estados globales de "todo o nada". Por
otra parte, el equilibrio entre la forma R y la forma T se establece en ausencia de los
sustratos y efectores.
Los sustratos y activadores tienen mayor afinidad por el estado R y los inhibidores por el
estado T. De esta forma, los ligandos van a desplazar el equilibrio entre los estados T y R,
de modo que todas las subunidades de la enzima se encuentren en uno u otro estado.
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
En la figura se representa esquemticamente este modelo para una protena oligomrica
constituida por dos subunidades en la cual sustrato (S) y el efector positivo (A) se unen
slo al estado R, mientras que el inhibidor (I) lo hace exclusivamente al estado T. En
ausencia de sustrato y activador el equilibrio entre los estados T y R est desplazado
hacia el estado T, es decir la mayor parte de las molculas de la enzima se encuentran al
estado T. Al agregarse el sustrato (S) o el activador (A), y dado que estos ligandos se
unen selectivamente a las molculas que se encuentran en el estado R, el equilibrio se
desplaza en este sentido.
Como la transicin entre las formas T y R para las subunidades es concertada, es
suficiente la unin de la molcula de sustrato o activador a una sola de las subunidades
para que la otra quede en la forma R, dejando de esa forma disponible otro sitio de ms
alta afinidad para el sustrato. Cuanto ms sustrato o activador se agregue mayor ser el
nmero de oligmeros en la forma R, observndose en consecuencia lo que se denomina
un efecto cooperativo positivo del sustrato y del activador, que se traduce en una curva
de saturacin sigmoide. En el primer caso (sustrato), y de acuerdo a lo que se indic
anteriormente,
el
efecto
ser
homotrfico cooperativo o positivo
y en el segundo caso (activador),
heterotrfico
cooperativo
o
positivo. Pero si se agrega activador
en cantidad suficiente, el equilibrio
quedar totalmente desplazado hacia
la forma R, y todas las molculas del
oligmero estarn exclusivamente en
esa forma y la adicin del sustrato en
ese caso, no podr producir un mayor
desplazamiento
del
equilibrio,
comportndose entonces el sistema
como un sistema para el cual es vlido
un tratamiento cintico del tipo
Michaelis-Menten, obtenindose entonces una curva de saturacin para el sustrato de tipo
hiperblico.
En contraste con lo que ocurre con el sustrato y el activador, el inhibidor se une
exclusivamente a la forman T. Si debido a la presencia de sustrato en concentracin
saturante, la enzima se encontraba originalmente casi exclusivamente en el estado R, el
agregado de inhibidor producir un desplazamiento hacia la forma T y por ende la curva
9
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
de saturacin para el sustrato se har ms sigmoide a medida que aumenta la
concentracin del inhibidor. El efecto en este caso ser heterotrfico negativo (del
inhibidor con respecto al sustrato).
El modelo de Koshland, Nemethy y Filmer tambin denominado modelo secuencial se
basa en la explicada teora del ajuste inducido. El modelo establece que la unin de un
ligando (sustrato, activador o inhibidor) a una de las subunidades de la molcula
enzimtica oligomrica, produce un cambio conformacional de dicha subunidad. Esa
distorsin en una subunidad puede afectar secuencialmente la estabilidad y configuracin
de las subunidades vecinas, en la misma forma que la distorsin de una parte de una
cadena polipeptdica, aumentando o disminuyendo la afinidad de las mismas por el
sustrato. La siguiente figura ilustra lo dicho para el caso de una enzima alostrica que
posee dos subunidades, cada una de ellas capaz de unirse a una molcula de sustrato y
que presenta un efecto homotrfico positivo de S sobre S.
En el modelo secuencial las interacciones entre las subunidades son posibles estando las
subunidades en distintos estados conformacionales.
En el modelo concertado slo seran posibles los estados TT y RR de la figura anterior y
no el hbrido TR, los cuales por otra parte deben preexistir actuando el ligando como
estabilizador del estado al cual se une preferencialmente. En cambio el modelo
secuencial, si bien no descarta la posibilidad extrema de un cambio simultneo en todas
las subunidades, sostiene preferentemente la existencia de cambios secuenciales en la
conformacin de las subunidades inducidas por la unin del o los ligandos, con la
posibilidad de ocurrencia de estados conformacionales hbridos cuando la protena est
parcialmente saturada.
Enzimas alostricas
- Las enzimas alostricas presentan estructura cuaternaria.
- Tienen diferentes sitios activos, unen ms de una molcula de
sustrato
- La unin del sustrato es cooperativa
- La curva de velocidad en funcin de la (s) presenta una forma
sigmoidea
- Pequeos cambios en la concentracin del modulador se asocian
con grandes cambios en la actividad de la enzima
10
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
Regulacin enzimtica
Cuanto ms se avanza en el conocimiento de la bioqumica celular, especialmente por los
aportes hechos en los ltimos aos por la biologa molecular, ms se afianza el concepto
enunciado oportunamente por Changeux, de equiparar el funcionamiento de una clula al
de una verdadera fbrica qumica automtica diseada para aprovechar lo ms
eficientemente la energa disponible. En efecto, en una fbrica automtica coexisten
varias lneas de produccin que trabajan simultneamente en forma concertada y que se
regulan a s mismas y entre ellas por medio de controles automticos, consistentes en
circuitos electrnicos especficos de retroalimentacin.
Estos principios pueden aplicarse tambin a los seres vivos. As, el funcionamiento de la
clula ms sencilla, implica la existencia de una verdadera maraa de procesos
metablicos consistentes en secuencias de reacciones qumicas catalizadas por enzimas
especficas. Cada una de estas vas metablicas sera equiparable a las mencionadas
lneas de produccin de la fbrica automtica y las mquinas elementales de la fbrica
celular seran las mencionadas enzimas. Existen en principio cuatro formas posibles de
que la clula controle la velocidad de funcionamiento de dichas vas metablicas:
1) DISPONIBILIDAD DE SUSTRATO
Como ya hemos indicado, la actividad de la enzima guarda proporcionalidad con los
niveles de sustrato. Estos determinan la mayor o menor velocidad en la actividad
enzimtica. Al aumentar la concentracin de sustrato en la clula aumenta su utilizacin y
viceversa. Generalmente el sustrato debe ingresar a la clula o al interior de una
organela. Ejemplo: -oxidacin y sntesis de cuerpos cetnicos.
2) MODIFICACIN COVALENTE
Muchas enzimas son reguladas por el agregado o sustraccin de grupos unidos
covalentemente a la misma.
La regulacin covalente ms frecuente se realiza por modificacin de los residuos de
tirosina, serina y/o treonina de las enzimas por un proceso de unin o eliminacin de
grupos fosfatos. Existen tambin enzimas cuya actividad es modulada por la insercin
covalente de otros grupos., como se muestra en la siguiente tabla:
11
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
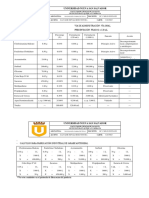
En la siguiente tabla se dan ejemplos de algunas enzimas cuyas actividades estn
reguladas por modificacin covalente que implica fosfo- desfosforilaciones.
3) MODULACIN ALOSTRICA.
Ya se describi anteriormente. Algunos casos particulares dan origen a diferentes modos
regulatorios.
12
DEPARTAMENTO DE BIOQUMICA HUMANA
MATERIA QUMICA BIOLGICA - CICLO LECTIVO 2015
En algunas vas metablicas, la enzima que cataliza
la primera etapa de la serie suele ser inhibida por el
producto de la ltima. Cuando la concentracin de
ese producto final aumenta, ello indica que su
elaboracin excede las necesidades y se frena el
funcionamiento de la va reduciendo la actividad de la
enzima reguladora. Se habla de un proceso de
retroinhibicin.
Tambin puede suceder que una enzima sea
estimulada por algn agente que se acumula en el
medio. Cuando existe un exceso de sustrato, l
mismo promueve su utilizacin activando a la enzima.
E1
E2
E3
E4
S1 A B C
+
E1 E2 E3 E4
S1 X Y Z P
4) INDUCCIN O REPRESIN DE LA SINTSIS DE LA ENZIMA.
Implica el control de la sntesis de las enzimas regulatorias involucradas en un camino
metablico. Se habla entonces de induccin enzimtica o represin enzimtica segn
que la velocidad de produccin de una dada enzima (o de un conjunto de enzimas
metablicamente relacionadas) y por ende su concentracin celular, sea aumentada o
disminuida respectivamente como respuesta a las necesidades de la clula, actuando por
lo general un metabolito particular como seal desencadenante del proceso. En el caso
de la induccin, ese metabolito puede ser el mismo sustrato de la enzima (metabolito
inductor), y en la represin, el producto final de la va metablica de la cual la enzima
reprimida forma parte (metabolito represor). Este mecanismo es mucho ms lento que los
anteriores ya que implica la sntesis o degradacin de las enzimas involucradas.
13
You might also like
- Código Ético Del Tecnico de FarmaciaDocument6 pagesCódigo Ético Del Tecnico de FarmaciaHeidy Marisa Morales Cartty100% (1)
- Ley Nacional de FolkloreDocument4 pagesLey Nacional de FolkloreSimón WitonNo ratings yet
- Temario HerreriaDocument1 pageTemario HerreriaDaniel DanielsenNo ratings yet
- Documento CompletoDocument12 pagesDocumento CompletoSimón WitonNo ratings yet
- EstudiosDocument2 pagesEstudiosSimón WitonNo ratings yet
- Manual de Soldadura INDURA PDFDocument175 pagesManual de Soldadura INDURA PDFjorge_rubio1115No ratings yet
- Arte y Etnografia Levi StraussDocument8 pagesArte y Etnografia Levi StraussRolandoJaimeNo ratings yet
- Descripcion DensaDocument17 pagesDescripcion DensaMarcela CárcamoNo ratings yet
- Las Fibras Miocárdicas IndividualesDocument6 pagesLas Fibras Miocárdicas IndividualesSimón WitonNo ratings yet
- Curvas RespiradorDocument13 pagesCurvas RespiradorJesus PerezNo ratings yet
- Higado Ictericia 2015 CrisDocument63 pagesHigado Ictericia 2015 CrisSimón WitonNo ratings yet
- In Cretin AsDocument4 pagesIn Cretin AsSimón WitonNo ratings yet
- Balance Glomerulotubular Retroalimentacion TubuloglomerularDocument22 pagesBalance Glomerulotubular Retroalimentacion TubuloglomerularSimón WitonNo ratings yet
- 8471 PDFDocument6 pages8471 PDFFiorella Perez MedranoNo ratings yet
- Monitorizacion Invasiva y No InvasivaDocument10 pagesMonitorizacion Invasiva y No Invasivam_ale437396No ratings yet
- Pruebas de FuncionDocument17 pagesPruebas de FuncionSenobia Álvarez VeraNo ratings yet
- Manual de Soldadura INDURA PDFDocument175 pagesManual de Soldadura INDURA PDFjorge_rubio1115No ratings yet
- Pares CranealesDocument2 pagesPares CranealesSimón WitonNo ratings yet
- Temario HerreriaDocument1 pageTemario HerreriaDaniel DanielsenNo ratings yet
- DopplerDocument4 pagesDopplerSimón WitonNo ratings yet
- CienCIA Nueva 18Document68 pagesCienCIA Nueva 18Simón WitonNo ratings yet
- Cap 4 La HemorragiaDocument5 pagesCap 4 La HemorragiaDaniel AlfaroNo ratings yet
- Tronco Encefalico Configuración InternaDocument19 pagesTronco Encefalico Configuración InternaMorfologia Aplicada100% (3)
- Clase No 12 Oscar Varsavsky 2014Document27 pagesClase No 12 Oscar Varsavsky 2014juancomunaNo ratings yet
- Diabetes 2Document38 pagesDiabetes 2Simón WitonNo ratings yet
- Atlas de Anatomía Depto Anatomía FMed UBADocument202 pagesAtlas de Anatomía Depto Anatomía FMed UBALaura Panique LazcanoNo ratings yet
- Mdicamentos CitostticosDocument15 pagesMdicamentos CitostticosSimón WitonNo ratings yet
- BIOQUIMICA TERCERA EDICION Libro de Text PDFDocument6 pagesBIOQUIMICA TERCERA EDICION Libro de Text PDFwaldirNo ratings yet
- Casos Clinicos 2012 13 29junio PDFDocument85 pagesCasos Clinicos 2012 13 29junio PDFSimón WitonNo ratings yet
- Bioquimica MedicaDocument17 pagesBioquimica MedicaNay Snyder Ballesteros EspinozaNo ratings yet
- AntispicoticosDocument28 pagesAntispicoticosAlejandra Ovalle100% (1)
- Empresas en Mi Localidad - Aaron SiccosDocument3 pagesEmpresas en Mi Localidad - Aaron Siccosjuan aaronNo ratings yet
- Gráficos para Materialización RadiestésicaDocument2 pagesGráficos para Materialización RadiestésicajanethCNo ratings yet
- Ivc Vig FM052Document4 pagesIvc Vig FM052Camilo LopezNo ratings yet
- VademecumDocument37 pagesVademecumSofia Carolina AvellanedaNo ratings yet
- RAMS Farmacia 2013Document44 pagesRAMS Farmacia 2013joseph_uni100% (1)
- FARMACOLOGIA EN ODONTOPEDIATRIA para Unne Virtual 1Document21 pagesFARMACOLOGIA EN ODONTOPEDIATRIA para Unne Virtual 1DistribuidoraJasmine JDNo ratings yet
- Calculo-Jarabe Antigripal y Elixir AntiespasmódicoDocument4 pagesCalculo-Jarabe Antigripal y Elixir AntiespasmódicoNeftali VenturaNo ratings yet
- Paracetamol o AcetaminofenDocument11 pagesParacetamol o AcetaminofenZuriel MartinezNo ratings yet
- Aparato Digestivo - OtcDocument24 pagesAparato Digestivo - OtcLuis EnriqueNo ratings yet
- Taller 1 y 2 Comp 7Document9 pagesTaller 1 y 2 Comp 7vivianaNo ratings yet
- Clasificacion de AntiarrítmicosDocument2 pagesClasificacion de AntiarrítmicosMarielyCancelaNo ratings yet
- Requisito MedicamentosDocument10 pagesRequisito MedicamentosANA RIVERANo ratings yet
- Lista Chequeo de ExperienciaDocument4 pagesLista Chequeo de ExperienciaIván Leonardo Rodríguez BarreroNo ratings yet
- Rtca 11.03.56 09Document10 pagesRtca 11.03.56 09Oscar GonzalezNo ratings yet
- Introducción A La FarmacologíaDocument58 pagesIntroducción A La FarmacologíaSHEYLA SHARINA FUENTES PINTO100% (3)
- Informe Gestion Comercial Trabajo FinalDocument10 pagesInforme Gestion Comercial Trabajo FinalCarlos ToscanoNo ratings yet
- Ac Citric Anh SucroalDocument2 pagesAc Citric Anh SucroalSo MINo ratings yet
- Ensayo Historia de La FarmaciaDocument3 pagesEnsayo Historia de La FarmaciaCarlos CogolloNo ratings yet
- Prioridad de P.ADocument34 pagesPrioridad de P.AMauricio PradinesNo ratings yet
- Técnicas para La Aplicación de Las Distintas Hierbas MedicinalesDocument2 pagesTécnicas para La Aplicación de Las Distintas Hierbas MedicinalesIvonne Jager Ramirez100% (1)
- Sulfato de HierroDocument8 pagesSulfato de HierroWalter Cerna QuevedoNo ratings yet
- AnestésicosDocument44 pagesAnestésicosGabriel MontoyaNo ratings yet
- Guía de Trabajos Prácticos Tecnología Farmacéutica 2004Document42 pagesGuía de Trabajos Prácticos Tecnología Farmacéutica 2004eliceriosaavedraNo ratings yet
- Reporte 5 - Preparacion de Acido Salicilico y Sintesis de La Aspirina!Document22 pagesReporte 5 - Preparacion de Acido Salicilico y Sintesis de La Aspirina!Ligia FletesNo ratings yet
- PC-SF-02 Control de Factores AmbientalesDocument3 pagesPC-SF-02 Control de Factores AmbientalesJuan Carlos Hernandez0% (1)
- Mezclado de SólidosDocument16 pagesMezclado de SólidosManuel Alexander Albujar Zelada100% (1)
- Phar2250 M3 Reglamento 156 Caps 7 8Document44 pagesPhar2250 M3 Reglamento 156 Caps 7 8Xia xiang Maldonado AstacioNo ratings yet
- Adicion de MedicamentosDocument7 pagesAdicion de MedicamentosYuridia Chávez R100% (1)