Professional Documents
Culture Documents
Capitulo 1
Uploaded by
ushuaia7745Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Capitulo 1
Uploaded by
ushuaia7745Copyright:
Available Formats
Ejercicios y problemas de Termodinmica I
CAPTULO 1
Principio cero de la termodinmica y temperatura. Ecuaciones de estado.
Coeficientes termodinmicos importantes. Relaciones diferenciales en
termodinmica.
Resumen de teora:
Principio cero de la termodinmica:
- Dos sistemas aislados A y B puestos en contacto prolongado alcanzan el
equilibrio trmico.
- Si A y B separadamente estn en equilibro trmico con C, estn tambin en
equilibrio trmico entre si. (Propiedad transitiva)
Temperatura emprica:
( x) = 273.16
Ecuaciones de estado importantes:
Gas ideal:
Slido paramagntico (Ley de Curie):
x
x PT
pV = nRT
TM = HC
Gas de Van der Waals:
n2a
p + 2 (V nb) = nRT
V
Coeficientes termodinmicos importantes:
Dilatacin cbica
Compresibilidad isoterma
1 V
1 V
=
T =
V T p
V p T
Piezotrmico
1 p
=
p T V
Julin Moreno Mestre
Problemas:
1
Los sistemas A y B son sales paramagnticas con coordenadas (H, M) y (H, M)
respectivamente, mientras que el sistema C es un gas con coordenadas (p, V). Cuando
A y C estn en equilibrio trmico se cumple: nRcH MpV = 0 , y cuando lo estn B y
C se cumple: M ' pV nR(c' H '+ aM ' ) = 0 , siendo los smbolos n, R, a, c y c
constantes:
a) Cules son las funciones, del par de variables de cada sistema, iguales entre si
en el equilibrio trmico?
b) Cul es la relacin que expresa el equilibrio trmico entre los sistemas A y B?
Solucin:
a) Partiendo de las relaciones entre los sistemas en el equilibrio, las funciones del par
de variables iguales entre si en el equilibrio son:
nRcH
nRcH MpV = 0 pV =
nRcH nR (c ' H '+ aM ')
M
=
pV =
M
M'
nR(c ' H '+ aM ')
M ' pV nR(c ' H '+ aM ') = 0 pV =
M'
b) La relacin en el equilibrio entre los sistemas A y B la extraemos a partir de la
relacin obtenida en el apartado a):
RcH R(c ' H '+ aM ')
nRcH nR(c ' H '+ aM ')
=
=
M
M'
M
M'
2
Los sistemas A y B son gases ideales con coordenadas (p,V) y (p,V), respectivamente,
y el sistema C es una sustancia elstica de coordenadas (F,L). Cuando A y C estn en
equilibrio trmico se cumple:
L L2
kpV 20 FR = 0
L0 L
Cuando estn en equilibrio trmico A y B se cumple:
pV p '(V ' b) = 0
siendo b, R, k y L0 constantes. Cules son las funciones del par de variables de cada
sistema, iguales entre s en el equilibrio trmico? Cul es la relacin que expresa el
equilibrio trmico entre los sistemas B y C?
Solucin: Partiendo de las relaciones de equilibrio:
L L2
FR
kpV 20 FR = 0 pV =
1
L L20
FR L L20
L0 L
k 2 pV = p '(V ' b) =
k L0 L2
L0 L
pV p '(V ' b) = 0 pV = p '(V ' b)
Partiendo de la relacin entre el par de variables de cada sistema en el equilibrio,
podemos deducir la relacin que expresa el equilibrio trmico entre B y C:
FR L L20
p '(V ' b) =
k L0 L2
Ejercicios y problemas de Termodinmica I
3
Un slido dielctrico tiene como variables la polarizacin , P, y el campo elctrico E,
una sal paramagntica la imanacin, I, y el campo magntico H y un gas tiene las
coordenadas presin, p, y la densidad . Cuando estn en equilibrio mutuo, el primero
y el segundo:
d EH = IP
y cuando estn en equilibrio el primero y el tercero cumplen la condicin:
pP = d E
donde y son constantes y d es la susceptibilidad dielctrica del material no
conductor. Cul es la ecuacin que expresa el equilibrio trmico entre el segundo y el
tercer sistema? Tomando como temperatura emprica la del gas ideal: T = MpV / mR ,
donde M es la masa molecular del gas, determinar las ecuaciones de estado de los tres
sistemas. (Carranza)
Solucin: Despejamos d E en las ecuaciones del equilibrio antes citadas:
d EH = IP d E=
IP
IP pP
H
d E=
=
pP
H
pP = d E d E=
Por tanto el equilibrio entre el segundo y el tercero es:
I p
=
H
En el problema la temperatura emprica del gas es:
p
T=
Partiendo que la temperatura emprica del gas ideal es:
MpV Mp V Mp M p
=
=
=
T=
mR
R m R R
Esto significa que la constante es:
M
=
R
Por tanto la temperatura emprica del gas es:
M p
T=
R
Por la relacin de equilibrio de la sal y el gas sabemos que la temperatura de la sal es:
I
T =
H
Y por ello tambin sabemos que la temperatura emprica del slido dielctrico ser:
E
IP
d E=
= PT d E = PT T = d
P
H
Julin Moreno Mestre
4
Tres sistemas, que llamaremos 1, 2 y 3 y que tienen el volumen y la presin como
variables mecnicas, se ponen en contacto trmico por parejas. Cuando el primero y el
tercero estn en equilibrio trmico se cumplen:
p1V1 p2V2 = bp1
y cuando lo estn el segundo y el tercero:
V3 ( p2V2 p3V3 ) = a
donde a y b son constantes. Cumplen estos tres gases el principio cero? Si lo hacen,
Cules son las funciones que se igualan en el equilibrio trmico? (Carranza)
Solucin: Si lo cumplen, ya que existen dos ecuaciones que relacionan las variables de
estado de dos sistemas con uno de ellos, y esto implicar que todos los tres sistemas
van a estar ligados en el equilibrio por tres ecuaciones. Por tanto las funciones que se
igualan en el equilibro trmico son:
p2V2 = p1V1 bp1
p1V1 p2V2 = bp1
a
p2V2 = p1V1 bp1 = + p3V3
p2V2 = + p3V3
V3 ( p2V2 p3V3 ) = a
V3
V3
Tres gases 1, 2 y 3, cumplen las siguientes ecuaciones cuando se encuentran en
equilibrio trmico mutuo entre parejas:
p2 + V2
k p2 + hV2
ln V1 =
+ ln
ln p3 =
+ ln
hV3
p1
donde , , k y h son constantes. Determinar las relaciones necesarias entre las
constantes para que se cumpla el principio cero y las funciones que definen la
temperatura emprica en cada sistema.
Solucin: Realizamos un par de operaciones algebraicas:
k p + hV2
p2 + V2
ln p3 = 2
+ ln
+ ln
ln V1 =
hV3
p1
ln
V1
p1 ln
p2 + V2
p1
V1
ln
= p2 + V2
p3
hV3 ln
k p2 + hV2
hV3
p3
= k p2 + hV2
Si las constantes k y h son proporcionales a y respectivamente, se cumplir el
principio cero:
k = m
h = m
Donde m es una constante de proporcionalidad. Finalmente por igualacin y
simplificacin obtenemos:
p
V
p2 + V2 = p1 ln 1 = V3 ln 3
Se define la temperatura emprica como = ( X , Y ) , en nuestro caso = ( p, V ) . Por
tanto las funciones que describen la temperatura emprica en los sistemas descritos son:
p
V
1 ( p1 , V1 ) = p1 ln 1
2 ( p2 ,V2 ) = p2 + V2
3 ( p3 ,V3 ) = V3 ln 3
Ejercicios y problemas de Termodinmica I
6
Los valores lmites a p 0 del producto pV en un termmetro de gas a volumen
constante, en contacto trmico con dos sistemas, 1 y 2, son 45.423 y 53.394 Pam3,
respectivamente. Calclese la relacin de temperaturas T ( 1)/T( 2), de los dos
sistemas. Si el sistema 1 es una clula de punto triple del agua, cul es la temperatura
T( 2)?
Solucin: Partiendo de la definicin de temperatura en nuestro caso:
= ( X , Y ) = ( p,V ) = pV
Por tanto la relacin de temperaturas:
T (1 ) p1V
p 45.423
=
= 1 =
= 0.851
T ( 2 ) p2V p2 53.394
Supngase que se define una escala absoluta de temperaturas, T, tal que la diferencia
entre el punto triple del agua y el cero absoluto son 300 grados. Cul sera la
temperatura del punto de ebullicin del agua? (La temperatura del punto de ebullicin
del agua en la escala absoluta habitual es 373.15K).
Solucin: Considerando la antigua temperatura en Kelvin, la aplicamos para conocer
las temperaturas en la nueva escala absoluta. Utilizamos la siguiente expresin:
x
T ( x) = 273.16
x3
Colocamos la temperatura del punto triple x3 de la nueva escala absoluta de
temperaturas y consideraremos x como la temperatura de ebullicin del agua en la
nueva escala, y T(x) , resultando la ecuacin:
x
373.15
x = 300
= 409.81
373.15 = 273.16
300
273.16
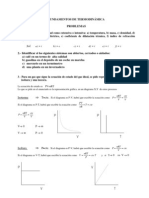
Un termmetro de gas, a volumen constante, se utiliza para determinar la temperatura
absoluta de un sistema. Las lecturas corregidas de la presin en el bulbo cuando, lleno
con diversas cantidades de gas, se pone en contacto con agua en el punto triple (p0) y
con el sistema (p) son:
p0 (mmHg)
1000.00
800.00
500.00
200.00
100.00
p (mmHg)
1296.02
1036.86
648.11
259.30
129.66
Calclese la temperatura del sistema en la escala de los gases ideales.
Solucin: Partiendo de la temperatura del agua en el punto triple y de la expresin:
p
p
T = T0
= 273.16
p0
p0
Determinamos cual es la temperatura calculada del sistema para cada muestra de gas:
p0 (mmHg)
1000.00
800.00
500.00
200.00
100.00
p (mmHg)
1296.02
1036.86
648.11
259.30
129.66
T (K)
354.02
354.04
354.08
354.15
354.18
Haciendo una media aritmtica de las temperaturas nos da como resultado aproximado
de la temperatura del sistema 354.09 K.
10
Julin Moreno Mestre
9
Un termistor obedece la ley:
R (T ) = R 0 e B / T
donde R 0 y B son constantes. Cuando se calibra dicho termistor en el punto triple del
agua se encuentra una resistencia R 3 = 938.7 y en el punto de vapor Rv = 1055.2 .
Hallar la temperatura que mide ese termistor cuando su lectura es R = 1004,5 .
Solucin: Planteemos el sistema de ecuaciones exponenciales que se nos plantea para
calcular la temperatura que nos piden que medira el termistor:
938.7 = R 0 e B / 273.16 B = 119.26 K
1055.2 = R 0 e B / 373.16 R0 = 1452.6
Y ahora deducimos la temperatura del termistor sustituyendo las constantes:
1004.5 = 1452.6e 119.26 / T T = 324.24 K
10 Un termopar se calibra manteniendo una de sus dos soldaduras en el punto de hielo,
th = 0.00 C, y se obtiene:
(t ) = t + t 2
donde = 0.04 mV/C y = 4.0010-6 mV/C2. Determinar la fuerza electromotriz que
produce dicho termopar cuando una soldadura se encuentra en el punto de vapor,
tv = 100.00 C y la otra en el punto de fusin del cinc, tZn = 419.53 C. (Carranza)
Solucin: La fuerza electromotriz producida por el termopar entre las dos soldaduras
ser debida a la diferencia de potencial generada en las dos soldaduras a distintas
temperaturas:
T = (tZn ) (tv ) = 17.48 4.04 = 13.44 mV
11 La resistencia de un termmetro de platino es de 18.56 en el punto de fusin del
estao y de 9.83 en el punto triple del agua. En estos mismos puntos las presiones de
un termmetro de H2 a volumen constante son 17.2 atm y 6.80 atm. Para otra cantidad
de gas en el bulbo se obtiene 1.85 atm y 1.00 atm. Adems, las fuerzas electromotrices
de un termmetro cobre-niquel en los mismos puntos son 9.02 mV y 2.98 mV.
Determnese la temperatura de fusin del estao en las distintas escalas termomtricas.
Solucin: Utilizaremos en los clculos la expresin:
X
TSn = 273.16 Sn
X3
Calcularemos la temperatura ahora en cada termmetro:
18.56
Termmetro de platino: TSn = 273.16
= 515.76 K
9.83
12.7
= 510.17 K
Termmetro de gas H2: TSn = 273.16
6.8
1.85
= 505.35 K
Termmetro de otro gas: TSn = 273.16
1
9.02
Termmetro de Cu-Ni: TSn = 273.16
= 826.81 K
2.98
11
Ejercicios y problemas de Termodinmica I
12 La ecuacin de estado de un gas perfecto es:
pV = nRT
Calcular el coeficiciente de compresibilidad isoterma y de dilatacin cbica.
Solucin: Partiendo de las expresiones diferenciales de dichos coeficientes, derivando
determinaremos los mismos:
1
1
1 V
nR 1
1 V
nRT 1
= =
=
T =
=
= T =
=
2
p
T
V T p Vp T
V p T Vp
p
13 Un mol de gas real, a presiones moderadas, cumple con la ecuacin:
p (V b ) = RT
Donde R y b son constantes. Calcular el coeficiciente de compresibilidad isoterma y de
dilatacin cbica.
Solucin: Partiendo de las expresiones diferenciales de dichos coeficientes, derivando
determinaremos los mismos:
R
RT
1 V
R
1 V
RT
=
T =
= 2 T = 2
=
=
Vp
Vp
V T p Vp
V p T Vp
14 Hallar el volumen final de 200 g de agua que sufre una compresin isoterma a 0 C
desde 1 bar hasta 300 bar.
T = 0.50885 Gpas1
Datos: (0 C, 1 bar) = 999.84 kg/m3
Solucin: Sabiendo que:
1 V
dV
T =
= T dp ln V = T p + f (T )
V p T
V
Como es a temperatura constante, entonces f (T ) cte :
ln V = T p + k
Partiendo de los datos del problema, determinamos el volumen inicial ocupado por los
200 g de agua:
m
200
= 0.200032 L
Vi = =
999.84
Y conocido el volumen inicial, convirtiendo las presiones y el coeficiente de
compresibilidad a pascales, obtendremos el volumen final:
ln Vi = T pi + k
ln V f ln Vi = T ( p f pi ) V f = exp ln Vi T ( p f pi )
ln V f = T p f + k
V f = 0.197012 L
12
Julin Moreno Mestre
15 Una vasija contiene 8.450 g de agua a 0C y el resto de la misma se llena con parafina.
Cuando el agua se congela a 0C, se expulsan 0.620g de parafina. La densidad de la
parafina a 20C es 0.800 g/cm3 y su coeficiente de dilatacin 9.010-4K-1. Calclese la
densidad del hielo. Considrese la densidad del agua igual a 1g/cm3.
Solucin: Integramos la ecuacin diferencial del coeficiente de dilatacin lineal de la
parafina:
1 V
V
= T ln V = T + f ( p ) V (T ) = f ( p)e T
=
V T p
V
A partir de la expresin de la densidad:
m
m T
e
= =
V
f ( p)
pensemos que al ser un proceso isobrico entonces f (p) cte , y que la masa de la
parafina es tambin constante, por tanto la expresin de la densidad de la parafina es:
(T ) = ke T
Conociendo a 20 C = 293 K la densidad de la parafina, averiguamos el valor de la
constante k:
4 293
(293) = ke910
= 0.8 k = 1.041 kg/L
La densidad de la parafina a 273 K es:
(273) = 1.041e910
4 273
= 0.814 g/cm3
El volumen de parafina desalojado es:
m 0.620
V= =
= 0.763 cm3
0.814
La vasija a 0 C tena inicialmente agua lquida y parafina, pero a 0 C el agua se
congela y cambia su densidad cambiando por tanto su volumen, el volumen de parafina
expulsado de la vasija es equivalente a la ganancia de volumen del agua al convertirse
en hielo. Por tanto el volumen del hielo ser:
VH2O(s) = VH2O(l) + V = 8.450 + 0.763 = 9.212 cm3
Teniendo en cuenta que toda la masa de agua lquida se convierte en hielo, la densidad
del hielo es por tanto:
mH2O 8.450
H2O(s) =
=
= 0.917 g/cm3
VH2O(s) 9.212
13
Ejercicios y problemas de Termodinmica I
16 Un hilo metlico de 0.0085 cm2 de seccin, sometido a una fuerza de 20 N y a la
temperatura de 20 C, est situado entre dos soportes rgidos separados 1.2 m.
a) Cul es la fuerza recuperadora final si la temperatura se reduce a 8C?
b) Si adems de la anterior disminucin de temperatura los soportes se acercan
0.012 cm, cul ser la fuerza recuperadora final?
Supngase que en todo momento el hilo se mantiene rectilneo y que el coeficiente de
dilatacin lineal y el mdulo de Young isotermo tienen valores constantes e iguales a
1.510-5 K-1 y 21011 N/m2, respectivamente.
Solucin: A partir de las correspondientes relaciones diferenciales:
1 L
L F
L =
=
L T F
A L T
Procedemos a integrar las ecuaciones diferenciales:
1 L
L
L F
L F
L = L T =
=
=
L T F
L
A L T
L A
F
F
LT = ln L + g ( F )
ln L =
+ f (T ) f (T ) = ln L
A
A
Tras este proceso podemos distinguir la ecuacin de estado ms un trmino constante:
F
LT = ln L
+ cte
A
Con un valor inicial, determinamos el valor del trmino constante.
20
1.5105 293 = ln1.2
+ cte cte = 30227.1
0.85106 21011
Por tanto:
F
LT = ln L
0.177808
A
Ahora respondemos a los apartados del ejercicio:
a) Tenemos que calcular la fuerza cuando la temperatura es 8 C.
F
1.5105 281 = ln1.2
0.177808 F = 50.6 N
0.85106 21011
b) No solo la temperatura es de 8 C, sino que adems cambia la longitud:
F
1.5105 281 = ln(1.19988)
0.177808 F = 33.8 N
0.85106 21011
14
Julin Moreno Mestre
17 Los coeficientes trmicos de dilatacin isobrica y compresibilidad isoterma T de
cierto gas real vienen dados por las expresiones:
Rv 2 (v b)
v 2 (v b) 2
=
=
T
RTv 3 2a (v b) 2
RTv 3 2a (v b) 2
siendo a y b dos constantes caractersticas del gas y v el volumen molar.
a) Hllese la ecuacin de estado de dicho gas, teniendo en cuenta que para
volmenes molares altos el gas se comporta idealmente.
b) Qu volumen ocupar un mol de gas ideal a 300 K y 14 atm suponiendo que a
= 3.61 atmL2/mol2 y b = 0.0428 L/mol.
Solucin: a) Integramos el coeficiente de compresibilidad isoterma:
v 2 (v b ) 2
1 v
RTv 3 2a(v b) 2
p
=
T =
RTv 3 2a(v b) 2
v p T
v 3 (v b) 2
v T
RT
2a
RT
a
dp =
3 dv p =
+ 2 + f (T )
2
v
vb v
(v b)
Pero el coeficiente de dilatacin isobrica presenta dificultades:
Rv 2 (v b)
1 v
RTv 3 2a (v b) 2
T
=
=
=
RTv 3 2a (v b) 2 v T p
Rv 3 (v b)
v p
Hay problemas ya que no es una ecuacin de variables separadas, buscaremos con la
relaciones diferenciales un recurso que nos permita su integracin:
T p
1 RTv 3 2a (v b) 2 v b
T
p v b
=
3
v (v b)
vb
v p
v T R
p v v T R
T p
R
RT
p v b T v b
dp =
dT =
+ g (v )
=
=
R
vb
vb
v T R
p v v T
p v
Por tanto la funcin de estado es:
RT
a
p=
+ 2 +k
v b v
Segn las condiciones del problema, si el volumen molar es muy grande, entonces la
ecuacin de estado debe desembocar en la de un gas ideal, eso significa que:
RT
a
+ 2 + k v b v
p=
RT
RT
k =0
p=
+ k
p=
v b v
2
gas ideal
v
v
a / v 0
v grande
Por tanto la ecuacin de estado buscada es esta:
RT
a
p=
+ 2
v b v
b) Si n = 1 entonces v = V , por tanto la ecuacin de estado:
RT
a
p=
+ 2
V b V
Sustituyendo llegamos a la ecuacin (que desemboca en ecuacin de tercer grado):
0.082300 3.61
14 =
+
V = 1.65 L.
V 0.0428 V 2
Para resolver la ecuacin anterior necesitamos ayuda informtica o mtodos numricos.
15
Ejercicios y problemas de Termodinmica I
18 Los coeficientes de dilatacin cbica y de compresibilidad isoterma de cierta sustancia
vienen dados por:
3aT 3
b
=
T =
V
V
siendo a y b constantes. Determnese la ecuacin de estado que relaciona p, V y T.
Solucin: Procedemos a integrar las ecuaciones diferenciales de los coeficientes de
dilatacin cbica y de compresibilidad isoterma:
3aT 3 1 V
b
1 V
=
=
T = =
V
V T p
V
V p T
V
3aT 3 =
T p
V
b =
p T
bp = V
3aT 3T = V
3aT 4
= V + f ( p)
bp = V + g (T )
4
3aT 4
V = g (T ) bp
V=
+ f ( p)
4
Tras este proceso de integracin, es ahora fcil determinar la ecuacin de estado
resultante ms un trmino constante fruto del proceso de integracin:
3aT 4
V=
bp + cte
4
19 El coeficiente de dilatacin de un gas vale:
4T 3
T 4 4
donde es una constante, y el coeficiente de compresibilidad T = p 1 . Hallar la
ecuacin de estado del gas.
Solucin: Solucin: Procedemos a integrar las ecuaciones diferenciales de los
coeficientes de dilatacin cbica y de compresibilidad isoterma:
4T 3
1 V
1
1 V
= 4 4=
T = =
T
V T p
p
V p T
p
V
4T 3
V
=
T =
4
4
p
V
T
V
4
4
ln p = ln V + g (T )
ln(T ) = ln V + f ( p)
ln V = ln p + g (T )
ln V = ln(T 4 4 ) + f ( p)
Tras este proceso de integracin, es ahora fcil determinar la ecuacin de estado
resultante ms un trmino constante fruto del proceso de integracin:
ln V = ln(T 4 4 ) ln p + cte
Para simplificarla, reagrupamos los logaritmos en un lado de la igualdad y nos
valdremos de sus propiedades:
Vp
Vp
= cte
= cte 4
ln V ln(T 4 4 ) + ln p = cte ln 4
4
T 4
T
16
Julin Moreno Mestre
20 La ecuacin de estado de una sustancia elstica ideal es:
L L2
F = KT 20
L0 L
donde F es la fuerza recuperadora, K es una constante y L0 (valor de la longitud a
fuerza recuperadora nula) es funcin solo de la temperatura. Determnese:
a) El coeficiente de dilatacin lineal.
b) El mdulo de Young de la sustancia, as como el valor de este ltimo a fuerza
recuperadora nula.
Solucin: a) Transformamos la ecuacin de estado para facilitarnos la labor del clculo
del coeficiente de dilatacin lineal.
L L2
L3 L30
F = KT 20 = KT
FL0 L2 = KT ( L3 L30 )
2
L0 L
L0 L
Procedemos a derivar considerando F como constante:
L
L
3
3
2
FL0 L2 ) =
KT ( L3 L30 ) 2 FL0 L
(
= K ( L L0 ) + 3L KT
T
T
T F
T F
Y sabiendo que el coeficiente de dilatacin lineal es:
1 L
L =
L T F
lo sacaremos de la ecuacin:
1 L
1 L
3
3
3
2 FL0 L2
= K ( L L0 ) + 3L KT
L T F
L T F
2 FL0 L2 L = K ( L3 L30 ) + 3L3 KT L L L2 ( 2 FL0 3LKT ) = K ( L3 L30 )
L =
K ( L3 L30 )
2 FL0 L2 3L3 KT
Mediante la ecuacin de estado, eliminamos F:
L3 L30 )
K ( L3 L30 )
(
L =
L =
2TL30 L3T
L3 L30
2
3
L
L
L
KT
2 KT
3
2 0
L0 L
b) Derivamos la ecuacin inicial de nuestro problema:
2 L20 1
L F
L
= = KT 3 +
A L T A
L0
L
Y ahora para fuerza recuperadora nula L = L0:
2 L20 1
3KT
L0
= KT 3 + =
A
A
L0 L0
17
Ejercicios y problemas de Termodinmica I
21 El coeficiente de dilatacin trmica del mercurio a 273 K es 1.8104K1 . El
coeficiente de compresibilidad isotermo es 5.3106 bar1. Si una ampolla
completamente llena de mercurio, sellada y sin espacio vapor, se calienta desde 273 a
274 K, cul sera el aumento de presin desarrollado en el interior de la ampolla?
Solucin: Partiendo de las relaciones diferenciales de los coeficientes:
1 V
1 V
=
T =
V T p
V p T
Procedemos integrando a buscar la ecuacin de estado del mercurio:
1 V
V
1 V
V
=
T =
T p =
T =
V T p
V
V p T
V
ln V = T + f ( p)
ln V = T p + g (T )
Podemos deducir ahora la ecuacin de estado ms un trmino constante:
ln V = T T p + k
Para calcular el incremento de presin despejamos la presin en la ecuacin de estado:
k + T ln V
p=
El incremento de presin es:
k + T f ln V k + Ti ln V (T f Ti )
p = p f pi =
=
= 33.96 bar
22 Demuestre que la ecuacin:
p T V
= 1
V T p V T p
se cumple en un gas ideal y en un gas de Clausius de ecuacin p(V b) = RT .
Solucin: Sea la ecuacin de estado del gas ideal:
pV = nRT
Sean sus derivadas parciales de la ecuacin de arriba:
T
V
nR
nRT
p
V
= 2
V
p
V T
T p
p V nR
Por tanto, sustituyendo, simplificando y teniendo en cuenta la ecuacin del gas ideal:
nRT
nRT V nR
= 1
=
2
pV
V nR p
Demostrado
En el caso de la ecuacin de un gas de Clausius:
T
RT
V b
R
p
V
=
2
(V b)
R
V T
T p p
p V
Ahora sustituyendo, simplificando y considerando la ecuacin del gas de Clausius:
RT V b R
RT
= 1
=
2
p (V b)
(V b) R p
Demostrado.
18
Julin Moreno Mestre
23 Un metal, cuyos coeficientes de dilatacin cbica y de compresibilidad isotrmica son
5105 K1 y 1.21011 Pa1 respectivamente, est a una presin de 105 Pa y a una
temperatura de 20 C. Si se le recubre con una capa gruesa y muy ajustada de una
sustancia de dilatacin y compresibilidad despreciables:
a) Cul ser su presin final al elevar su temperatura hasta 32 C?
b) Cul es la mxima temperatura que puede alcanzar el sistema si la presin ms
alta que puede resistir la envoltura es 1.21018 Pa?
Solucin: Partiendo de las relaciones diferenciales de los coeficientes:
1 V
1 V
=
T =
V T p
V p T
Procedemos integrando a buscar la ecuacin de estado del mercurio:
1 V
V
1 V
V
=
T =
T p =
T =
V T p
V
V p T
V
ln V = T + f ( p)
ln V = T p + g (T )
Podemos deducir ahora la ecuacin de estado ms un trmino constante:
ln V = T T p + k
Al recubrirse de una capa gruesa que le impide dilatarse, esto supone que V es
constante y por tanto rescribimos la ecuacin de estado como:
k = T T p
Determinamos ahora el valor de la constante considerando los valores iniciales del
problema:
k = 5105 293 1.21011 105 = 1.465102
a) Su presin final al subir la temperatura hasta 32 C = 305 K ser:
1.465102 = 5105 305 1.21011 p p = 5.01107 Pas
b) La mxima temperatura que puede alcanzar el sistema con la presin ms alta
soportable ser:
1.465102 = 5105 T 1.210111.2108 T = 321.8 K
24 La constante dielctrica relativa del agua vara con la temperatura de la forma:
r = a bT
donde a y b son constantes. Sabiendo que:
P
e = = 0 ( r 1)
E T
Establecer una ecuacin de estado para el agua lquida sometida al campo elctrico.
Solucin: A partir de la ecuacin diferencial que cumple la susceptibilidad dielctrica:
P
e = = 0 ( r 1)
E T
Buscaremos integrando la ecuacin de estado que nos piden para el agua lquida:
P
= 0 (a bT 1) P = 0 (a bT 1)E P = 0 (a bT 1)E + cte
E T
Tengamos presente que si el campo es cero, entonces tambin es nula la polarizacin,
luego el trmino cte es nulo.
P = 0 (a bT 1)E + cte
19
Ejercicios y problemas de Termodinmica I
25 Un paramagntico ideal cumple la ley de Curie con la susceptibilidad dependiente solo
de la temperatura:
1 M
C
m =
=
V H T T
donde C es una constante. Suponiendo que se conoce su coeficiente de dilatacin, ,
que es una funcin exclusiva de la temperatura, determinar la influencia del campo
magntico sobre el coeficiente magnetotrmico que se define como:
M
T H
Solucin: Nos valdremos para obtener la relacin de las segundas derivadas parciales
cruzadas, y nos valdremos adems que el momento magntico del material M es una
variable de estado:
M M
V
( mV ) = m V + m
=
H T H
T H
H T H T T H T H T
M m
m
1
V + V m = V m
=
V + V m =
T
T
H T H T T H
Integramos una vez con respecto a H:
H
M
=
dH
H T H
0 V m T dH
T
Ningn elemento del integrando del segundo miembro depende del campo magntico,
luego:
1
M
M
=
+ V m
T
T H T H =0
20
Julin Moreno Mestre
21
You might also like
- Temperatura aproximada 363,35 KDocument5 pagesTemperatura aproximada 363,35 KJessenia CruzNo ratings yet
- Termodinámica gases ideales coeficiente expansiónDocument18 pagesTermodinámica gases ideales coeficiente expansiónJesús CubasNo ratings yet
- Termodinámica gases idealesDocument5 pagesTermodinámica gases idealesmonmoNo ratings yet
- Term o Metro GalileoDocument4 pagesTerm o Metro Galileogaminster69350% (1)
- Ejercicios Resueltos de Termodinamica PDFDocument113 pagesEjercicios Resueltos de Termodinamica PDFLeonardo Apaza PilcoNo ratings yet
- Cuestionario Primer ParcialDocument33 pagesCuestionario Primer ParcialJuan Silva LopezNo ratings yet
- Termodinámica: Equilibrio térmico gases ideales y termómetrosDocument1 pageTermodinámica: Equilibrio térmico gases ideales y termómetrosAlejandro AmadorNo ratings yet
- TermodinamicaDocument11 pagesTermodinamicaCamilo FernandezNo ratings yet
- Problemas de Termodinámica FundamentosDocument24 pagesProblemas de Termodinámica FundamentosSebastian Andres De Oro0% (1)
- Reporte de InvestigaciónDocument9 pagesReporte de InvestigaciónAby GeårNo ratings yet
- ResumenDocument6 pagesResumenJulioNo ratings yet
- Determinación de Funciones Termodinámicas de Reacción Por Medidas de F.E.M.Document7 pagesDeterminación de Funciones Termodinámicas de Reacción Por Medidas de F.E.M.Marcelo CumiaannNo ratings yet
- Equilibrio térmico de sistemas magnéticos y gases idealesDocument3 pagesEquilibrio térmico de sistemas magnéticos y gases idealesrios258No ratings yet
- Termo1 20BDocument6 pagesTermo1 20BJesus Saravia MendozaNo ratings yet
- TemodinámicaDocument12 pagesTemodinámicaMario Flores SalazarNo ratings yet
- FISICA Termodinamica PDFDocument18 pagesFISICA Termodinamica PDFfranco tiraNo ratings yet
- Problemas BuenossDocument10 pagesProblemas BuenossMoyCoral67% (6)
- CAPÍTULO VI Temperatura y DilatacionDocument11 pagesCAPÍTULO VI Temperatura y DilatacionMarco Antonio Escobedo AguilarNo ratings yet
- Determinación Del Calor de Vaporizacion de Un LíquidoDocument9 pagesDeterminación Del Calor de Vaporizacion de Un LíquidoCarlos David Ramos RosalesNo ratings yet
- Primera Ley de La TermodinámicaDocument6 pagesPrimera Ley de La Termodinámicamejora continuaNo ratings yet
- Introducción A La Termodinamica 2Document250 pagesIntroducción A La Termodinamica 2cualquieraquesea100% (1)
- Ejercicios de Aplicacion A La Ingenieria MecánicaDocument10 pagesEjercicios de Aplicacion A La Ingenieria Mecánicamarco sosaNo ratings yet
- Investigación I LuchoDocument10 pagesInvestigación I LuchoCarolina Velazquez EspinoNo ratings yet
- Método de Parámetros ConcentradosDocument7 pagesMétodo de Parámetros ConcentradosRaul RomeroNo ratings yet
- Paredes AdiabaticasDocument30 pagesParedes Adiabaticasingfrank89No ratings yet
- Plantas de conversión térmicaDocument80 pagesPlantas de conversión térmicaJuanPazNo ratings yet
- Tema 1 - IntroduccionDocument5 pagesTema 1 - IntroduccionMary Y Adán Navarro CabreraNo ratings yet
- Tema 9 TermodinámicaDocument20 pagesTema 9 TermodinámicaValentina SandonNo ratings yet
- Problemario Termo IPN Septiembre 2015Document35 pagesProblemario Termo IPN Septiembre 2015Carol Sán0% (1)
- Ejercicios Física AplicadaDocument6 pagesEjercicios Física AplicadaNATALIA ORTEGA GOMEZNo ratings yet
- Termodinámica - Gas Real.Document3 pagesTermodinámica - Gas Real.CARLOS ESTEBAN MORENO DUENASNo ratings yet
- Hoja 1Document2 pagesHoja 1Nicolás KozakNo ratings yet
- ENTALPÍA DE VAPORIZACION (Comp) PDFDocument13 pagesENTALPÍA DE VAPORIZACION (Comp) PDFIncodecsa PerusacNo ratings yet
- Informe de Gases PDFDocument7 pagesInforme de Gases PDFJuan LopezNo ratings yet
- TERMODINAMICA EJERCICIOSDocument5 pagesTERMODINAMICA EJERCICIOSAndrea VillaNo ratings yet
- 1 Parcial de Física Térmica y Mecánica EstadísticaDocument2 pages1 Parcial de Física Térmica y Mecánica EstadísticaJose GuerraNo ratings yet
- Entropia Gas RealDocument7 pagesEntropia Gas RealAldry SolizNo ratings yet
- Gas Ideal-PRINCIPIOSDocument2 pagesGas Ideal-PRINCIPIOSJEANET MAZA CCALLONo ratings yet
- Parametros Concentrados 1Document6 pagesParametros Concentrados 1Samuel Lepe80% (5)
- Termodinamica-Ejercicios Resueltos y TeoriaDocument63 pagesTermodinamica-Ejercicios Resueltos y TeoriaErick CaceresNo ratings yet
- Boletin 1 PDFDocument3 pagesBoletin 1 PDFKaedarNo ratings yet
- Tareaunica TermoDocument13 pagesTareaunica TermoGutierrez LopezNo ratings yet
- Termodinámica-Parte II: Leyes de los gases y procesos termodinámicosDocument17 pagesTermodinámica-Parte II: Leyes de los gases y procesos termodinámicosDenilson Chuquipoma SantosNo ratings yet
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSFrom EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSRating: 4.5 out of 5 stars4.5/5 (7)
- Ingeniería química. Soluciones a los problemas del tomo IFrom EverandIngeniería química. Soluciones a los problemas del tomo INo ratings yet
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesFrom EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesNo ratings yet
- Experiencias sobre circuitos eléctricos en serie operados por corriente directaFrom EverandExperiencias sobre circuitos eléctricos en serie operados por corriente directaNo ratings yet
- Curso básico de teoría de númerosFrom EverandCurso básico de teoría de númerosRating: 5 out of 5 stars5/5 (2)
- Problemas DinamicaDocument6 pagesProblemas Dinamicaushuaia7745No ratings yet
- ParábolasDocument1 pageParábolasushuaia7745No ratings yet
- Ecua Exp Con LogDocument1 pageEcua Exp Con Logushuaia7745No ratings yet
- Demostracion Suma Angulos TrianguloDocument1 pageDemostracion Suma Angulos Trianguloushuaia7745No ratings yet
- Test EsfericaDocument68 pagesTest Esfericaushuaia7745No ratings yet
- 2-Operaciones Con Vectores IDocument8 pages2-Operaciones Con Vectores Iushuaia7745No ratings yet
- Ecuaciones Logaritmicas Cambio VariableDocument1 pageEcuaciones Logaritmicas Cambio Variableushuaia7745No ratings yet
- Proporcionalidad Inversa - OdpDocument4 pagesProporcionalidad Inversa - Odpushuaia7745No ratings yet
- Proporcionalidad Inversa - OdpDocument4 pagesProporcionalidad Inversa - Odpushuaia7745No ratings yet
- Funcion ExponencialDocument2 pagesFuncion Exponencialushuaia7745No ratings yet
- Areas CompuestasDocument1 pageAreas Compuestasushuaia7745No ratings yet
- Problemas 1ºDocument1 pageProblemas 1ºushuaia7745No ratings yet
- La geometría analítica de Descartes y los vectores fijosDocument8 pagesLa geometría analítica de Descartes y los vectores fijosushuaia7745No ratings yet
- AngulosDocument4 pagesAngulosushuaia7745No ratings yet
- Sistemas No Linelaes EjerciciosDocument2 pagesSistemas No Linelaes Ejerciciosushuaia7745No ratings yet
- Nuestra Necesidad de Consuelo Es InsaciableDocument4 pagesNuestra Necesidad de Consuelo Es Insaciableushuaia7745No ratings yet
- Sistemas de Ecuaciones No LinealesDocument4 pagesSistemas de Ecuaciones No Linealesushuaia7745No ratings yet
- FuncionesDocument29 pagesFuncionesushuaia7745No ratings yet
- Sistemas de Ecuaciones No LinealesDocument4 pagesSistemas de Ecuaciones No Linealesushuaia7745No ratings yet
- Sistemas de Ecuaciones No Lineales PDFDocument1 pageSistemas de Ecuaciones No Lineales PDFushuaia7745No ratings yet
- ATestamento Tema 7Document10 pagesATestamento Tema 7Sherley MarlyNo ratings yet
- Comprension LectoraDocument3 pagesComprension Lectoraushuaia7745No ratings yet
- ATestamento Tema 4Document10 pagesATestamento Tema 4ushuaia7745No ratings yet
- Las Genealogias de GenesisDocument1 pageLas Genealogias de GenesisMarlon Menacho VelaNo ratings yet
- ATestamento Tema 6Document9 pagesATestamento Tema 6ushuaia7745No ratings yet
- ATestamento Tema 0 IntroduccionDocument1 pageATestamento Tema 0 Introduccionushuaia7745No ratings yet
- ATestamento Tema 8Document8 pagesATestamento Tema 8ushuaia7745No ratings yet
- ATestamento Tema 5Document9 pagesATestamento Tema 5ushuaia7745No ratings yet
- ATestamento Tema 3Document10 pagesATestamento Tema 3ushuaia7745No ratings yet
- AT Tema 1Document10 pagesAT Tema 1aledescargaNo ratings yet
- Los Mándalas Del ZodiacoDocument2 pagesLos Mándalas Del Zodiacoeatableattorney66No ratings yet
- Mapa PolíticoDocument3 pagesMapa PolíticoyohanaNo ratings yet
- Extintores PortatilesDocument37 pagesExtintores PortatilesCI Amilcar50% (4)
- Tipos de cimentación y sus característicasDocument11 pagesTipos de cimentación y sus característicasJunior Barcianovich DelgadovNo ratings yet
- Ecuaciones Diferenciales Ordinarias de Orden Superior y Sistemas de Ecuaciones Difereniales OrdinDocument13 pagesEcuaciones Diferenciales Ordinarias de Orden Superior y Sistemas de Ecuaciones Difereniales OrdinAnonymous EzFnUb4Q6UNo ratings yet
- Problemas de ElectromagnetismoDocument45 pagesProblemas de ElectromagnetismoJose Miguel Lopez DelgadoNo ratings yet
- Continuidad de Una FunciónDocument6 pagesContinuidad de Una FunciónVictor VillarruelNo ratings yet
- Resistencia de Materiales Ejercicios Virtuales 03Document7 pagesResistencia de Materiales Ejercicios Virtuales 03Juan Carlos LiñanNo ratings yet
- Ca Unimix (Es) F 1VCP000008-0903Document36 pagesCa Unimix (Es) F 1VCP000008-0903marcotorressimonNo ratings yet
- Tecnologías de Produccion MiSwacoDocument72 pagesTecnologías de Produccion MiSwacoJuan Heredia100% (1)
- Arg Masterflex2000Document2 pagesArg Masterflex2000Raul CabanillasNo ratings yet
- Unidad 2. Actividad 3. PendienteDocument4 pagesUnidad 2. Actividad 3. PendienteJudith RoldánNo ratings yet
- Homomorfismos de gruposDocument8 pagesHomomorfismos de gruposOlga Antonia OrtizNo ratings yet
- Determinación de acetilsalicilato y cafeína en cafiaspirina por CLDocument4 pagesDeterminación de acetilsalicilato y cafeína en cafiaspirina por CLClau VargasNo ratings yet
- PlanetasDocument3 pagesPlanetasJFernando TorresNo ratings yet
- Análisis Del Flujo de Cargas en Redes de Baja TensiónDocument15 pagesAnálisis Del Flujo de Cargas en Redes de Baja Tensióneduarzn9081No ratings yet
- G01 - Informe FinalDocument27 pagesG01 - Informe FinalMARLON BRUNONo ratings yet
- Diseño en Climas Cálidos - Alan KonyaDocument147 pagesDiseño en Climas Cálidos - Alan KonyaGonzalo Acosta MijaresNo ratings yet
- Guia 1 Electrostatica 1 v2Document6 pagesGuia 1 Electrostatica 1 v2Luis VillarNo ratings yet
- Subestacion AndahuasiDocument14 pagesSubestacion AndahuasiEvelyn Chacon BorjaNo ratings yet
- Informe Final 3 de Circuitos Electronicos 1 PDFDocument32 pagesInforme Final 3 de Circuitos Electronicos 1 PDFJhon Alex López SotoNo ratings yet
- Método de LowryDocument6 pagesMétodo de LowryGutslutNo ratings yet
- Eliminación Del Biofouling en Intercambiadores de Calor-Condensadores Que Minimicen El Impacto Ambiental en El Medio MarinoDocument742 pagesEliminación Del Biofouling en Intercambiadores de Calor-Condensadores Que Minimicen El Impacto Ambiental en El Medio MarinoYesenia Rojas Lillo0% (1)
- 3-6-19 1er Parcial - Metodologia AnalisisDocument15 pages3-6-19 1er Parcial - Metodologia AnalisisDariana OsuchNo ratings yet
- La Trabajabilidad de Una Mezcla de Mortero Tiene Que Ver ConDocument4 pagesLa Trabajabilidad de Una Mezcla de Mortero Tiene Que Ver ConrudyuyyyyyNo ratings yet
- Instalación Eléctrica DomiciliariaDocument8 pagesInstalación Eléctrica Domiciliariayulieth159No ratings yet
- Flexion AsimetricaDocument14 pagesFlexion AsimetricaJuan Rodriguez100% (4)
- Dibujo TecnicoDocument8 pagesDibujo TecnicoodlawsozepolNo ratings yet
- Características de Los PalpadoresDocument7 pagesCaracterísticas de Los PalpadoresNani SierraNo ratings yet
- Ficha Acido FosforicoDocument2 pagesFicha Acido FosforicoÁlvaro Olórtegui IglesiasNo ratings yet