Professional Documents
Culture Documents
Atomos y Enlaces
Uploaded by
María RJOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Atomos y Enlaces
Uploaded by
María RJCopyright:
Available Formats
FSICA Y QUMICA 1 BACH.
IES. Ruiz Gijn
UTRERA
ESTRUCTURA ATMICA. ENLACE QUMICO
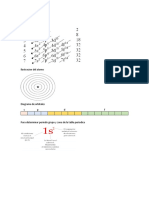
1.-/ Indique el n de protones, neutrones y electrones de los siguientes tomos e iones:
a) Ar (Z = 18, A = 40)
b) 12753I
c) S2 (Z = 16, A = 32)
d) 8838 Sr2+
e) Cl (Z = 17, A = 35)
f) Fe3+ (Z = 26, A = 56)
+
g) Ag (Z = 47, A = 108)
h) Au (Z = 79, A = 197)
i) Cu2+ (Z = 29, A = 64)
Sol:
a) 18 p, 22 n, 18 e. b) 53 p, 74 n, 53 e. c) 16 p, 16 n, 18 e. d) 38 p, 50 n, 36 e.
e) 17 p, 18 n, 18 e. f) 26 p, 30 n, 23 e. g) 47 p, 61 n, 46 e. h) 79 p, 118 n, 79 e.
i) 29 p, 35 n, 27 e.
2.-/ Un ion de un elemento
neutrones que contiene:
Sol: 3+ ; 14 n.
27
13X
contiene 10 electrones. Indique la carga del ion y el nmero de
3.-/ Sabiendo que el ion trivalente positivo de un tomo contiene 24 protones y 28 neutrones, indique
sus nmeros msico y atmico, as como los electrones que presenta.
Sol: A = 52 ; Z = 24 ; 21 e.
4.-/ Un ion divalente negativo de un tomo contiene 16 protones y 16 neutrones. Indique sus nmeros
atmico y msico, as como los electrones que contiene.
Sol: A = 32 ; Z = 16 ; 18 e.
5.-/ El plomo presenta cuatro istopos de masas y abundancias respectivas: 204 y 2 %; 207 y 28,2 %;
208 y 57,8 %; 209 y 12 %. Calcule la masa atmica de este elemento.
Sol: Ma = 207,76 uma.
6.-/ El Mg est formado en la naturaleza por tres istopos de masas 23,98 uma, 24,99 uma y 25,98
una. La abundancia relativa de cada uno de ellos es 78,60 %, 10,11 % y 11,29 %. Determine la masa
atmica del magnesio.
Sol: Ma = 24,31 uma.
7.-/ Escriba la configuracin electrnica de los siguientes tomos e iones:
a) Al (Z = 13)
b) Al3+
c) Ca (Z = 20)
d) Br (Z = 35)
e) Fe (Z = 26)
f) Fe3+
g) Ag (Z = 47)
h) S2 (Z = 16)
Sol:
a) 1s2 2s22p6 3s23p1 b)1s2 2s22p6 c) 1s2 2s22p6 3s23p6 4s2
d) 1s2 2s22p6 3s23p63d10 4s24p6
e) 1s2 2s22p6 3s23p63d6 4s2
f) 1s2 2s22p6 3s23p63d5
2
2
6
2
6
10
2
6
9
2
2
2
6
2
6
g) 1s 2s 2p 3s 3p 3d 4s 4p 4d 5s
h) 1s 2s 2p 3s 3p
8.-/ Escriba las configuraciones electrnicas, en su estado fundamental, de los tomos de Azufre y
Bario.
Sol:
S: 1s2 2s22p6 3s23p4 Ba: 1s2 2s22p6 3s23p63d10 4s24p64d10 5s25p6 6s2
9.-/ Si un tomo en su estado fundamental tiene ocupado totalmente el nivel n = 3, cuntos
electrones contiene?.
Sol: 30.
10.-/ Escriba la configuracin electrnica de los siguientes tomos e iones, sin mirar su n atmico:
a) Na
b) O
c) Cl
d) Ca2+
3+
g) Ar
h) Rb+
e) Cl
f) Al
Sol:
a) 1s2 2s22p6 3s1
b)1s2 2s22p4 c) 1s2 2s22p6 3s23p5 d) 1s2 2s22p6 3s23p6
2
2
6
2
6
e) 1s 2s 2p 3s 3p
f) 1s2 2s22p6 g) 1s2 2s22p6 3s23p6 h) 1s2 2s22p6 3s23p63d10 4s24p6
Estructura atmica. Enlace qumico
IES. Ruiz Gijn
FSICA Y QUMICA 1 BACH.
UTRERA
11.-/ Identifica grupo, periodo y elemento, correspondientes a las siguientes configuraciones
electrnicas:
b) 1s2 2s22p6 3s23p4
c) 1s2 2s22p6 3s23p6 4s1
a) 1s2 2s22p3
2
2
6
2
2
6
2
6
2
d) 1s 2s 2p
e) 1s 2s 2p 3s 3p 4s
f) 1s2 2s22p6 3s23p63d10 4s24p5
Sol:
a) P=2; Gr=15; N
b) P=3; Gr=16; S
c) P=4; Gr=1; K
d) P=2; Gr=18; Ne
e) P=4; Gr=2; Ca
f) P=4; Gr=17; Br
12.-/ Indica los iones ms estables y sus configuraciones electrnicas de los elementos:
a) Al
b) O
c) K
d) Mg
e) Br
Sol:
a) Al3+: 1s2 2s22p6
b) O2: 1s2 2s22p6
c) K+: 1s2 2s22p6 3s23p6 d) Mg2+: 1s2 2s22p6
e) Br: 1s2 2s22p6 3s23p63d10 4s24p6
13.-/ De las siguientes configuraciones electrnicas, diga cules son posibles y cules pertenecen a
estados fundamentales o estados excitados de un tomo e identifique a los tomos correspondientes:
a) 1s2 1p62p3
b) 1s2 2s22p6 3s23p4 4s1
c) 1s2 2s22p62d10 3s23p63d10 4s24p6
d) 1s2 2s22p6 3s23p6
Sol:
a) y c) no son posibles. b) Es un estado excitado del cloro. d) Estado fundamental del argn.
14.-/ Identifica el periodo, el nombre del grupo y los elementos correspondientes a las siguientes
configuraciones electrnicas:
a) 1s2 2s22p5
b) 1s2 2s1
c) 1s2 2s22p6 3s23p4
e) 1s2 2s22p6 3s23p63d10 4s24p6
d) 1s2 2s22p6 3s1
Sol:
a) P=2; Gr= halgenos; F
b) P=2; Gr= alcalinos; Li
c) P=3; Gr= anfgenos; S
d) P=3; Gr= alcalinos; Na
e) P=4; Gr= gases nobles; Kr
15.-/ Un tomo A tiene como configuracin electrnica: 1s2 2s22p6 3s23p6 5s1. Justifique la veracidad
o falsedad de las siguientes afirmaciones:
a) El elemento A se encuentra en su estado fundamental.
b) Pertenece al grupo de los metales alcalinos.
c) Est en el quinto periodo del sistema peridico.
d) Formar, preferentemente, compuestos con enlace covalente.
e) El ion ms estable que podr formar ser A+.
Sol:
a) Falsa
b) Verdadera
c) Falsa
d) Falsa
e) Verdadera
16.-/ Dados los elementos y compuestos: KCl; CO2; NaF; Ag; Cl2; MgCl2; SO2; Cu; CaF2; Fe.
a) Indique el tipo de enlace en cada uno de ellos.
b) Justifique los que sern ms solubles en agua y cules conducen la corriente elctrica a
temperatura ambiente.
Sol:
a) Inico: KCl, NaF, MgCl2, CaF2. Covalente: CO2, Cl2, SO2. Metlico: Ag, Cu, Fe.
b) Solubles en agua: Los compuestos inicos. Conductores: Los de enlace metlico y los inicos
disueltos en agua.
17.-/ Escriba las estructuras de Lewis de los compuestos: F2, N2, H2O, NH3, O2, CH4, Cl2, CO2 y CCl4.
18.-/ Dados los elementos e iones A (Z = 17), B (Z =19), C (Z= 18), D2+ (Z = 20) y E2 (Z = 8). Escriba
sus configuraciones electrnicas e indique el grupo, periodo y elemento al que pertenecen.
Sol:
A: 1s2 2s22p6 3s23p5; Gr= Halgenos (17); P= 3; Cloro (Cl).
B: 1s2 2s22p6 3s23p6 4s1; Gr= Alcalinos (1); P= 4; Potasio (K).
C: 1s2 2s22p6 3s23p6; Gr= Gases nobles (18); P= 3; Argn (Ar).
D2+: 1s2 2s22p6 3s23p6; Gr= Alcalinotrreos (2); P= 4; Calcio (Ca).
E2: 1s2 2s22p6; Gr= Anfgenos (16); P= 2; Oxgeno (O).
Estructura atmica. Enlace qumico
IES. Ruiz Gijn
FSICA Y QUMICA 1 BACH.
UTRERA
19.-/ Explique brevemente el enlace por puentes de hidrgeno.
20.-/ Justifique la existencia de los siguientes iones: Na+, Mg2+, Cl, O2, P3 y Zn2+.
Sol:
Hacer la configuracin electrnica y ver la prdida o ganancia de electrones para obtener la
configuracin de gas noble.
Ejercicios del Libro de Texto:
Antiguo
Nuevo
Pg. 56: 8, 14.
Pg. 57: 23, 31.
Pg. 65: 4, 15.
Pg. 57: 18, 21.
Estructura atmica. Enlace qumico
You might also like
- Guía de Aprendizaje 2 - Números CuánticosDocument4 pagesGuía de Aprendizaje 2 - Números CuánticosKAREN JULIETH VASQUEZ LOPEZNo ratings yet
- Química Básica Numeros Cuanticos PDFDocument69 pagesQuímica Básica Numeros Cuanticos PDFJOHANNo ratings yet
- Ejercicios de La Masa MolecularDocument3 pagesEjercicios de La Masa MolecularjuliaNo ratings yet
- Los Dos EscarabajosDocument5 pagesLos Dos Escarabajosmelgarromulo100% (1)
- Distribucion Electronica Colombia AprendeDocument8 pagesDistribucion Electronica Colombia AprendeMarcela Reyes Guio0% (1)
- Estructura Atómica IIDocument6 pagesEstructura Atómica IIayikan120% (1)
- Configuracion ElectronicaDocument15 pagesConfiguracion ElectronicaFatima VillarNo ratings yet
- Ejercicios Didacticos: Configuración ElectrónicaDocument5 pagesEjercicios Didacticos: Configuración ElectrónicaLuis Alberto Verano MatosNo ratings yet
- QuimizaDocument2 pagesQuimizaDavid Flores100% (1)
- Lectura Cientifi Sexto PasteurDocument2 pagesLectura Cientifi Sexto PasteurMarcela VargasNo ratings yet
- Ejercicios Ampliacion Quimica San JoseDocument4 pagesEjercicios Ampliacion Quimica San JoseManu CorteceroNo ratings yet
- SEMINARIO. Ondas y MASDocument4 pagesSEMINARIO. Ondas y MASPianistasenderistaNo ratings yet
- Taller Del Mio CidDocument3 pagesTaller Del Mio CidYoel Andres SalinaNo ratings yet
- Evaluacion Presion 11Document1 pageEvaluacion Presion 11Lina M HernándezNo ratings yet
- Configuracion Electronica PDFDocument2 pagesConfiguracion Electronica PDFAlexandra ChavarroNo ratings yet
- Ejercicios de Propiedades PeriodicasDocument2 pagesEjercicios de Propiedades PeriodicasYarara YararaNo ratings yet
- Taller de Estructura Atomica y Tabla PeriodicaDocument1 pageTaller de Estructura Atomica y Tabla PeriodicaCHARLIE DANIEL AMAYA RODRIGUEZNo ratings yet
- NÚMEROS CUÁNTICOS PrácticaDocument3 pagesNÚMEROS CUÁNTICOS PrácticaDenis Eduardo Paredes AquimaNo ratings yet
- El Senor Don Sodio y Dona CloroDocument3 pagesEl Senor Don Sodio y Dona CloroJAIDER SANTIAGO MEDINA TIQUENo ratings yet
- Tarea Tabla PeriodicaDocument4 pagesTarea Tabla PeriodicaCristian Flores SaicoNo ratings yet
- Quimica Segundo Grado 10 DesarolladaDocument6 pagesQuimica Segundo Grado 10 DesarolladaAdriana CastroNo ratings yet
- Solucionario de La Domiciliaria Del Ciclo Semestral UNIDocument30 pagesSolucionario de La Domiciliaria Del Ciclo Semestral UNIusuariosichNo ratings yet
- Atmomos PDFDocument2 pagesAtmomos PDFVianis AriasNo ratings yet
- 03 Sistema Periodico SolucionarioDocument10 pages03 Sistema Periodico SolucionarioCristina FernandezNo ratings yet
- U1 - S1 - Ficha de Trabajo 1-Estructura Del Átomo y Tabla PeriódicaDocument2 pagesU1 - S1 - Ficha de Trabajo 1-Estructura Del Átomo y Tabla PeriódicaMartha MezarinoNo ratings yet
- Trabajo Práctico Números CuánticosDocument3 pagesTrabajo Práctico Números CuánticosGuillermo Juri100% (1)
- Guia para Ficha AbrilDocument4 pagesGuia para Ficha AbrilJair A. ChauxNo ratings yet
- Ejercicios para Proyectar 2Document2 pagesEjercicios para Proyectar 2Rosario Pilar100% (1)
- Guia de Quimica # 2 Septimo GradoDocument10 pagesGuia de Quimica # 2 Septimo GradoLINDA CANTILLONo ratings yet
- Rut Ips DarienDocument5 pagesRut Ips DarienSebastianGutierrezHernandezNo ratings yet
- 5 Configuración Electrónica QUIMICA TERCERODocument5 pages5 Configuración Electrónica QUIMICA TERCEROluisandersonsotodava100% (2)
- Taller Estados de OxidaciónDocument2 pagesTaller Estados de OxidaciónIngri BaronNo ratings yet
- Evaluacion de QuimicaDocument4 pagesEvaluacion de Quimicamprm2579No ratings yet
- Taller Configuración ElectrónicaDocument2 pagesTaller Configuración ElectrónicaCB Hank100% (1)
- Evaluacion Bimestral 7° Matematicas Ii Periodo 2021Document5 pagesEvaluacion Bimestral 7° Matematicas Ii Periodo 2021Diana Carolina Ramirez LancherosNo ratings yet
- Configuracion Electronica Con KernellDocument2 pagesConfiguracion Electronica Con KernellJ Piero Tito AñañosNo ratings yet
- Números Cuanticos y Configuración Electrónica PDVDocument15 pagesNúmeros Cuanticos y Configuración Electrónica PDVPaula Astudillo VegaNo ratings yet
- Taller Tabla PeriódicaDocument4 pagesTaller Tabla PeriódicaJuanEstebanMora100% (1)
- Ejercicios-Configuracion ElectronicaDocument5 pagesEjercicios-Configuracion Electronicaomar aro criollo fabrisio100% (1)
- 4 Enlace Químico 4Document21 pages4 Enlace Químico 4Vyvi CsiNo ratings yet
- Taller Propiedades Periodicas (2) CorrepcDocument7 pagesTaller Propiedades Periodicas (2) CorrepcSergio Hernandez100% (1)
- Evaluacion Atomo 1Document5 pagesEvaluacion Atomo 1imatesmariaNo ratings yet
- ) ) Guia Didactica de Aprendizaje # 2 Naturales Séptimo 2021Document16 pages) ) Guia Didactica de Aprendizaje # 2 Naturales Séptimo 2021Laura AvilitaNo ratings yet
- Guia de Aprendizaje 1. Soluciones QuimicasDocument6 pagesGuia de Aprendizaje 1. Soluciones QuimicasPEUBEPE JAJAJANo ratings yet
- Formas de Los Orbitales Atómicos HibridaciónDocument12 pagesFormas de Los Orbitales Atómicos HibridaciónJaqueline Lopez RuizNo ratings yet
- Trabajo Práctico 1 Sexto ADocument3 pagesTrabajo Práctico 1 Sexto Aarmando paredesNo ratings yet
- Quimica Segunda Parte ContinuacionDocument3 pagesQuimica Segunda Parte Continuacionwilliam LibreNo ratings yet
- Quimica 6° Julio PDFDocument4 pagesQuimica 6° Julio PDFHaydee Yamile Cobos ForeroNo ratings yet
- Competencias Específicas Del ÁreaDocument4 pagesCompetencias Específicas Del Áreaanibal ariasNo ratings yet
- Guia y Taller de Grado 9 PDFDocument3 pagesGuia y Taller de Grado 9 PDFdavid gonzales100% (2)
- Tema: Configuracion Electronica GRADO: 7°1 Taller en ClaseDocument2 pagesTema: Configuracion Electronica GRADO: 7°1 Taller en ClaseLiyiPaternina0% (1)
- Guía Nº5 Enlace QuimicoDocument2 pagesGuía Nº5 Enlace QuimicoA01312078No ratings yet
- PRÁCTICA N 10 Reacciones RedoxDocument8 pagesPRÁCTICA N 10 Reacciones RedoxDiego Melendez ParedesNo ratings yet
- Solucionario Fe U04Document2 pagesSolucionario Fe U04diego pelusaNo ratings yet
- Guia Relaciones Seres VivosDocument10 pagesGuia Relaciones Seres Vivosdaniela reyesNo ratings yet
- La Pila (Laboratorio)Document13 pagesLa Pila (Laboratorio)Juan Carlos LazaroNo ratings yet
- Guía de Mareas y Corrientes MarinasDocument6 pagesGuía de Mareas y Corrientes MarinasPaola Andrea Hernández PradenasNo ratings yet
- Tabla de ValenciasDocument1 pageTabla de ValenciasjuanNo ratings yet
- Ejer Cici Osato Moyen LaceDocument3 pagesEjer Cici Osato Moyen Laceanon_161932416No ratings yet
- Taller de QuímicaDocument6 pagesTaller de QuímicaOscar Augusto SanchezNo ratings yet
- Manual Sintaxis 1c2ba Bachillerato PDFDocument22 pagesManual Sintaxis 1c2ba Bachillerato PDFMaría RJNo ratings yet
- Ud4. Los ViverosDocument41 pagesUd4. Los ViverosMaría RJNo ratings yet
- Directrices Cronicas ComentarioDocument1 pageDirectrices Cronicas ComentarioMaría RJNo ratings yet
- Relacion PlatónDocument1 pageRelacion PlatónMaría RJNo ratings yet
- Gramatica Primaria CuadernilloDocument36 pagesGramatica Primaria CuadernilloFrank SA CespedesNo ratings yet
- UD.6.Reproducc AsexualDocument49 pagesUD.6.Reproducc AsexualMaría RJNo ratings yet
- Introducción El Antiguo Régimen Historia de EspañaDocument2 pagesIntroducción El Antiguo Régimen Historia de EspañaMaría RJNo ratings yet
- U 7 FuntetoDocument18 pagesU 7 FuntetoomarNo ratings yet
- Exámenes 2º Eso Matematicas - BuenosDocument20 pagesExámenes 2º Eso Matematicas - BuenosMeryGrassMancheñoDíazNo ratings yet
- POLINOMIOSDocument5 pagesPOLINOMIOSitianaraNo ratings yet
- Examen de Nietzsche Tipo SelectividadDocument9 pagesExamen de Nietzsche Tipo Selectividadalexpliego97No ratings yet
- FICHASDocument1 pageFICHASMaría RJNo ratings yet
- Ejercicios de Tri Ngulos 4 Eso Curso 2010 2011 Soluciones1322136923461Document3 pagesEjercicios de Tri Ngulos 4 Eso Curso 2010 2011 Soluciones1322136923461JuanDavidAbelinoPatiñoTrasladinoNo ratings yet
- La Novela 2º BachDocument2 pagesLa Novela 2º BachMaría RJNo ratings yet
- Dos Textos Talento MR Ripley y Recursos para ComentarioDocument4 pagesDos Textos Talento MR Ripley y Recursos para ComentarioMaría RJNo ratings yet
- Manual de HorticulturaDocument58 pagesManual de HorticulturaTheGoldstein AttackNo ratings yet
- Conceptos EnpDocument4 pagesConceptos EnpMaría RJNo ratings yet
- Dos Textos Talento MR Ripley y Recursos para ComentarioDocument4 pagesDos Textos Talento MR Ripley y Recursos para ComentarioMaría RJNo ratings yet
- La Lirica Desde Los Años 70 A Nuestros DiasDocument2 pagesLa Lirica Desde Los Años 70 A Nuestros DiasMaría RJNo ratings yet
- La Segunda República y La Guerra CivilDocument7 pagesLa Segunda República y La Guerra CivilMaría RJNo ratings yet
- Geografia 2Document6 pagesGeografia 2María RJNo ratings yet
- Orientaciones A Los Profesores - Padres Del Lenguaje OralDocument2 pagesOrientaciones A Los Profesores - Padres Del Lenguaje OralMaría RJNo ratings yet
- EnunciadosDocument2 pagesEnunciadosMaría RJNo ratings yet
- Ejercicios Resueltos Economía 1º - Tema 2Document9 pagesEjercicios Resueltos Economía 1º - Tema 2luigocu93% (88)
- TEMA 8 La Restauracion 2 BachDocument7 pagesTEMA 8 La Restauracion 2 BachMaría RJNo ratings yet
- Informe Ceuta 2009Document8 pagesInforme Ceuta 2009María RJNo ratings yet
- Raices CuadradasDocument15 pagesRaices CuadradasMaría RJNo ratings yet
- Relación Platón Con AristótelesDocument1 pageRelación Platón Con AristótelesMaría RJNo ratings yet
- El Renacimiento en EspañaDocument6 pagesEl Renacimiento en EspañaMaría RJNo ratings yet
- Introducción El Antiguo Régimen Historia de EspañaDocument2 pagesIntroducción El Antiguo Régimen Historia de EspañaMaría RJNo ratings yet
- Laboratorio 4 de Sistemas de Comunicación Digital IDocument8 pagesLaboratorio 4 de Sistemas de Comunicación Digital IAndrésEduardoMartinezNo ratings yet
- Sistemas DistribuidosDocument47 pagesSistemas Distribuidoskiejic67% (3)
- Pea Electricista Industrial 5Document4 pagesPea Electricista Industrial 5GRACE NICOLE AQUINO LAZONo ratings yet
- Ejercicios Propuesto TransistoresDocument18 pagesEjercicios Propuesto TransistoresWalter Eliecer UmañaNo ratings yet
- EcualizadoresDocument10 pagesEcualizadoresDavid PeñalveNo ratings yet
- Como Trabaja Un Transpondedor LinealDocument7 pagesComo Trabaja Un Transpondedor LinealfaridvbNo ratings yet
- Acoplamiento de AmplificadoresDocument2 pagesAcoplamiento de AmplificadoresVitore Morleone82% (11)
- Examenes Segundo ParcialDocument10 pagesExamenes Segundo ParcialLenny RayssaNo ratings yet
- Tareas Info 310Document56 pagesTareas Info 310Otacilio Antonio CastilloNo ratings yet
- 1 - Acti9 - INTERRUPTOR DIFERENCIAL, iID, iIDsi PDFDocument7 pages1 - Acti9 - INTERRUPTOR DIFERENCIAL, iID, iIDsi PDFjhonnyNo ratings yet
- Informe 2Document8 pagesInforme 2Fercho Rojas RamosNo ratings yet
- Lab2p2 PDFDocument2 pagesLab2p2 PDFJorge Luis RodriguezNo ratings yet
- Efecto FaradayDocument8 pagesEfecto FaradayFanny MéndezNo ratings yet
- Laboratorio 1 MaterialesDocument15 pagesLaboratorio 1 MaterialesGiordano Carbajal BlasNo ratings yet
- Modelo Atómico de Rutherford y BohrDocument15 pagesModelo Atómico de Rutherford y BohrCarmen Pinto MarambioNo ratings yet
- 2 EL DIODO 2022 ModDocument4 pages2 EL DIODO 2022 ModJavier ChoqueNo ratings yet
- Lab 4Document8 pagesLab 4Franklin Daniel Carbajal OsisNo ratings yet
- En Torno Al VideoDocument15 pagesEn Torno Al VideoJuan José Wally Artista VisualNo ratings yet
- PDH EquiposDocument25 pagesPDH EquiposHugo G. RuedaNo ratings yet
- Tema 7 Automatismos CableadosDocument191 pagesTema 7 Automatismos CableadoshoasdNo ratings yet
- Activar 58 (Hojas Tecnicas) PDFDocument35 pagesActivar 58 (Hojas Tecnicas) PDFAntony Cervantes CervantesNo ratings yet
- Acoplo y Adaptacion de Impedancias.Document3 pagesAcoplo y Adaptacion de Impedancias.Alejandro VillcaNo ratings yet
- Informe Instalaciones Eléctricas EdificioDocument5 pagesInforme Instalaciones Eléctricas EdificioHenrry LingNo ratings yet
- Certif Med-Val-Ev LeqA de TV PDFDocument2 pagesCertif Med-Val-Ev LeqA de TV PDFpepemartillo591No ratings yet
- Reguladores de Voltaje Lineales ICDocument4 pagesReguladores de Voltaje Lineales ICcarlosNo ratings yet
- Motores GráficoDocument4 pagesMotores GráficonatalyNo ratings yet
- Arrancador Con Resistores PrimariosDocument8 pagesArrancador Con Resistores PrimariosfermrtechNo ratings yet
- Informe Pasantías Francisco RapettiDocument4 pagesInforme Pasantías Francisco RapettiFrancisco RapettiNo ratings yet
- Simulación Del Diodo Semiconductor PDFDocument7 pagesSimulación Del Diodo Semiconductor PDFMateo CabreraNo ratings yet
- 2 Diodos y RectificadoresDocument11 pages2 Diodos y RectificadoresEmmanuel OsunaNo ratings yet