Professional Documents
Culture Documents
Analisis Quimico Terminado
Uploaded by
Jesus GuerraCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Analisis Quimico Terminado
Uploaded by
Jesus GuerraCopyright:
Available Formats
DETERMINACION GRAVIMETRICA DEL HIERRO
JESUS GUERRA, ADRES OSORIO, JHOSEP CORREA
UNIVERSIDAD DE SUCRE
FACULTAD DE EDUCACIN Y CIENCIA
BIOLOGA IL SEMESTRE
INTRODUCCION
El hierro contenido en una muestra
puede analizarse precipitndolo como
xido hidratado (color pardo-rojizo;
Kps= 4x10-38), a partir de una
disolucin bsica.
El precipitado formado se calcina
despus para producir Fe2O3 . La
precipitacin comienza alrededor
de pH =2. El xido hidratado es gelati
noso, posee carcter bsico dbil y
puede tener impurezas ocluidas, por
la gran superficie que presenta.
Cuando se sospecha la presencia de
impurezas, el precipitado inicial se
disuelve en cido y se vuelve a
precipitar. As, la contaminacin por
oclusin disminuye.
En la gravimetra por precipitacin, el
analito se precipita como un
compuesto poco soluble, luego se
filtra, despus se lava para eliminar
impurezas, continuamente se lleva a
un compuesto de formula conocida
por medio de un calentamiento
adecuado y por ltimo se pesa. Se
puede separar en dos pasos que
seran la formacin del precipitado y
la calcinacin.
OBJETIVOS
Familiarizar al estudiante con
los pasos en un proceso de
anlisis cuantitativo
gravimtrico.
Determinar gravimtricamente
el contenido de hierro en una
muestra problema, y expresar
el resultado como %P/V de
Fe(N03)3. 9H2O
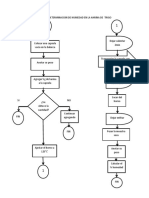
MATERIALES Y METODOS
Se pes el crisol
Se tom 25 ml de la solucin
problema ( FeSO4 x 7H2O)
Se aforo en un matraz de 100
ml
Se tom 25 ml de solucin
anterior en un beacker de 250
ml
Se aadi un ml de HNO3 y se
hirvi por 10 min
Se aadi ml de H2O destilada
y se dej reposar hasta que
llegara a Temperatura
ambiente
Se le agrego a la solucin
anterior una sln de NH3
Se llev a ebullicin durante 5
min
Se filtr el precipitado y se
enjuago con agua caliente
Se dobl el papel filtro, se
coloc en el crisol y se calcino
entre 550 y 560
se dej enfriar en el desecador
y se pes y el crisol
RESULTADO Y
DISCUSIONES
Cuando se agreg NH4OH
lentamente y se observ que la
disolucin formaba dos capas,
esto debido a que el hidrxido
de hierro (III) es muy insoluble
(Kps del orden de 10-37) y se
precipita de forma cuantitativa
aun a pH 4.
El ion amonio formado en la
precipitacin
tiende
a
desplazar
a
los
dems
cationes de la capa contra-ion
El xido hidratado de hierro es un
precipitado gelatinoso muy insoluble
en agua. La coagulacin del material
coloidal se favorece realizando la
precipitacin a partir de la solucin
caliente. La filtracin se realizo
utilizando un papel de filtracin
porosa. El precipitado se calcino en el
laboratorio y el papel se quemo a una
temperatura de 550C para remover
totalmente el agua.
CONCLUSIONES
Se aprendi mas sobre los procesos
de anlisis cuantitativos
gravimtricos, gracias a los
instrumentos que nos brinda el
laboratorio, por esto, aprendimos y
pudimos realizar esta prctica de
forma rpida y sin problemas.
Se logro determinar el contenido
gravimtrico del hierro gracias a los
conocimientos que obtuvimos en las
clases tericas, los cuales nos
facilitaron el desarrollo de esta
prctica de laboratorio.
* En la prctica se podr determinar
el porcentaje de Fe2O3 en la
muestra gracias a los mtodos
gravimtricos.
BIBLIOGRAFIA
* Orozco, F.: anlisis qumico
cuantitativo. Porra, Mxico, 1982. P.
100-102
* Ramete, R.: Equilibrio y Anlisis
Qumico, Fondo Educativo
Interamericano, Estados Unidos,
1983. P. 89http://www.monografias.com/trabajos
14/metodosgravimetricos/metodosgra
vimetricos.shtml
II.
http://es.wikipedia.org/wiki/An%C3%A
1lisis_gravim%C3%A9trico
III. Biblioteca de Consulta Microsoft
Encarta 2005. 1993-2005
Microsoft Corporation.
IV. Ayres Gilbert, anlisis
cuantitativo Pg. 246-249
You might also like
- Procedimiento de Copelacion y RefinacionDocument7 pagesProcedimiento de Copelacion y RefinacionLuis Enrique Surco FalconNo ratings yet
- Control y Prevención de Riesgos en La Fabricacion de VidrioDocument85 pagesControl y Prevención de Riesgos en La Fabricacion de Vidrioosc8240% (1)
- Guia de Farmacognosia y FitoquímicaDocument93 pagesGuia de Farmacognosia y FitoquímicaAna Karen Lopez Lozano80% (5)
- Laboratorio # 5. Determinación Solidos en Una Muestra de AguaDocument5 pagesLaboratorio # 5. Determinación Solidos en Una Muestra de AguaJUAN MANUELNo ratings yet
- Laboratorio 6 - INFORME PDFDocument6 pagesLaboratorio 6 - INFORME PDFDavid IraeNo ratings yet
- SiO2 y Mat Insoluble en CalDocument3 pagesSiO2 y Mat Insoluble en CalAlejandra NuñezNo ratings yet
- Diagrama de Flujo Gravimetría Lllln2-QuímicaDocument2 pagesDiagrama de Flujo Gravimetría Lllln2-QuímicaJose Manuel JimenezNo ratings yet
- Informe Acabado de Moldeo y ColadaDocument20 pagesInforme Acabado de Moldeo y ColadanirvanaNo ratings yet
- Análisis de Un CarbónDocument15 pagesAnálisis de Un CarbónRONALDNo ratings yet
- Obtención de Un Compuesto BinarioDocument3 pagesObtención de Un Compuesto BinarioHugh RuanoNo ratings yet
- Guevara 13302, Intriago 13240, Ixcotoyac 13190, Gonzalez 13002. Lab 3 % de Humedad y Actividad de Agua QQ AADocument9 pagesGuevara 13302, Intriago 13240, Ixcotoyac 13190, Gonzalez 13002. Lab 3 % de Humedad y Actividad de Agua QQ AAEddy IxcotoyacNo ratings yet
- Práctica 2Document29 pagesPráctica 2Leslie López RangelNo ratings yet
- Guia 2. Fundicion PDFDocument6 pagesGuia 2. Fundicion PDFAngel RojasNo ratings yet
- NMX y 093 Scfi 2003Document5 pagesNMX y 093 Scfi 2003Libros Perfección escritaNo ratings yet
- Practica 3 - Determinación de Cenizas Totales (Contenido Mineral) en Harina de TrigoDocument28 pagesPractica 3 - Determinación de Cenizas Totales (Contenido Mineral) en Harina de TrigoJoel SantosNo ratings yet
- Cobre y Aleaciones de CobreDocument33 pagesCobre y Aleaciones de CobreAnonymous pUyTGziy3L100% (1)
- Determinación de CenizasDocument10 pagesDeterminación de CenizasYudith Rosaluz Imata Condori100% (2)
- Diferencias Entre Gravimetria y VolumetriaDocument3 pagesDiferencias Entre Gravimetria y Volumetriakaterine100% (1)
- Analisis de Oro y PlataDocument9 pagesAnalisis de Oro y PlataRAULYEPEZSANCHEZNo ratings yet
- Informe Práctica 3Document16 pagesInforme Práctica 3Jeniffer Isabel Núñez MoyanoNo ratings yet
- Determinacion Del Calcio-CuantiDocument14 pagesDeterminacion Del Calcio-CuantiJoseNo ratings yet
- Informe 3, Humedad y CenizasDocument3 pagesInforme 3, Humedad y CenizasManuela Hurtado100% (4)
- Azufre en Minerales FierroDocument4 pagesAzufre en Minerales FierroG&S Laboratory100% (1)
- Práctica N 5Document10 pagesPráctica N 5Anthony FreireNo ratings yet
- Diagramas de Humedad y CenizasDocument2 pagesDiagramas de Humedad y CenizasTesla Norales67% (3)
- Informe 3 FITOQUIMICADocument12 pagesInforme 3 FITOQUIMICAFranklin Perez CamonesNo ratings yet
- Tarea 3 CenizasDocument2 pagesTarea 3 CenizasWILLIANS RIVAS CCANSAYANo ratings yet
- PREINFORME 7, 8 y 9Document30 pagesPREINFORME 7, 8 y 9JORGE ENRIQUE CONTRERAS MOLINARESNo ratings yet
- Libreta de Laboratorio y SeguridadDocument3 pagesLibreta de Laboratorio y Seguridadadrian3baqueNo ratings yet