Professional Documents
Culture Documents
Practica 2 Hidrolisis
Uploaded by
Liliana Lino0 ratings0% found this document useful (0 votes)
496 views5 pagesEste documento describe un experimento para determinar si diferentes sales son ácidas, básicas o neutras cuando se disuelven en agua. Se midió el pH de las disoluciones de NaCl, Na2CO3, NH4Cl y FeCl3 usando papel pH y se agregaron indicadores de pH para determinar si las disoluciones eran ácidas o básicas. Los resultados mostraron que NaCl es neutro, Na2CO3 es básico, NH4Cl es ácido y FeCl3 es ácido.
Original Description:
Copyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentEste documento describe un experimento para determinar si diferentes sales son ácidas, básicas o neutras cuando se disuelven en agua. Se midió el pH de las disoluciones de NaCl, Na2CO3, NH4Cl y FeCl3 usando papel pH y se agregaron indicadores de pH para determinar si las disoluciones eran ácidas o básicas. Los resultados mostraron que NaCl es neutro, Na2CO3 es básico, NH4Cl es ácido y FeCl3 es ácido.
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
496 views5 pagesPractica 2 Hidrolisis
Uploaded by
Liliana LinoEste documento describe un experimento para determinar si diferentes sales son ácidas, básicas o neutras cuando se disuelven en agua. Se midió el pH de las disoluciones de NaCl, Na2CO3, NH4Cl y FeCl3 usando papel pH y se agregaron indicadores de pH para determinar si las disoluciones eran ácidas o básicas. Los resultados mostraron que NaCl es neutro, Na2CO3 es básico, NH4Cl es ácido y FeCl3 es ácido.
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 5
4
Nombre y Apellidos: Liliana Lino Zabala
Materia: Qumica Analtica Fecha: 22/03/2014
______________________________________________________________
______
Prctica N 2
HIDRLISIS DE SALES
OBJETIVO/S:
- Ententer las causas por las cuales las disoluciones de sales normales, pueden
ser, no slo neutras, sino cidas o bsicas.
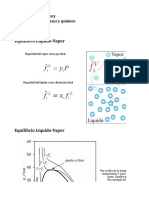
FUNDAMENTO TERICO:
La hidrlisis es la reaccin del agua con una sustancia. Entre las sustancias que
pueden sufrir esta reaccin se encuentran numerosas sales, que als er disueltas en
agua, sus iones constituyentes se combinan con los H
3
O
+
con los OH
-
, procedentes
de la disociacin del agua. Esto produce un desplazamiento del equilibrio de
disociacin del agua y como sonsecuencia se modifica el p.H.
Las sales de los cidos dbiles o bases dbiles se hidrolizan por accin del agua,
dependiendo el grado de la reaccin de la debilidad del cido o la base. Es decir,
cuanto ms dbil sea el cido o la base, mayor es la hidrlisis.
MATERIALES Y REACTIVOS:
Materiales:
- 8 tubos de ensayo
- Gradillas para tubos
- Pipeta Pasteur
- Pipeta de 10ml
- pizeta
Reactivos:
- Agua destilada
- Papel Tornasol: Litmus paper red (cido)
- Papel Tornasol: Litmus paper blue (bsico)
5
- Indicador rojo de Metilo
- Fenolftalena
- Papel p.H
- NH
4
Cl
- Na
2
CO
3
- FeCl
3
- NaCl
PROCEDIMIENTO:
1. Realizaremos cada sal por duplicado, tenemos 4 sal.
2. Tomar 8 tubos de ensayo limpios y pipetear a cada uno de ellos 10ml de agua
destilada.
3. Acontinuacin agregar un pizca de sal, de cada una de las sales en sus tubos
correspondientes.
4. En un vidrio de reloj cortar trocitos de papel tornasol y papel p.H.
5. Ahora, con la ayuda de una pipeta Pasteur echar una gota de cada una de las
disoluciones a los trocitos de papel.
6. Observa los resultados y antalos en una tabla.
7. Por ltimo agregar indicadores:
- A la primera fila de tubos ( 4 tubos con cada una de las disoluciones)
agregar 1 gota de Fenolftalena.:
En medio cido, es incoloro.
En medio Bsico, en Fucsia.
- A la segunda fila de tubos (4 tubos con casa una de las disoluciones),
agregar 1 gota de Rojo de Metilo.
En medio cido, es rojo.
En medio Bsico, es amarillo.
8. Observa el viraje de color, anotando el color que toma la disolucin y
anotndolo en la tabla.
6
ESQUEMA:
7
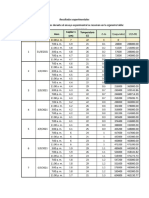
RESULTADOS y CONCLUSIONES
COLOR
N Tornasol
azul
Tornazol
rojo
Papel
p.H
Fenolftalena Rojo de
Metilo
1 NaCl No cambia No cambia 7 incoloro Amarillo
2 Na
2
CO
3
No cambia No cambia 9 Fucsia Amarillo
3 NH
4
Cl Rojo No cambia 6 incoloro Amarillo
4 FeCl
3
Rojo No cambia 3 amarillo Rojo
Podemos comprobar que :
NaCl es una sal Neutra.
Na
2
CO
3,
es una sal Bsica.
NH
4
Cl, es una sal cida
FeCl
3,
es una sal cida.
8
OBSERVACIONES
Datos para los indicadores utilizados:
Indicador Intervalo de
viraje
Color de la forma
cida
Color de la forma
bsica
Tornasol 4,5 8,3 rojo azul
Rojo de Metilo 8,2 6,0 rojo amarillo
Fenolftalena 8,2 10,0 incoloro morado
You might also like
- Informe Calores de Neutralización y SoluciónDocument4 pagesInforme Calores de Neutralización y SoluciónPaula Ramirez100% (1)
- Determinacion de La Dureza Del AguaDocument15 pagesDeterminacion de La Dureza Del Aguarudy quispeNo ratings yet
- Laboratorio Nº10 Determinación de La Dureza Del AguaDocument14 pagesLaboratorio Nº10 Determinación de La Dureza Del AguaAdorian FārNo ratings yet
- IQ 09 01 - Clase2021-12-01Document51 pagesIQ 09 01 - Clase2021-12-01Adolfo LazoNo ratings yet
- Miercoles Saponificación Del Acetato de EtiloDocument12 pagesMiercoles Saponificación Del Acetato de EtiloAnonymous Mp0qhmNo ratings yet
- CompendioEjercicios 3Document10 pagesCompendioEjercicios 3Jesus BuenaventuraNo ratings yet
- Tarea de Equilibrio de 2 ComponentesDocument3 pagesTarea de Equilibrio de 2 ComponentesMaribel MamaniNo ratings yet
- Practica 1Document17 pagesPractica 1Rodrigo100% (1)
- 5.titulaciones ConductimetricasDocument12 pages5.titulaciones Conductimetricasjofre232450% (2)
- Determinacion Acidez en VinagreDocument3 pagesDeterminacion Acidez en VinagreAngie Rozo0% (1)
- PRÁCTICA 2. Determinación de Cloro Activo en Una Muestra de BlanqueadorDocument4 pagesPRÁCTICA 2. Determinación de Cloro Activo en Una Muestra de BlanqueadorYessyMedinaNo ratings yet
- Practica Aniones 4Document7 pagesPractica Aniones 4Grecia Hernandez ReyesNo ratings yet
- Diagrama de Fases de Un Sistema TernarioDocument13 pagesDiagrama de Fases de Un Sistema TernarioJohn Montellanos100% (2)
- Laboratorio de Ingenieria Quimica 1Document4 pagesLaboratorio de Ingenieria Quimica 1Xavier CrAlNo ratings yet
- Precipitacion de SulfurosDocument4 pagesPrecipitacion de SulfurosBruno Valverde100% (1)
- Lab Oratorio 8Document18 pagesLab Oratorio 8erickasegoviacaceresNo ratings yet
- Diagrama de SolubilidadDocument18 pagesDiagrama de SolubilidadTote KingNo ratings yet
- Antecedentes Practica 8Document9 pagesAntecedentes Practica 8Tania MorenoNo ratings yet
- Problemas T15 - 14-01-2019Document6 pagesProblemas T15 - 14-01-2019Miguel Garcia0% (1)
- Balance de Materia Con Reaccion Quimica Hidratacion de Anhidrido AceticoDocument9 pagesBalance de Materia Con Reaccion Quimica Hidratacion de Anhidrido AceticoANAHI ALVARADO TOLENETINONo ratings yet
- Balance de Masa Reactor de Acido NitricoDocument4 pagesBalance de Masa Reactor de Acido NitricoJairo GarciaNo ratings yet
- Produccion de Carbonato de CalcioDocument5 pagesProduccion de Carbonato de CalcioCamilo TorresNo ratings yet
- 2 Practica2 Leyhenry 2019 2 ResueltaDocument34 pages2 Practica2 Leyhenry 2019 2 ResueltaDiegNo ratings yet
- Producción de Acetato de Etilo Por Esterificación Del Ácido AcéticoDocument4 pagesProducción de Acetato de Etilo Por Esterificación Del Ácido AcéticoDaniela Rivera ArenasNo ratings yet
- Actividad4 LUFDocument5 pagesActividad4 LUFNina CárdenasNo ratings yet
- Ejercicios Tema7Document9 pagesEjercicios Tema7Ximena AcNo ratings yet
- Practica Absorcion de CO2Document37 pagesPractica Absorcion de CO2Camilo VanegasNo ratings yet
- Oxidación Química de Un Colorante PDFDocument8 pagesOxidación Química de Un Colorante PDFJona HernandezNo ratings yet
- TP NRO 4 labIIDocument12 pagesTP NRO 4 labIIJose TorreaniNo ratings yet
- Liq 4 Practica 2Document9 pagesLiq 4 Practica 2Daniel FrutosNo ratings yet
- Informee 5Document3 pagesInformee 5luis arces sanchezNo ratings yet
- Conductancia de ElectrolitosDocument10 pagesConductancia de ElectrolitosClaudiaNoeliaIngaGutierrezNo ratings yet
- Síntesis de Colorantes Organicos: Fenolftaleína, Anaranjado de MetiloDocument16 pagesSíntesis de Colorantes Organicos: Fenolftaleína, Anaranjado de MetiloCarlos Ruben Suarez GavidiaNo ratings yet
- Cinética: (C. Valenciana, 2006)Document47 pagesCinética: (C. Valenciana, 2006)Jean ParedesNo ratings yet
- Determinacion de Sulfatos Por EspectrofotometriaDocument13 pagesDeterminacion de Sulfatos Por EspectrofotometriaJorge Roque Villamizar Sanchez0% (1)
- QG Ibq1 Equipo#10 Pract#11 Cinética QuímicaDocument16 pagesQG Ibq1 Equipo#10 Pract#11 Cinética QuímicaSandra Jocelyn Martínez AcevedoNo ratings yet
- Práctica 1 Liq IiDocument10 pagesPráctica 1 Liq IiNeydy Tellez RiveraNo ratings yet
- Labo I (Volumen Molar Parcial)Document14 pagesLabo I (Volumen Molar Parcial)Sandra Hilario QNo ratings yet
- Práctica 2.régimen No PermanenteDocument7 pagesPráctica 2.régimen No PermanenteEstudiante de QuímicaNo ratings yet
- Practica 3a Termoquim PDFDocument3 pagesPractica 3a Termoquim PDFyaleimy fernandez rojasNo ratings yet
- Practica 6Document19 pagesPractica 6Ray AcostaNo ratings yet
- Practica EQUIPO 3 Dureza Del AguaDocument4 pagesPractica EQUIPO 3 Dureza Del AguaRicardo Aragón100% (1)
- Analisis de Cationes Del Tercer GrupoDocument7 pagesAnalisis de Cationes Del Tercer GrupoYessenia AlejoNo ratings yet
- Persulfato TerminadoDocument13 pagesPersulfato TerminadoJonathan SuazoNo ratings yet
- PRACTICA N.1docx PDFDocument3 pagesPRACTICA N.1docx PDFBeymar ContrerasNo ratings yet
- Procesos y Compuestos Quimicos InorganicosDocument3 pagesProcesos y Compuestos Quimicos InorganicosGala De La VegaNo ratings yet
- Volumen Molar ParcialDocument11 pagesVolumen Molar ParcialJose Luis IGNo ratings yet
- Metodo Grafico de WinkelmannDocument4 pagesMetodo Grafico de WinkelmannCarmen HernandezNo ratings yet
- Determinación de Ácido Acético en Una Muestra de Vinagre 5Document8 pagesDeterminación de Ácido Acético en Una Muestra de Vinagre 5Fatima ReyesNo ratings yet
- Guion 3 PDFDocument13 pagesGuion 3 PDFJibran MedinaNo ratings yet
- Descripción Tema Exp N°7 Equilibrio Químico 2022-IDocument25 pagesDescripción Tema Exp N°7 Equilibrio Químico 2022-ICRISTOFER ESTANIS SANCHEZ MENDOZANo ratings yet
- Lab 09Document11 pagesLab 09ljsilva11No ratings yet
- Ejercicios Parcial I Del Dos 2022Document4 pagesEjercicios Parcial I Del Dos 2022Andres RamNo ratings yet
- Aldehidos y Cetonas (Primera Parte)Document9 pagesAldehidos y Cetonas (Primera Parte)0XROBERTX0No ratings yet
- Las Reacciones Electroquímicas de La Corrosión Del AluminioDocument4 pagesLas Reacciones Electroquímicas de La Corrosión Del AluminioCristian HidalgoNo ratings yet
- Oxidación de Vitamina CDocument8 pagesOxidación de Vitamina CAngel LopezNo ratings yet
- Diagrama Ternario Informe LaboDocument14 pagesDiagrama Ternario Informe LaboIz RemyNo ratings yet
- Reporte 2 ElectroquimicaDocument6 pagesReporte 2 ElectroquimicaJose Emmanuel ChemaNo ratings yet
- Informe 9 Medina - MuzzioDocument15 pagesInforme 9 Medina - MuzzioMarcelaDenisseMuzzio100% (1)
- Experimento Ácido BaseDocument13 pagesExperimento Ácido BaseClaudia100% (1)
- RNM PRM SFT PDFDocument17 pagesRNM PRM SFT PDFLiliana LinoNo ratings yet
- Dolor TeoriaDocument11 pagesDolor TeoriaLiliana LinoNo ratings yet
- 2007 Manual Metodos Inmunologicos Completo Web PDFDocument139 pages2007 Manual Metodos Inmunologicos Completo Web PDFLiliana LinoNo ratings yet
- Bromatologia de La LecheDocument17 pagesBromatologia de La LecheLiliana LinoNo ratings yet
- Industria FarmaceúticaDocument7 pagesIndustria FarmaceúticaLiliana LinoNo ratings yet
- Extraccion Mecanica Mani 1Document5 pagesExtraccion Mecanica Mani 1Liliana LinoNo ratings yet
- Contador Celular 1Document11 pagesContador Celular 1Liliana LinoNo ratings yet
- Operaciones Farmaceúticas Básicas - Docx ExpoDocument2 pagesOperaciones Farmaceúticas Básicas - Docx ExpoLiliana Lino63% (8)
- Informe Perfil LipidicoDocument19 pagesInforme Perfil LipidicoLiliana Lino67% (3)
- Practica 5 GravimetriaDocument7 pagesPractica 5 GravimetriaLiliana LinoNo ratings yet
- Laboratorio de Biologia y GeneticaDocument12 pagesLaboratorio de Biologia y GeneticaLiliana LinoNo ratings yet
- Farmacia ModernaDocument4 pagesFarmacia ModernaLiliana LinoNo ratings yet
- Ud 4 Técnicas SiembraDocument5 pagesUd 4 Técnicas SiembraLiliana LinoNo ratings yet
- FotografiaDocument31 pagesFotografiaRafael Gtz GamaNo ratings yet
- Armadura EspacialDocument2 pagesArmadura EspacialClau GómezNo ratings yet
- Apuntamiento de Antena SatelitalDocument15 pagesApuntamiento de Antena SatelitalFer FloresNo ratings yet
- Metodo de Doble IntegraciónDocument7 pagesMetodo de Doble IntegraciónMax Solis VitorNo ratings yet
- Cinetica y EquilibrioDocument23 pagesCinetica y EquilibrioNieves Del Barrio Masegosa100% (1)
- Historia de Vida FinalDocument32 pagesHistoria de Vida FinalJesúsEnriqueGarciaNo ratings yet
- Grupo 8 (Balotario Final)Document7 pagesGrupo 8 (Balotario Final)Jesus Ferro VillaNo ratings yet
- Resumen MicropilotesDocument7 pagesResumen Micropilotesoavg06No ratings yet
- Unidad 3. Transformada de La Laplace y Series de FourierDocument76 pagesUnidad 3. Transformada de La Laplace y Series de FourierJuan Gongora50% (2)
- Ecuación EikonalDocument3 pagesEcuación EikonalNoe Hernandez TorrejonNo ratings yet
- Caratula de Física IIIDocument10 pagesCaratula de Física IIIPalma Quito FrankNo ratings yet
- Co2 ManualDocument124 pagesCo2 ManualARTURONo ratings yet
- (Tutoría) Práctica #1 Fuerza Eléctrica y Campo EléctricoDocument2 pages(Tutoría) Práctica #1 Fuerza Eléctrica y Campo EléctricoEder BellosoNo ratings yet
- Diagram AsDocument5 pagesDiagram AsAnonymous 26x1DNpIUNo ratings yet
- Guia 13,14,15 Interacciones Parte I PDFDocument5 pagesGuia 13,14,15 Interacciones Parte I PDFlomioylotuyoNo ratings yet
- Phelps Dodge Caracteristicas Nyy y N2xy-1Document11 pagesPhelps Dodge Caracteristicas Nyy y N2xy-1Eduardo EspinozaNo ratings yet
- Memoria Subestación ELÉCTRICADocument17 pagesMemoria Subestación ELÉCTRICAfernandezh0% (1)
- Tecnicas de DiagnosticoDocument127 pagesTecnicas de DiagnosticoLewis TeranNo ratings yet
- Programa Cpem 55 3°a T.M. 2011Document3 pagesPrograma Cpem 55 3°a T.M. 2011Jexx ValleNo ratings yet
- Razonamiento Abstracto MatematicaDocument8 pagesRazonamiento Abstracto MatematicaSusu García AlarcónNo ratings yet
- C2B2 Examen Bimestral 3Document3 pagesC2B2 Examen Bimestral 3Roberto SaucedoNo ratings yet
- Metodo de ImpedanciasDocument14 pagesMetodo de ImpedanciasdiegoNo ratings yet
- TP N°2 - ElectroestaticaDocument8 pagesTP N°2 - ElectroestaticaMauricioNo ratings yet
- Resistencia de MaterialesDocument24 pagesResistencia de MaterialesJose ManuelNo ratings yet
- M MMP 1-06-03 GranulometriaDocument14 pagesM MMP 1-06-03 GranulometriaLuis Alberto cortezNo ratings yet
- Practica Esiqie Secador RotatorioDocument6 pagesPractica Esiqie Secador RotatorioLizbeth Soto0% (1)
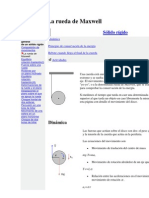
- La Rueda de MaxwellDocument4 pagesLa Rueda de Maxwelljojito11No ratings yet
- Emulsiones No AcuosasDocument43 pagesEmulsiones No AcuosasAdhemar Arroyo JimenezNo ratings yet
- Reactor de Tanque AgitadoDocument12 pagesReactor de Tanque AgitadoMiguel Angel Romani MontesNo ratings yet
- Analitica Experimental Oxido ReducciónDocument22 pagesAnalitica Experimental Oxido ReducciónKarina GFNo ratings yet