Professional Documents
Culture Documents
Diagrama Líquido Vapor Ecuación Wilson Matlab
Uploaded by
aruazul100%(1)100% found this document useful (1 vote)
298 views5 pagesCopyright
© Attribution Non-Commercial (BY-NC)
Available Formats
PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Attribution Non-Commercial (BY-NC)
Available Formats
Download as PDF, TXT or read online from Scribd
100%(1)100% found this document useful (1 vote)
298 views5 pagesDiagrama Líquido Vapor Ecuación Wilson Matlab
Uploaded by
aruazulCopyright:
Attribution Non-Commercial (BY-NC)
Available Formats
Download as PDF, TXT or read online from Scribd
You are on page 1of 5
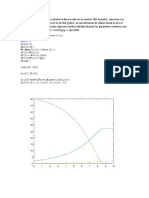
Elaboracin de Diagrama Lquido-Vapor mediante coeficientes de fugacidad y actividad
utilizando la ecuacin de Wilson en un sistema binario: Acetato de Etilo-1 Propanol
Se comienza calculando los coeficientes de actividad con base en la funcin de exceso
utilizando la ecuacin de Wilson para una mezcla lquida, a partir de la siguiente expresin
para la energa libre de Gibbs molar de exceso de la mezcla:
La anterior ecuacin se utiliza para los coeficientes de actividad del lquido, mediante el
siguiente desarrollo matemtico:
x
1
=1x
2
Los parmetros de la ecuacin de Wilson son calculados con las siguientes ecuaciones o
pueden ser consultados en la literatura.
Donde:
I
i
L
=:olumcn molor Jcl lquiJo i puro
z
i
s =cncrgos Jc intcroccin cntrc los molculos cspcciicoJos cn los subinJiccs
La presin de vapor o de saturacin del lquido i se calcula mediante la Ecuacin de Antoine.
De la ecuacin para el equilibrio fsico a bajas presiones y de la ley de Dalton de las presiones
parciales se obtiene:
Los cuales para el sistema binario se convierte en:
El clculo del coeficiente de fugacidad
1
del gas i en la mezcla gaseosa, se hace de la
siguiente manera:
Zm puede calcularse para T y P dadas a partir de la ecuacin cbica de Redlich-Kwong para
la mezcla gaseosa (se selecciona la raz real de mayor valor) usando los pseudo-parmetros
de Kay:
Cdigo de Programacin:
f unct i on wwi l son( p, T, x1)
cl ose
z=1;
k=1;
p=340; %mmHg
T=55; %Temper at ur a de Ebul l i ci n del component e mas vol at i l
x1=1;
V1L=97. 8;
V2L=74. 7;
Lambda1211=2. 65; %gcal / gmol
Lambda1222=2. 55; %gcal / gmol
R=1. 9872;
%Const ant es de Ant oi ne
%Acet at o de Et i l
a1=7. 10179;
b1=1244. 951;
c1=217. 881;
Pc=38. 8;
Tc=523. 3;
%Pr opanol
a2=8. 37895;
b2=1788. 020;
c2=227. 438;
Pc=51. 75; %bar
Tc=536. 8; %K)
whi l e x1>=0
x2=1- x1;
A12=( V2L/ V1L) *( exp( ( - Lambda1211) / ( R*T) ) ) ;
A21=( V1L/ V2L) *( exp( ( - Lambda1222) / ( R*T) ) ) ;
G1=exp( - l og( x1+( A12*x2) ) +x2*( ( A12/ ( x1+( A12*x2) ) ) -
( A21/ ( ( A21*x1) +x2) ) ) ) ;
G2=exp( - l og( x2+( A21*x1) ) +x1*( ( A12/ ( x1+( A12*x2) ) ) -
( A21/ ( ( A21*x1) +x2) ) ) ) ;
p1=exp( a1- ( b1/ ( T- c1) ) ) ;
p2=exp( a2- ( b2/ ( T- c2) ) ) ;
y1=( ( x1*( p1*G1) ) / ( ( ( x1*( p1*G1) ) +( x2*( p2*G2) ) ) ) ) ;
Pest =( ( y1*p) / ( x1*G1) ) ;
z=abs( Pest - p1) ;
T=( b1/ ( a1- l og( Pest ) ) ) +c1;
i f z <=0. 1
VT( k) =T;
Vx1( k) =x1;
Vy1( k) =y1;
k=k+1;
T=T+1. 0;
x1=x1- 0. 001;
end
end
pl ot ( Vx1, VT, ' r ' , Vy1, VT, ' b' )
gr i d
t i t l e( ' CURVAS DE PUNTO DE ROCI O Y PUNTO DE BURBUJ A: SI STEMA ACETATO DE
ETI LO - PROPANOL' )
xl abel ( ' FRACCI ON MOLAR DEL COMPONENTE MAS VOLATI L' )
yl abel ( ' TEMPERATURA [ K] ' )
f i gur e
pl ot ( Vx1, Vy1, ' r ' )
t i t l e( ' cur vas de x1 vs y1' )
gr i d
hol d on
x=l i nspace( 0, 1, 100) ;
y=x;
pl ot ( x, y)
xl abel ( ' FRACCI ON MOLAR DEL COMPONENTE MAS VOLATI L EN EL LI QUI DO' )
yl abel ( ' FRACCI ON MOLAR DEL COMPONENTE MAS VOLATI L EN EL VAPOR' )
f unct i on [ T, A1, A2, Am, B1, B2, Bm, Fi 1, Fi 2, y1m, pi est 1, z, Tast ] =cal c( pi est ,
y1, p, x1, GAM1, zm, p1, p2, GAM2)
T=( b1/ ( a1- l og( Pest ) ) ) +c1;
A1=( 0. 4278/ ( Pc1*( ( T/ Tc1) ^2. 5) ) ) ^0. 5;
A2=( 0. 4278/ ( Pc2*( ( T/ Tc2) ^2. 5) ) ) ^0. 5;
Am=( y1*A1) +( 1- y1) *A2;
B1=0. 0867/ ( Pc1*( T/ Tc1) ) ;
B2=0. 0867/ ( Pc2*( T/ Tc2) ) ;
Bm=( y1*B1) +( 1- y1) *B2;
Fi 1=10^( 0. 4343*( zm- 1) *( B1/ Bm) - l og10( zm-
Bm*( p/ 760) ) *( Am^2/ Bm) *l og10( 1+( ( Bm*( p/ 760) ) / zm) ) *( 2*A1/ Am- ( B1/ Bm) ) ) ;
Fi 2=10^( 0. 4343*( zm- 1) *( B2/ Bm) - l og10( zm-
Bm*( p/ 760) ) *( Am^2/ Bm) *l og10( 1+( ( Bm*( p/ 760) ) / zm) ) *( 2*A2/ Am- ( B2/ Bm) ) ) ;
y1m=( ( x1*p1*G1) / Fi 1) / ( ( ( x1*p1*G1) / Fi 1) +( ( ( 1- x1) *p2*G2) / Fi 2) ) ;
Pest 1=( Fi 1*y1m*p) / ( x1*G1) ;
z=abs( Pest 1- Pest ) ;
Tast =( b1/ ( a1- l og( Pest 1) ) ) +c1 ;
Resultados:
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1
900
950
1000
1050
1100
1150
1200
DIAGRAMA LQUIDO-VAPOR: SISTEMA ACETATO DE ETILO - PROPANOL
FRACCION MOLAR DEL COMPONENTE MAS VOLATIL
T
E
M
P
E
R
A
T
U
R
A
[
K
]
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1
0
0.1
0.2
0.3
0.4
0.5
0.6
0.7
0.8
0.9
1
CURVA DE x1 vs y1
FRACCION MOLAR DEL COMPONENTE MAS VOLATIL EN EL LIQUIDO
F
R
A
C
C
I
O
N
M
O
L
A
R
D
E
L
C
O
M
P
O
N
E
N
T
E
M
A
S
V
O
L
A
T
I
L
E
N
E
L
V
A
P
O
R
You might also like
- Pirolisis Del Benceno Matlab y ScilabDocument18 pagesPirolisis Del Benceno Matlab y ScilabnataliaNo ratings yet
- Problem As Org ADocument29 pagesProblem As Org AMoises Aguirre MuñozNo ratings yet
- Laboratorio Nº10 Determinación de La Dureza Del AguaDocument14 pagesLaboratorio Nº10 Determinación de La Dureza Del AguaAdorian FārNo ratings yet
- Ejercicios Del Punto de Pliegue PDFDocument2 pagesEjercicios Del Punto de Pliegue PDFGilbert Rodriguez PalmaNo ratings yet
- Ejercicio para Punto Extra PDFDocument30 pagesEjercicio para Punto Extra PDFJonathan AlonsoNo ratings yet
- La Fermentacion de Glucosa A Etanol Se Lleva A Cabo en Un Reactor TAD Usando SDocument1 pageLa Fermentacion de Glucosa A Etanol Se Lleva A Cabo en Un Reactor TAD Usando SAndrea Bocanegra MartinezNo ratings yet
- Problemas Cap 10Document29 pagesProblemas Cap 10Oscar Andrade AvilaNo ratings yet
- Practica No. 4 Análisis y Evaluación de Una Torre de Destilación Empleando Simuladores de Procesos. Trabajo Práctico Sistemas Multicomponente.Document26 pagesPractica No. 4 Análisis y Evaluación de Una Torre de Destilación Empleando Simuladores de Procesos. Trabajo Práctico Sistemas Multicomponente.Pablo CamejoNo ratings yet
- 2 o Parcial de Laboratorio de Fisicoquimica Fquim 2018Document2 pages2 o Parcial de Laboratorio de Fisicoquimica Fquim 2018DianaLizethRomHinojosaNo ratings yet
- Apéndice KDocument3 pagesApéndice KMariana CarmonaNo ratings yet
- Ejer D Trans D Masa II Con Graficos ADocument20 pagesEjer D Trans D Masa II Con Graficos AJulian SoloNo ratings yet
- Segundo Examen Parcial de Diseño de Procesos - 2021Document3 pagesSegundo Examen Parcial de Diseño de Procesos - 2021Kenia Paola Betsabe Martinez GalvanNo ratings yet
- FlashDocument7 pagesFlashLidia Cecilia Jesús CuevasNo ratings yet
- Guia de Aprendizaje 2UI - CP1Document6 pagesGuia de Aprendizaje 2UI - CP1javier gagoNo ratings yet
- Absorcion No IsotermicaDocument6 pagesAbsorcion No IsotermicaNatalia Moreno MorenoNo ratings yet
- Ev 2 PropiDocument3 pagesEv 2 PropiandiesNo ratings yet
- Equlibrio de Reacciones Termodinamica de Acetato de EtiloDocument21 pagesEqulibrio de Reacciones Termodinamica de Acetato de EtiloBryan Emerson Chupayo SandovalNo ratings yet
- Feno EjercicioDocument4 pagesFeno EjercicioDianis ChavezNo ratings yet
- Examen Parcial Pi135a - 2021-2Document3 pagesExamen Parcial Pi135a - 2021-2Katherine Ayala CordovaNo ratings yet
- Clase 3 Aux. Emerson (I-2020)Document4 pagesClase 3 Aux. Emerson (I-2020)Edzon YujraNo ratings yet
- Taller Final Cinética QuímicaDocument91 pagesTaller Final Cinética QuímicaCRISTANCHO TORRES AURA CAMILANo ratings yet
- Ecuaciones de Estado y Factores CruzadosDocument21 pagesEcuaciones de Estado y Factores CruzadosJosé Luis LMNo ratings yet
- Ejercicios Conducción Calor UnidimensionalDocument4 pagesEjercicios Conducción Calor UnidimensionalDiego Alejandro Castaño BarragánNo ratings yet
- Problemas de Fugacidad PDFDocument1 pageProblemas de Fugacidad PDFMariia Martinezz AguiilarNo ratings yet
- Laboratorio Teorico, PasaporteDocument6 pagesLaboratorio Teorico, PasaporteJuan GudielNo ratings yet
- Curso Chemcad 03 PDFDocument60 pagesCurso Chemcad 03 PDFAdrianaCarbonellNo ratings yet
- Problema 1. Teorema Pi de BuckinghamDocument6 pagesProblema 1. Teorema Pi de BuckinghamAna Sordo CastilloNo ratings yet
- Trabajo CumenoDocument11 pagesTrabajo CumenoAnonymous zhDyxFqeZNo ratings yet
- Absorción So2 Seccion CDocument25 pagesAbsorción So2 Seccion CFernando guevara venturaNo ratings yet
- Laboratorio1 CorregidoDocument17 pagesLaboratorio1 CorregidoDorothy RojasNo ratings yet
- Balance de Energia - CristalizadorDocument2 pagesBalance de Energia - CristalizadorTaniaNo ratings yet
- Producción Del Dimetil Carbonat1Document7 pagesProducción Del Dimetil Carbonat1floryguapoNo ratings yet
- Determinacion de La AeptDocument13 pagesDeterminacion de La AeptJavier JulianNo ratings yet
- Ejercicio # 10 - Aislamiento Tuberias AnálisisDocument1 pageEjercicio # 10 - Aislamiento Tuberias AnálisisDaniela Guáqueta0% (1)
- Problemas de Termo1Document3 pagesProblemas de Termo1LOPEZ GARCÍA VANIA ABIGAILNo ratings yet
- Propiedades Molares ParcialesDocument18 pagesPropiedades Molares ParcialesFrancisco LaraNo ratings yet
- Guia Problemas Difusion Reaccion 2018051731Document7 pagesGuia Problemas Difusion Reaccion 2018051731Ana Belen ZuritaNo ratings yet
- Problema 3.27Document6 pagesProblema 3.27Diego.CCNo ratings yet
- RTA y PistonDocument22 pagesRTA y PistonMalu AisneNo ratings yet
- Practica Nº3 1-2019Document9 pagesPractica Nº3 1-2019Libertad Mariana Casanova VelásquezNo ratings yet
- Microsoft PowerPoint - Problemas Resuelt PDFDocument6 pagesMicrosoft PowerPoint - Problemas Resuelt PDFMarckos Ramos AbadNo ratings yet
- Reporte de Cristalización PEMEXDocument21 pagesReporte de Cristalización PEMEXjesus arcadio100% (1)
- Cuaderno Liquid o Liquid oDocument52 pagesCuaderno Liquid o Liquid oCatalina Camargo Angarita89% (9)
- Laboratorio 2Document13 pagesLaboratorio 2Angel Eduardo VillónNo ratings yet
- Coeficientes - de - Difusion - MASA IDocument9 pagesCoeficientes - de - Difusion - MASA IEduardo VazquezNo ratings yet
- Practica Determinacion de FosforoDocument8 pagesPractica Determinacion de FosforoJairoNo ratings yet
- Resolución de Problema de Destilación Por El Método de PonchonDocument14 pagesResolución de Problema de Destilación Por El Método de PonchonAnahi Montiel100% (1)
- Batch IsotérmicoDocument14 pagesBatch IsotérmicoFrancisco Lara50% (2)
- PERVAPORACIONDocument27 pagesPERVAPORACIONLuis100% (1)
- Lou - I - Agitacion 2008-IiDocument22 pagesLou - I - Agitacion 2008-IiMax1267No ratings yet
- LAB - INTEGRAL I - U5yU6Document13 pagesLAB - INTEGRAL I - U5yU6Alondra MendezNo ratings yet
- Taller de Transferencia de Masa-Tema 1Document4 pagesTaller de Transferencia de Masa-Tema 1luisa0% (1)
- Ejemplo de Metodo-Unifac Reporte 1Document7 pagesEjemplo de Metodo-Unifac Reporte 1chavaNo ratings yet
- 3-26 Ocon TojoDocument6 pages3-26 Ocon TojoJurgen Corpi GómezNo ratings yet
- Balance de MateriaDocument23 pagesBalance de MateriaDaniel Moroco RiveraNo ratings yet
- Transferencia de MasaDocument5 pagesTransferencia de MasaELIZABETHNo ratings yet
- 1er Examen Parcial Termoii Montalvan Zuniga MarceDocument4 pages1er Examen Parcial Termoii Montalvan Zuniga MarceJazmin Flores MondragónNo ratings yet
- Segundo Examen Parcial de Metodos NumericosDocument4 pagesSegundo Examen Parcial de Metodos NumericosThalii Ramiirez MaldonadoNo ratings yet
- Unifac - Programa MatlabDocument3 pagesUnifac - Programa Matlabjessica noemy chuquimantari mallquiNo ratings yet
- Prob 12.5 y 12.7 Henley and SeaderDocument3 pagesProb 12.5 y 12.7 Henley and SeaderaruazulNo ratings yet
- Prob 15.8 Henley and SeaderDocument5 pagesProb 15.8 Henley and SeaderaruazulNo ratings yet
- Participantes en Las OrganizacionesDocument6 pagesParticipantes en Las OrganizacionesaruazulNo ratings yet
- Bioestimulación y BioaumentaciónDocument2 pagesBioestimulación y Bioaumentaciónaruazul88% (8)
- Feria de Ciencias 2014Document3 pagesFeria de Ciencias 2014Edgar AlarcónNo ratings yet
- G1. Actividad Sobre Fundamentos de Electricidad 1Document7 pagesG1. Actividad Sobre Fundamentos de Electricidad 1Miguel Angel PerezNo ratings yet
- Pavimento Flexible, Concreto Asfaltico y Mantenimiento.Document6 pagesPavimento Flexible, Concreto Asfaltico y Mantenimiento.cbruk1No ratings yet
- SIMBA en Perforación de RocasDocument71 pagesSIMBA en Perforación de RocasSamuel Klinton100% (1)
- El Az+ - Car Elaborado en Central El PalmarDocument7 pagesEl Az+ - Car Elaborado en Central El PalmarDana Roberts0% (1)
- Turbo Máquinas Hidráulicas Motrices o MotorasDocument8 pagesTurbo Máquinas Hidráulicas Motrices o Motoraslapelilameta100% (1)
- Caso Practico Contaminación AtmosféricaDocument4 pagesCaso Practico Contaminación AtmosféricaFrancisca Andrade AlvaradoNo ratings yet
- Práctico Integrador de Sistemas de Ec. LinealesDocument2 pagesPráctico Integrador de Sistemas de Ec. LinealescelesteNo ratings yet
- Ejercicios de Enlaces Quimicos ResueltosDocument4 pagesEjercicios de Enlaces Quimicos ResueltosLeidy Johana Cely RojasNo ratings yet
- Tamisado y SecadoDocument13 pagesTamisado y SecadoDiana Sevillano AscateNo ratings yet
- Evaluacion 3DDocument1 pageEvaluacion 3DEndis Livingston ForbesNo ratings yet
- Mercedes Benz ACTROSDocument2 pagesMercedes Benz ACTROSDiego Santana0% (1)
- Guia 2.1 de ElectricidadDocument8 pagesGuia 2.1 de ElectricidadisneldaNo ratings yet
- Anexo 1Document5 pagesAnexo 1Eliud Gutierrez HernandezNo ratings yet
- Reforzamiento Sismico de ColegiosDocument18 pagesReforzamiento Sismico de Colegioshomero_a_lNo ratings yet
- 07-Un Casco de Seguridad Puede SalvarloDocument1 page07-Un Casco de Seguridad Puede SalvarloAnalista Seguridad industrialNo ratings yet
- Propuesta de Mejora en El Proceso de ProducciónDocument30 pagesPropuesta de Mejora en El Proceso de ProducciónKevin PeñaNo ratings yet
- Formato Pedidos Condesa Junio 2020Document1 pageFormato Pedidos Condesa Junio 2020Alejandro VillanuevaNo ratings yet
- Certificado de Producto 2014039273Document1 pageCertificado de Producto 2014039273Ramiro OrtegaNo ratings yet
- Contrato de ArrendamientoDocument3 pagesContrato de ArrendamientoBaruchs BaruchsNo ratings yet
- Arbol de Causa Efecto y de Medios y Fines - Proyecto de InvestigacionDocument4 pagesArbol de Causa Efecto y de Medios y Fines - Proyecto de InvestigacionRoberth Erasmo Chavez GallegosNo ratings yet
- Transportadores Hidraulicos OrdenadoDocument101 pagesTransportadores Hidraulicos Ordenadohahimive0% (1)
- EJERCICIOS DE CONVECCIÓN FORZADA y LIBREDocument3 pagesEJERCICIOS DE CONVECCIÓN FORZADA y LIBREAdrian NarvaezNo ratings yet
- Informe HojaDocument11 pagesInforme Hojabrayan de hoyosNo ratings yet
- DIgSILENT Proyect2Document1 pageDIgSILENT Proyect2Jhordy Cristobal MattosNo ratings yet
- Informe Tipo de Analisis ElectricoDocument11 pagesInforme Tipo de Analisis ElectricoCristián JaramilloNo ratings yet
- F-DC-04 Manual de Prácticas U3-4Document5 pagesF-DC-04 Manual de Prácticas U3-4EnriqueRomeroNo ratings yet
- Memoria de Calculo Iluminación ExteriorDocument17 pagesMemoria de Calculo Iluminación ExteriorCesar Gabriel Berdejo Rivera100% (1)
- Taller de Flujo Multifasico-2008 - (v6) PDFDocument78 pagesTaller de Flujo Multifasico-2008 - (v6) PDFarmando0212-1100% (1)
- Cuadro Comparativo Teorias PsicologicasDocument3 pagesCuadro Comparativo Teorias Psicologicaszaida100% (1)