Professional Documents
Culture Documents
Estudo dos sistemas dispersos: soluções, colóides e suspensões
Uploaded by
Marco MoreiraOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Estudo dos sistemas dispersos: soluções, colóides e suspensões
Uploaded by
Marco MoreiraCopyright:
Available Formats
1 .
EST U DO DOS SI ST EM A S DI SPERSOS
1 .1 . Di s p e r s e s
Uma disperso consiste num sistema no qual uma substncia (disperso) encontra-se disseminada, na forma de pequenas partculas no interior de outra (dispersante) Dependendo do tamanho da partcula que constitui o disperso, a disperso assume caractersticas diversas, sendo classificada em trs tipos : solues, colides e suspenses. A classificao acima feita de acordo com o dimetro mdio das partculas dos disperso: Tipo de disperso Soluo verdadeira Colide Suspenso Tamanho da partcula dispersa entre 0 e 10-9 m (1 nanometro) entre 10-9 e 10-6 m (1 103 nanometro) acima de 10-6 m (acima de 103 nanometro)
Como caractersticas gerais dos trs tipos de disperses podemos mencionar que: a) solues verdadeiras ou solues: - o disperso (soluto) constitudo de tomos, ons ou pequenas molculas; - pelas reduzidas dimenses do disperso (soluto), as solues verdadeiras sempre sero sistemas homogneos, sendo que as partculas no so visveis mesmo com equipamentos ticos de alta resoluo e ampliao; - no h sedimentao das partculas e no possvel a sua separao por nenhum tipo de filtro; Exemplos: - sacarose em gua, NaCl em gua, etanol em gua, atmosfera (isenta de poeira), etc. b) colides: - o disperso constitudo por aglomerados de tomos, molculas ou ons ou, at mesmo, por macromolculas; - as partculas do disperso so visualizveis em equipamentos ticos (microscpios) de alta resoluo (ampliao); - as partculas podem ser separadas por ultracentrifugao (elevado nmero de RPM) ou por ultrafiltrao (filtros cujo dimetro do poro bastante reduzido);
Exemplos: leite, gelatina em gua, fumaas em geral, neblina, etc. c) suspenses: - o disperso constitudo de grandes aglomerados de tomos ou molculas; - as partculas do disperso so visveis em microscpio comum, constituindo-se em sistemas heterogneos; - as partculas do disperso sedimenta-se por ao da gravidade ou em centrfugas comuns podendo, tambm, ser separadas por filtros comuns de laboratrio; Exemplos: poeira no ar.
1 .2 . Es t u d o d a s So l u e s v e r d a d e i r a s o u So l u e s
Dentre os sistemas dispersos, as solues verdadeiras ou simplesmente solues so extremamente importantes no cotidiano do qumica, pois nas atividades mais comuns de laboratrio (anlises, snteses, separaes, formulao de produtos, etc) o qumico trabalha com solues que, em geral, so aquosas. 1.2.1. Formao de Solues Quando uma soluo formada ocorre uma disseminao espontnea de uma substncia no interior de outra, originando um sistema mais entrpico (desorganizado) que as substncias originais.
substncia A substncia B mistura A + B (soluo)
lllll lllll lllll
OOOO OOOO OOOO
l Ol Ol O lO l O Ol Ol O l Ol lO lO lOl Ol lO
parede de separao
removendo a parede
A fora motriz para esse processo de mistura a tendncia espontnea para um estado de maior desordem molecular (maior entropia). Para que ocorra o processo da dissoluo necessrio que as partculas do soluto e do solvente apresentem atraes entre si decorrentes de foras de natureza eletrosttica.
Em geral as foras atrativas dependem do tipo de soluto e solvente. Assim quando dissolvemos etanol (C2H5 OH) em gua, em virtude da presena do grupo OH na gua e no etanol a fora atrativa entre essas molculas a Ponte de Hidrognio ou Ligao de Hidrognio. Se a cadeia carbnica aumenta, diminui a polaridade da molcula do lcool e, com isso, a sua solubilidade em gua, por concorrncia de foras Van Der Waals dipolo induzido dipolo induzido. - metanol, etanol e propanol altamente solveis em gua; - butanol solubilidade 0,12 mols/100 g de gua; - pentanol solubilidade 0,031 mols/100 g de gua. Esse mesmo tipo de interao ir ocorrer naquelas molculas que apresentam grupos hidroxila ou amina (O H ou N H), como o caso dos lcoois de pequena cadeia carbnica, cidos carboxlicos, aminas e amidas. Nos glicdios (glicose, frutose, sacarose,...) a presena dos diversos grupos hidroxila ao longo da cadeia carbnica desses compostos tambm justifica a sua grande solubilidade em gua. Com exceo dos cidos carboxlicos, nas demais substncias ocorre apenas o processo de dissoluo, sem ionizao.
O fenmeno , portanto, explicado pela hidratao sofrida pelas extremidades polarizadas da molcula. A extremidade negativa da molcula da gua (localizada no tomo de oxignio) direciona-se para a regio de densidade positiva da molcula polar e as extremidades de carga positiva (localizadas nos tomos de hidrognio) direcionam-se para a regio de densidade negativa.
Quando dissolvemos um cristal de NaCl em gua, alm do processo da dissoluo ocorre a dissociao inica do soluto, sendo que os ons originados apresentam-se, na soluo, engaiolados por molculas do solvente (hidratao ou solvatao), unidos por foras atrativas do tipo on dipolo. Os compostos inicos se dissolvem na gua quando as foras de atrao entre os dipolos da H2O e os ons so maiores que as foras de atrao entre os ons no cristal. Nas bordas e quinas do cristal as foras atrativas entre os ons so menos intensas, favorecendo a interao com as molculas do solvente. Conforme as molculas de gua vo retirando os ons do cristal, novos ons so expostos e o processo continua, dissolvendo o cristal inico. A camada de molculas orientadas que cercam um on ajuda a neutralizar a carga do mesmo e serve para impedir os ons de carga oposta a se atrarem, formando uma espcie de blindagem. A orientao espacial das molculas de solvatao definida para um determinado tipo de on. Por exemplo: - o on Na+ hidrata-se com seis molculas de gua, o mesmo ocorrendo para o on Cl-; - o on Al+3 hidrata-se com oito molculas de gua. Nas solues de solutos apolares em solventes polares, como o caso de gases (O2, CO2, etc...) justifica-se a solubilidade a partir de interaes de Van Der Waals do tipo dipolo permanente dipolo induzido. Nesse caso temperatura e presso so fatores que concorrem significativamente para explicar a sulubilidade de um gs apolar na gua, o que, at certo ponto, contradiz a regra de solubilidade de que semelhante dissolve semelhante.
1.2.2. Classificao das Solues As solues podem ser classificadas segundo os critrios: a) quanto ao estado fsico: - slidas: ligas metlicas (ao = Fe, C, Mn; lato = Cu e Zn; bronze = Cu e Sn,..), medicamentos (comprimidos),... - lquidas: bebidas no gaseificados, bebidas alcolicas, gua mineral sem gs, soro fisiolgico,... - gasosas: ar (isento de poeira), GLP (vazado),.. *** misturas gasosas sempre so homognas !!! b) quanto natureza do soluto: - moleculares: as partculas do soluto so molculas. ex.: C12H22O11(slida) C12H22O11(aquosa) ex.: NaCl (slido) Na+(aquoso) + Cl-(aquoso)
H2O H2O
- inicas: as partculas do soluto so ons.
c) quanto ao Coeficiente de Solubilidade (C.S.): *** O Coeficiente de Solubilidade representa a maior massa que pode ser dissolvida em certa quantidade padro de um solvente, em determinada temperatura. ex.: NaCl = 35,7 gramas/100 gramas de H2O 00C. CaSO4 = 0,2 gramas/100 gramas de H2O 00 C. AgNO3 = 122 gramas/100 gramas de H2O 00 C. O Coeficiente de Solubilidade varia com a temperatura e, no caso de substncias gasosas, varia com a presso. A influncia da temperatura sobre a solubilidade varia de uma substncia para outra. As curvas de solubilidade so obtidas experimentalmente. No caso de um gs a solubilidade inversamente proporcional ao aumento da temperatura, isto , diminui a solubilidade com o aumento da temperatura e diretamente proporcional presso. Por esse motivo os peixes, nos dias quentes de vero preferem permanecer na sombra, sob as pedras e em locais mais profundos. A influncia na presso evidenciada pela Lei de Henry: C = k.P
onde:
C a concentrao de gs dissolvido; k uma constante de proporcionalidade; P a presso exercida sobre o sistema.
O grfico a seguir mostra, para solutos slidos, a influncia da temperatura na solubilidade. Para a maior parte dos sais a solubilidade aumenta com o aumento da temperatura, com exceo do Ce2(SO4)3. De todos os sais representados no diagrama ao lado o NaCl aquele que a variao de temperatura exerce a menor influncia na solubilidade e o KNO2 e CaCl2 aqueles sais cuja solubilidade mais fortemente influenciada pela variao de
Quanto ao C. S. as solues podem ser: - insaturadas: a quantidade de soluto dissolvido inferior ao C.S. ex.: 3,0 gramas de NaCl/100 gramas de H2O 00C. - saturadas: a quantidade de soluto dissolvido igual ao C. S. ex.: 35,7 gramas de NaCl/100 gramas de H2O 00 C. - super-saturadas: so solues obtidas por tcnicas especiais, nas quais a quantidade de soluto dissolvido superior ao C. S. No preparo de tais solues aquece-se a soluo na qual haja corpo de fundo do soluto at uma temperatura na qual ocorra total dissoluo, resfriando-se, aps, de forma gradativa, at alcanar a temperatura de referncia com o excesso de soluto dissolvido. Estas solues so muito instveis, podendo o excesso de soluto precipitar (sedimentar) por agitao mecnica, choque brusco de temperatura ou adio de um germen de cristalizao.
1.2.3. Preparao de solues Na atividade de laboratrio, seja em nvel acadmico ou na prpria indstria, as substncias so utilizadas, de modo geral, na forma de solues. Numa soluo, alm da proporo entre a quantidade de soluto e de soluo (ou solvente), expressa na forma de uma concentrao , indispensvel que se conheam caractersticas especficas de cada soluto, na preparao adequada dessa soluo. Dependendo da utilizao da soluo as mesmas devem ser consideradas segundo duas caractersticas bsicas: a) solues padro: usadas para fins analticos contendo uma quantidade exatamente conhecida de um reagente qualquer, na unidade de volume. Essa concentrao expressa com exatido (quatro decimais) ex.: 0,1538 g/L (massa/volume) 0,8543 mol/L (nmero de mols/volume) b) solues no padronizadas: usadas para fins no analticos sendo sua concentrao aproximada. No requerida a mesma exatido, com relao s solues padronizadas (um ou dois decimais) ex.: 0,5 g/L (massa/volume) 1,0 mol/L (nmero de mols/volume) O ttulo das solues padro deve ser conhecido com grande exatido. O grau de exatido requerido maior do que o correspondente aos trabalhos analticos mais comuns. Assim sendo desejvel que o ttulo das solues padro possa ser determinado com um erro inferior a 0,1 %. Maiores detalhes sero tratados nas disciplinas de Qumica Analtica Quantitativa. A preparao de uma soluo padro requer, direta ou indiretamente, o uso de um reagente quimicamente puro e com composio perfeitamente definida. Os reagentes com semelhantes caractersticas so denominados, comumente, padres primrios. So os seguintes os requisitos principais exigidos de um padro primrio: a) a substncia deve ser de fcil obteno, purificao, dessecao e conservao; b) no pode ser voltil; c) as impurezas devem ser facilmente identificveis com ensaios qualitativos de sensibilidade conhecida; d) a substncia no deve ser higroscpica (absorver umidade do ambiente) ou eflorescente; e) deve ser bastante solvel. O nmero de padres primrios relativamente limitado. So exemplos: carbonato de clcio, tetraborato de sdio, cido benzico, cloreto de sdio (aps dessecao a peso constante), nitrato de prata, tiocianato de potssio, cido oxlico, oxalato de sdio e dicromato de potssio.
Quando o reagente com que se tem de preparar a soluo um padro primrio, recorre-se a tcnica direta que consiste na pesagem, em balana analtica, da massa que se requer da substncia, dissoluo e diluio a um volume conhecido em balo volumtrico aferido. No rtulo dever constar a espcie qumica, seu ttulo, a data de praparao e seu preparador, conforme modelo. Embora o Sistema Internacional de unidades recomende para o volume a unidade metro cbico utilizamos o volume expresso em litro (L). As ilustraes a seguir indicam alguns dos equipamentos utilizados na titulaes (bureta, pipeta volumtrica, erlenmeyer,...) a tcnica correta de leitura, de transferncia de alquotas com a pipeta volumtrica e transferncia de soluo para o balo volumtrico. Leitura correta da bureta Transferncia de soluo
Transferncia de lquido para o balo
Como rotular a soluo !
FACULDADE DE QUMICA PUCRS
HCl M = 0, 2574 mol/ L
Linus Pauling 06/06/1966 Qumica Geral e Inorgnica II
Quando o reagente no padro primrio (por exemplo, o cido clordrico, os hidrxidos alcalinos e de amnio, o permanganato de potssio,...) a preparao direta da soluo no possvel. Recorre-se, ento, tcnica indireta, que consiste em preparar, inicialmente, uma soluo com concentrao aproximada desejada e, depois, padroniz-la, isto , determinar com exatido o sei ttulo em relao a um padro primrio adequado ou com referncia a uma outra soluo padro. Por exemplo, o cido clordrico no padro primrio e a sua soluo pode padronizada atravs de um padro primrio, como o caso do carbonato de sdio. A seguir esta soluo (j padronizada) pode ser usada para titular hidrxidos alcalinos (como por exemplo o hidrxido de sdio). Na padronizao devem ser obedecidas as seguintes condies: a) preciso dispor de um padro primrio adequado ou soluo padronizada; b) o peso do padro primrio no pode ser demasiadamente pequeno, em virtude do erro inerente ao aparelho de pesagem; c) o volume de soluo gasto na padronizao no deve ser pequeno demais, pois cada leitura na bureta est sujeita a um erro de 0,01 mL e um erro de escoamento de 0,02 mL, podendo o erro total chegar a 0,04 mL e, portanto, para garantir uma exatido de 0,1% preciso que o volume de soluo gasto na titulao no seja inferior a 40 mL. *** Obs.: como o objetivo em nossa disciplina no esgotar o assunto e sim mostrar caractersticas principais no prepa ro de solues, eventualmente o critrio acima poder no ser verificado !!! 1.2.4. Conservao das Solues Padro Como j afirmamos anteriormente as solues no so conservadas em bales volumtricos (so usados somente na preparao). As solues padro devem ser conservadas de maneira a manter inalterado seu ttulo tanto quanto possvel. Algumas solues so altamente estveis e outras no. Por exemplo, uma soluo 0,1 eqg/L de dicromato de potssio indefinidamente estvel. As solues de cido clordrico, ntrico e hidrxido de amnio, por serem estes solutos volteis, tem durao limitada. As solues de hidrxidos alcalinos reagem com o CO2 presente no ar formando carbonatos. Estes carbonatos solidificam no gargalo dos frascos de depsito e se os mesmos tiverem tampas de vidro esmerilhado, a presena de carbonatos ir emperrar as referidas tampas, sendo aconselhvel o uso de tampas com rolha de borracha ou polietileno ou rosqueadas. Aconselha-se o frasco escuro para evitar a decomposio fotoqumica, o que ocorre com facilidade em solues de perxido de hidrognio e permanganato de potssio.
10
1 .3 . Pr i n c i p a i s Ex p r e s s e s d e Co n c e n t r a o
A concentrao de uma soluo representa uma relao entre a quantidade do soluto e, em geral, a quantidade de soluo sendo que essas quantidades podem ser expressas em massa, nmero de mols, volume, nmero de molculas, etc. As principais formas de representar as concentraes so do tipo massa/volume, massa/massa, volume/volume, nmero de mols/volume, nmero de mols/massa e, assim, por diante. Assim, quando analisamos a composio de uma gua mineral, a qual expressa a quantidade de um constituinte, por exemplo Carbonato de sdio = 127 mg / L nos indica uma relao massa / volume. J na composio do soro fisiolgico, usado para limpeza e conservao de lentes de contato, a composio indica 0,9 % de NaCl. Isso significa uma relao massa / massa onde h, para cada 100 gramas de soluo, 0,9 gramas do soluto (NaCl) sendo o restante 99,1 gramas de solvente (gua). Nesse caso, especificamente, como se trata de uma soluo muito diluda e aquosa o mesmo valor percentual massa / massa tambm corresponde, aproximadamente, ao valor da relao massa / volume, em virtude da massa especfica do solvente (gua) ser unitrio (1,0 grama / mL). 1.3.1. Concentrao Comum ou Concentrao ( C ) Representa a razo entre a massa do soluto (em gramas) e o volume de soluo final (em litros).
C=
Aplicao Que massa de bicarbonato de sdio h em 750 mL de uma soluo que apresenta uma concentrao de 107 mg / L ? 1.3.2. Concentrao em Massa ou Ttulo em Massa ou Ttulo ( t )
m V
( Unidades: gramas/litro )
Representa a razo entre a massa do soluto (gramas) e a massa da soluo (gramas).
m= m m m +m
1 1 1
( no tem unidades = adimensional )
2
comum expressar o Ttulo em Massa sob a forma percentual. Assim
11
t%
t . 100
Aplicao Uma soluo aquosa de cido sulfrico apresenta Ttulo percentual 15 %. Que massa dessa substncia h em quilograma dessa soluo ? Qual a massa de solvente presente ? 1.3.3. Relao entre C e Lembrando que:
C=
m V
m= m m m +m
1 1 1
dividindo uma expresso pela outra resulta: que simplificando torna-se ou, ento
C/t = m/ V =
C / t = m1/ V C =m
m (massa especfica) .t
/ m1/m
Usualmente expressa- se a massa especfica (ou densidade absoluta) em grama / cm3 ou grama / mL e a Concentrao em grama / litro. Portanto para que a expresso acima represente Concentrao a mesma dever ser multiplicada pelo fator de converso 1000 mL / L, na forma
C =m
. t . 1000 (mL/L)
e dessa forma a Concentrao ter como unidade resultante grama / litro. 1.3.4. Concentrao em Volume ou Ttulo em Volume (t v )
Representa a razo entre o volume de solvente e o volume de soluo. Historicamente essa forma de concentrao tem sido expressa como o G L (graus Gay-Lussac) utilizada para representar a percentagem volumtrica de etanol em bebidas alcolicas.
tv
= V1 / V = V1 / V1 + V2
(adimensional)
Aplicao Que volume de etanol h numa garrafa de 750 cm3 de Jack Daniels ?
12
1.3.5. Concentrao em partes por milho (ppm) Corresponde a uma forma de Concentrao Comum (gramas/litro) aplicada para solues muito diludas, em geral aquosas, cujo significado equivale a 1 grama de soluto para cada 106 gramas de soluo. Assim uma soluo, na qual a quantidade de soluto seja de 15 ppm significa que h 15 gramas da substncia para cada 106 gramas de soluo. Demonstre que: 1 ppm = 1 mg / litro !!! 1.3.6. Concentrao em frao molar ( x1 ) Corresponde a razo entre o nmero de mols de um componente qualquer e o nmero de mols total da mistura. Essa expresso de concentrao muito utilizada para misturas de gases como, por exemplo, para definir a composio da atmosfera. Assim X1 =
n n +n +n
1 1 2
=
3
n n
onde n1 =
m M
1 1
( X1 = adimensional )
Aplicao Uma soluo aquosa de NaOH tem frao molar 0,15 . Qual seu Ttulo em massa ? 1.3.7. Concentrao em Quantidade de Matria ou em Molaridade ( M ) Corresponde razo entre o nmero de mols do soluto e o volume total da soluo. M =
n V
m M .V
1 1
C M
m.t .1000 M
1
( Unidade: mol / L = molar = M)
A expresso de concentrao expressa em molaridade a mais empregada dentre todas as formas usadas na Qumica. Aplicao A soluo dos lquidos de baterias de automveis consiste de gua e cido sulfrico em concentrao 3,95 mol / litro, aproximadamente. Sabendo que numa bateria comum a quantidade de soluo de 800 mL, que massa desse cido estar ali contida ?
13
1.3.8. Concentrao em Molalidade ( W )
W = weight = peso
Corresponde razo entre o nmero de mols do soluto e a massa, em quiligramas, de solvente. Observe que a molalidade a nica expresso de concentrao que relaciona a quantidade de soluto com a quantidade de solvente e no de soluo. W=
em quilo
n m
1 2
m M .m
1 1
=
2
em quilo
m .1000 Mm
1 1 2
( Unidades: mol/quilo ou molal)
em grama
Na ltima expresso o valor numrico 1000 na realidade corresponde ao fator de correo 1000 g / quilograma, quando a massa do solvente for dada em grama. A concentrao expressa em Molalidade comumente empregada no estudo dos efeitos coligativos das solues. Aplicao Uma soluo de cido sulfrico apresenta ttulo em massa igual a 15 %. Qual a sua Molalidade ? Para solues aquosas diludas J ust if ique !!!
M = W
1.3.9. Concentrao para espcies inicas Como podemos determinar as concentraes molares dos ons Na+ e SO4-2 para uma soluo de concentrao 27,2 gramas / Litro desse sal ? Idem para as concentraes dos ons H+ e SO4-2, numa soluo 0,75 mol / L desse cido, supondo um grau de dissociao (a) igual a 85 % do cido ?
14
1 .4 . Di l u i o e M i s t u r a s d e So l u e s
1) Diluio: diluir uma soluo consiste em adicionar solvente, sem modificar a quantidade de soluto.
+ Vgua
Soluo inicial
Soluo final
m1, V, C m1= C.V
+ Vgua
m1, V , C
m1= C . V
Como a massa do soluto a mesma, conclui-se que:
C . V = C . V
De modo semelhante, pode ser demonstrado que:
t.m
M . V = M . V
t . m
Na Concentrao de uma soluo o solvente removido por evaporao, mantendo constante a quantidade de soluto. As expresses so as mesmas da Diluio. A diferena ocorre no volume final:
Diluio: Concentrao:
V > V V < V
; ;
V = V + Vgua V = V - Vgua
2) Mistura (mesmo soluto): na mistura de solues do mesmo soluto no h reao entre as solues misturas.
15
(1)
(2)
(3)
+
Soluo 1 + Soluo 2
Soluo final
A massa de soluto na soluo final a soma das massas nas solues 1 e 2, portanto:
m1 + m1 = m1 logo:
C.V + C .V = C .V
De modo semelhante pode ser demonstrado que:
M . V + M . V = M . V t . m + t . m = t . m
A relao anterior pode ser aplicada para uma mistura de qualquer nmero de solues. Generalizando:
Cx . Vx = S C . V M x . Vx = S M . V tx . mx = S t . m
m1, V , C m1= C.V
m1 , V , C m1 = C .V
m1 , V , C m1 = C .V
16
3) Mistura (solutos diferentes): neste caso ocorre reao entre os constituntes. ex.: soluo de HCl misturada com soluo de NaOH. Neste caso, para que a reao seja completa entre os solutos os volumes misturados devem obedecer relao estequiomtrica corresponde reao. HCl 1 mol + NaOH 1 mol NaCl 1 mol + H2O 1 mol
Portanto, no ponto final dessa reao:
ncido = nbase
M a . Va = M b . Vb
ex.: soluo de H3PO4 misturada com soluo de NaOH. H3PO4 1 mol + 3 NaOH 3 mols Na3PO4 1 mol + 3 H2O 3 mols
No ponto final dessa reao:
nbase = 3 ncido
M b . Vb = 3 M a . Va
ex.: soluo de H2SO4 misturada com soluo de KOH. H2SO4 1 mol + 2 KOH 2 mols K2SO4 1 mol + 2 H2O 2 mols
No ponto final dessa reao:
nbase = 2 ncido
M b . Vb = 2 M a . Va
O principio acima descrito consiste de um mtodo volumtrico de determinao da concentrao de bases atravs do volume gasto de cido, de molaridade conhecida e vice-versa. Este processo denominado Titulao ou Padronizao. O ponto final das reaes de neutralizao pode ser visualizado atravs da adio de indicadores cido-base (fenolftalena, tornassol, azul de bromo timol, ...) Este principio no vlido somente para reaes cido-base, mas para qualquer tipo de reao, desde que se conhea a equao qumica correspondente e seu respectivo ajuste (coeficientes).
17
A figura ao lado mostra como pode ser determinada a concentrao de uma soluo usando-se a sua reao com outra, de molaridade conhecida. Na bureta coloca-se a soluo de concentrao conhecida, a qual adicionada a uma alquota (poro) de soluo de concentrao a determinar (em geral 25 mL). No ponto final da reao o indicar muda de colorao e pelo volume gasto na bureta podemos estabelecer as quantidades , em mols, que reagiram entre s, atravs das expresses acima mencionadas.
1 .5 . Ex e r c c i o s
1.5.1. Propriedades dos lquidos. 1) Em funo das foras interativas moleculares como se pode explicar: 1.1. a elevada tenso superficial da gua. 1.2. a dilatao anormal (anmala) do gelo. 2) Como toda a criana, voc, provavelmente, j deve ter enchido um copo acima da sua borda. Como se explica o fato do mesmo no transbordar? 3) A acetona (CH3COCH3) um lquido muito mais voltil do que a gua, fato esse comprovado pelo seu ponto de ebulio ser bastante inferior (53,6o C). Como esse fenmeno pode ser explicado ? 4) Porque a gua quente evapora mais rapidamente do que a gua fria ? 5) A miscibilidade (solubilidade) do etanol (CH3CH2OH) infinita, em gua. A solubilidade decorrente de foras atrativas entre as molculas das substncias envolvidas. Nesse caso qual o tipo de fora atrativa ? 6) Valendo-se de qualquer bibliografia de Qumica Geral, investigue a respeito do diagrama de fases da gua pura bem como do significado do ponto triplo da gua.
18
7) A solubilidade de gases em lquidos no mostra o mesmo comportamento do que a dos slidos. Varia diretamente com a presso (Lei de Henry) e inversamente com a temperatura. Em funo disso explique porque os peixes procuram os lugares mais profundos e sombrios durante as tardes de vero ? 8) O que ocasiona a descompressoem mergulhadores ? 1.5.2. Preparao de solues 1) Na preparao de uma soluo, quando que um soluto pode ser considerado um padro primrio ? 2) Enumere algumas caractersticas de um padro secundrio, citando, pelo menos, 5 exemplos de solutos que mostrem essas caractersticas ? 3) Porque as solues, mesmo as de padres secundrios, devem ser preparadas em bales volumtricos e no em bequer graduado ? 4) Investigue a respeito de duas solues que devem ser obrigatoriamente conservadas em frasco escuro, ao abrigo da luz, justificando tal procedimento em cada caso. 5) Qual a diferena entre uma pipeta graduada e uma pipeta volumtrica, ambas de mesma capacidade ? 1.5.3. Concentrao das solues 1) Procure estabelecer o significado para as expresses de concentrao encontradas em algumas solues de nosso cotidiano: Soro fisiolgico : NaCl a 0,9 % gua oxigenada a 10 volumes Graduao alcolica do conhaque 380 GL. 2) Sabendo-se que a solubilidade do NaCl, a 100o C de 39,0 g/100 g de gua e, a 20o C de 36,0 g/100 g de gua, calcule qual a massa de gua necessria para dissolver 780 g de NaCl 100o C e qual a massa de NaCl que permanecer dissolvida quando essa soluo for resfriada at 20o C ? Resposta: mgua = 2000 g ; mNaCl = 720,0 g 3) A frao molar do cido sulfrico 0,10, numa soluo aquosa. Qual a Concentrao em massa (Ttulo) da mesma ? Resposta: 37,6 %
19
4) O lcool hidratado usado como combustvel apresenta em mdia cerca de 3,7 % em massa de gua dissolvida no lcool. Qual o valor da frao molar do soluto nessa soluo ? Resposta: 0,089 5) O cido sulfrico para acumuladores (baterias) de automveis tem 32 % em massa de cido; o resto gua. A massa especfica dessa soluo 1,2 g/mL. Qual a Molaridade de cido sulfrico na soluo ? Resposta: 4,0 mol/L 6) Formalina uma soluo para preservao usada em biologia. Ela contm 40 cm3 de formaldedo (H-CHO), massa especfica 0,82 g/cm3, por 100 gramas de gua. Qual a Molalidade dessa soluo ? Resposta: 10,93 mol/kg de gua 7) A graduao alcolica do whiskey bourbon (destilado de malte e milho), produzido, principalmente, nos estados do Tenessee e Kentucky (USA), corresponde ao dobro da porcentagem em volume de lcool (C2H5OH). Para uma graduao 120 do whiskey bourbon, qual a molalidade do lcool etlico ? (massa especfica do etanol = 0,80 g/mL) Resposta: 26,08 mol/kg 8) Qual a massa de cloreto de clcio (CaCl2) que deve ser dissolvida em 400 gramas de gua para produzir uma soluo de ttulo 20% ? Resposta: 100 g 9) O bactericida permanganato de potssio, KmnO4, pode ser usado em gua dissolvido na proporo em massa de 1 : 40.000. Que volume de gua ser necessrio dissolver 1 comprimido de 0,1 gramas de permanganato para produzir a soluo acima ? Resposta: 4 l de gua 10) Em mdia, as cervejas apresentam teor alcolico (etanol) de 4% (40 GL). Qual o volume, em litros, de etanol, existente num tonel de 10.000 L de cerveja ? Resposta: 400 mL 11) Uma soluo cuja densidade 1,15 g/mL foi preparada dissolvendo-se 160 g de NaOH em 760 mL de gua. Determine a massa e o volume da soluo obtida. Respostas: m = 920 gramas ; V = 0,8 L 12) Segundo os padres modernos de controle ambiental, uma gua natural de superfcie no pode conter mais de 0,78 mg de cromo por litro. Qual a concentrao limite para o cromo em mol/L ? Resposta: 1,5 . 10-5 mol/L
20
13) O rtulo de uma soluo de cido clordrico comercial indica HCl 37,4 % em peso e massa especfica 1,18 g/mL. Qual a molaridade do HCl nessa soluo? Resposta: 12 mol/L 14) Um mL de soluo 1,0 M de cido clordrico equivale a 20 gotas. Qual o nmero de mols de HCl presentes em 1,0 gota ? Resposta: 5,0 . 10-5 mol 15) Certa massa de sulfato frrico foi dissolvida para perfazer 1,0 litro de soluo. O nmero total de partculas dispersas na soluo, considerando o soluto totalmente dissociado, foi igual a 6,02 . 1022 (0,1 N0). Qual a Molaridade da soluo em funo do Fe2(SO4)3 ? Resposta: 2,0 . 10-2 mol/L 16) A soluo aquosa de cloreto de sdio, vendida no comrcio e usada como colrio ou para limpar lentes de contato, apresenta Ttulo igual a 0,9 %. Qual a massa de NaCl contida em 1,0 litro dessa soluo ? Resposta: 9,0 gramas 17) Um analgsico em gotas deve ser ministrado em quantidade de 3 mg por quilograma de massa corporal, no podendo, entretanto, exceder a 200 mg por dose. Sabendo-se que cada gota contm cerca de 5 mg do analgsico, quantas gotas devero ser ministradas a um paciente de 70 quilogramas ? Resposta: 40 gotas 18) O rtulo de uma gua mineral distribuda para o consumo informa que ela contm principalmente 696,35 mg de bicarbonato de sdio (NaHCO3), alm de outros componentes. Qual a concentrao do bicarbonato de sdio, expressa em mol/litro dessa gua mineral ? Resposta: 0,008 mol/L 19) Uma soluo de Cr2(SO4)3, apresenta uma concentrao de 0,2 mol/L. Supondo o sal totalmente dissociado, qual a molaridade em relao aos ons presentes ? Respostas: Cromo = 0,4 mol/L ; Sulfato = 0,6 mol/L 20) A gua potvel pode ter no mximo 1,0 ppm de chumbo. Qual a maior massa de chumbo que pode existir em 0,50 L de gua potvel ? Resposta: 5,0 . 10-4 gramas
21
1.5.4. Diluio e Misturas de Solues * Diluio 1) A 50 gramas de uma soluo de cido sulfrico de 63% em massa so adicionados 400 g de gua. Qual a porcentagem de cido na soluo diluda obtida ? Resposta: 7 % 2) Que volume de gua, em mL, deve ser adicionado a 80 mL de soluo aquosa 0,1 M de uria, para que a soluo resultante seja 0,08 M ? Resposta: 20 mL 3) Que volume de cido sulfrico 20% em massa e densidade 1,139 g/mL necessrio para preparar 50 mL de soluo a 5% em massa e densidade 1,032 g/mL ? Resposta: 3,40 mL 4) Que volume de cido clordrico 0,25 mol/L poderemos obter pela diluio de 50 mL de HCl de massa especfica 1,185g/mL e que apresenta 36,5 de cido clordrico, em massa ? Resposta: 2,37 L 5) Foi adicionado certo volume de gua a 100 mL de soluo 1,0 M de NaOH, de modo que a sua concentrao ficou reduzida a 1/5 do valor inicial. Qual o volume de gua adicionado ? Resposta: 400 mL * Mistura de Solues 1) Misturando-se 280 mL de uma soluo 1/2 M de HCl com 200 mL de uma segunda soluo do mesmo cido contendo 14,6 g de HCl puro num volume de 500 mL, qual a Molaridade resultante ? Resposta: 0,625 mol/L 2) Misturando-se 250 mL de cido fosfrico, com massa especfica 1,12 g/mL, que contm 24,5% em massa de H3PO4, com 1/2 L de soluo 0,2 mol/L do mesmo cido, qual a Molaridade resultante ? Resposta: 1,06 mol/L 3) Uma soluo aquosa 2 M de NaCl, de volume 50 mL, foi misturada a 100 mL de outra soluo do mesmo sal, de molaridade 0,5 M. Qual a molaridade da mistura resultante ? Resposta: 1,0 mol/L
22
4) Volumes iguais de duas solues aquosas de NaOH de molaridades iguais a 0,4 e 0,8 mol/L, respectivamente, foram misturados e deram origem a uma nova soluo. Qual a molaridade e a concentrao em g/L dessa nova soluo ? Respostas: 0,6 mol/L ; 24,0 g/L 5) Em um balo volumtrico de 1000 mL juntaram-se 250 mL de uma soluo 2,0 M de cido sulfrico com 300 mL de soluo 1,0 M do mesmo cido e completou-se o volume at 1000 mL, com gua destilada. Qual a Molaridade da soluo resultante ? Resposta: 0,80 mol/L 1.5.5. Solues que Reagem entre si 1) Uma remessa de soda custica est sob suspeita de estar adulterada. Dispondo de uma amostra de 0,5 gramas, foi preparada uma soluo aquosa de 50 mL. Essa soluo foi titulada sendo consumidos 20 mL de uma soluo 0,25 M de cido sulfrico. Qual a percentagem de impurezas da amostra de soda, considerando-se que o cido no reage com as impurezas. Resposta: 20 % 2) Juntou-se 300 mL de soluo HCl 0,4 mol/L 200 mL de NaOH 0,8 mol/L. A soluo resultante ser cida, bsica ou neutra ? (a) Qual a Molaridade em relao ao reagente em excesso ? (b) Qual a Molaridade em relao ao sal formado ? Respostas: a soluo resultante ser bsica; (a) 0,08 mol/L ; (b) 0,24 mol/L 3) 100 mL de soluo de cido sulfrico 0,1 mol/L so adicionados a 500 mL de NaOH 0,5 mol/L. Para que valor ficar reduzida a molaridade da soluo bsica? 4) 30 mL de uma soluo de H2SO4 quando misturados com uma soluo de BaCl2 produzem uma precipitado branco (sulfato de brio) que, lavado e seco pesou 0,466 gramas. Qual a Molaridade da soluo cida ? Resposta: 0,065 mol/L 5) Uma indstria adquiriu hidrxido de sdio como matria-prima para a fabricao de sabo, a qual apresentava impurezas inertes ao HCl. Certa amostra de 3,0 gramas da base foi completamente neutralizada por 20 mL de HCl 3,0 mol/L. Determine (a) a percentagem de pureza da base e (b) a massa de material necessrio para a preparao de 1,0 L de soluo 1,0 mol/L ? Respostas: (a) 80 % ; (b) 50 g
23
*** Testes de nivelamento (no sero corrigidos ou comentados) 1 - O limite mximo de ingesto diria aceitvel (IDA) de cido fosfrico, usado como aditivo em alimento, de 5 mg/kg de peso corporal. O volume de refrigerante, em litros, contendo cido fosfrico na concentrao de 588 mg/L que uma criana de 20 kg pode ingerir para atingir o limite mximo de IDA A) 0,10 B) 0,17 C) 0,25 D) 0,50 E) 1,00 2 - Um laboratorista possui um frasco contendo 200 mL de uma soluo 0,4 M de cido ntrico. Para prosseguir em sua anlise, ele necessita de uma soluo 0,1 M do mesmo cido. O volume de gua, em mililitros, que deve adicionar a sua soluo cida para obter a soluo de concentrao desejada A) 100 B) 400 C) 500 D) 600 E) 800 3 - Para neutralizar, exatamente, uma certa quantidade de um monocido, foram gastos 4,0 g de NaOH quimicamente puro. O mesmo efeito seria obtido pelo emprego de A) 2,9 g de hidrxido de magnsio. B) 4,0 g de hidrxido de potssio. C) 5,8 g de cloreto de sdio. D) 7,4 g de hidrxido de clcio. E) 34,2 g de hidrxido de brio. 4 - Foi mergulhado 1,116 g de esponja de ferro (bombril) em 500 mL de uma soluo 0,1 M de CuSO4. Pode-se afirmar que ao final do processo A) praticamente todos os ons Cu++ foram consumidos, sobrando ainda ferro. B) todo o ferro foi consumido, sobrando ons Cu++ em soluo. C) todo o ferro foi oxidado a ons frrico e todos os ons Cu++ foram reduzidos a Cu0. D) a concentrao de ons cprico era igual de ons frrico. no sobrando mais esponja de ferro. E) nada pde ser observado, pois o on Cu++ no oxida o ferro. 5 - Para neutralizar uma soluo de cido ntrico, contendo 12,6 g do cido em 500 mL de soluo, o volume necessrio de soluo de hidrxido de sdio 1,0 M A) 2 mL B) 125 mL C) 200 mL D) 1250 mL E) 2000 mL
24
6 - Misturam-se volumes iguais de duas solues A e B de NaOH, de concentrao 1,0 mol/L e 2 mols/L, respectivamente, resultando uma soluo C. Adicionando-se 200 mL de gua soluo C, obtm-se a soluo D. Sobre essas solues pode-se afirmar que A) C e D apresentam diferentes quantidades de soluto. B) B e D tem concentraes iguais. C) a concentrao de C 1,5 mols/L e a de D maior do que 1,5 mols/L. D) a concentrao de C 1,5 mols/L e a de D menor que 1,5 mols/L. E) A e B apresentam a mesma quantidade de soluto. 7 - Para preparar uma soluo de hidrxido de sdio 2 M, deve-se A) diluir, aproximadamente, 33 mL de soluo de hidrxido de sdio 6 M com gua e completar a 100 mL. B) diluir, aproximadamente, 50 mL de soluo de hidrxido de sdio 3 M com gua e completar a 100 mL. C) dissolver 100 g de hidrxido de sdio puro em gua e completar a 1,0 litro. D) dissolver 60 g de hidrxido de sdio puro em gua e completar a 250 mL. E) dissolver 4 g de hidrxido de sdio puro em gua e completar a 100 mL. 8 - O vinagre uma soluo aquosa de cido actico. Qual a concentrao de cido no vinagre se foram gastos 30 mL de uma soluo de NaOH 0,2 M para titular 20 mL de vinagre? A) 0,2 mols/L. B) 0,3 mols/L. C) 0,3 mols/mL. D) 0,4 mols/mL. E) 0,4 mols/L. 9 - Necessita-se preparar uma soluo 0,02 M de NaCl, partindo-se de 20 mL de uma soluo 0,1 M do mesmo sal. O volume de gua, em mL, que deve ser adicionado para obter-se a soluo com a concentrao desejada A) 25 B) 40 C) 65 D) 80 E) 100 10 - Uma soluo aquosa de cido sulfrico, para ser utilizada em baterias de chumbo de veculos automotivos, deve apresentar concentrao igual a 4,0 mol/L. O volume total, em litros, de uma soluo adequada para se utilizar nestas baterias, que pode ser obtido a partir de 500 mL de soluo de cido sulfrico de concentrao 18 mol/L, igual a A) 0,50 B) 2,00 C) 2,25 D) 4,50 E) 9,00 11 - 50 mL de uma soluo 0,2 M de NaOH seriam completamente neutralizados com A) 20 mL de H2SO4 0,1 M B) 25 mL de H2SO4 0,2 M C) 25 mL de HNO3 0,2 M D) 25 mL de HCl 0,1 M E) 50 mL de HCl 0,1 M
25
12 - O volume, em mililitros, de soluo de cido clordrico a 37% em massa de densidade igual a 1,9 g/mL necessrio para preparar 10,0 litros de soluo 0,4 mol/L , aproximadamente A) 50 B) 78 C) 146 D) 208 E) 2.000 13 - O suco gstrico produzido pelo estmago durante o processo da digesto apresenta cido clordrico numa concentrao molar de 1,0 . l0-2 mol/L. Sabendose que durante a digesto so produzidos cerca de 100 mL de suco gstrico, qual a massa, expressa em gramas, de cido contido nesse volume ? A) 73,0. B) 36,5. C) 3,65. D) 0,0365. E) 0,073. 14 - O soro caseiro recomendado para evitar a desidratao infantil consiste de uma soluo aquosa de cloreto de sdio, 3,5 g/L, e de sacarose 11,0 g/L. A concentrao, em mol/L, do cloreto de sdio nessa soluo e, aproximadamente A) 0,03. B) 0,04. C) 0,06. D) 0,10. E) 0,15. 15 - Um aluno do curso de Qumica necessita preparar uma soluo 0,20 M em NaOH para ser utilizada em uma reao de neutralizao. A forma correta de preparao dessa soluo seria dissolver _______g de NaOH em ______ L de soluo. A) 2,0 0,50 B) 4,0 0,25 C) 4,0 0,50 D) 8,0 0,75 E) 8,0 1,50 16 - Foram adicionados 35,00 mL de gua destilada a 15,00 mL de uma soluo 0,50 M em KMnO4 . A molaridade desta nova soluo A) 0,050. B) 0,075. C) 0,100. D) 0,150. E) 0,175.
26
17 - Um tcnico necessita preparar uma soluo aquosa de hipoclorito de sdio, NaClO, 0,5 M, para o branqueamento de um tecido de algodo. No laboratrio foram encontrados somente 10,0 gramas do soluto e, portanto, o volume, em litros, de soluo obtida com a molaridade desejada de, aproximadamente, A) 0,27. B) 0,50. C) 2,70. D) 3,70. E) 5,00. 18 - Necessita-se preparar uma soluo de fluoreto de sdio de concentrao igual a 12,6 g/L, aproveitando 200 mL de uma soluo 0,9 M do mesmo sal. Para isso deve se adicionar A) 400 mL de gua. B) 600 mL de gua. C) 200 mL de gua. D) 0,3 mols do sal. E) 6,3 g do sal. 19 - Soluo salina normal uma soluo aquosa de cloreto de sdio, usada em medicina porque a sua composio coincide com aquela dos fludos do organismo. Sabendo-se que foi preparada pela dissoluo de 0,9 g do sal em 100 mL de soluo, podemos afirmar que a molaridade da soluo e, aproximadamente, A) 1,25. B) 0,50. C) 0,45. D) 0,30. E) 0,15. 20 - O Conselho Nacional do Meio Ambiente (CONAMA), atravs da resoluo no 20 de 18 de Junho de 1986, apresenta como limite para o cromo trivalente em efluentes lquidos, 2 ppm, ou seja, 2 mg de Cr+3 por litro de efluente. A concentrao aproximada, em mols/L, desse metal A) 1,8 . 10-3. B) 3,8 . 10-5. C) 5,9 . 10-7. D) 7,6 . 10-3. E) 9,1 . 10-5. 21 - O soro fisiolgico uma soluo de cloreto de sdio a 0,9 %. A quantidade aproximada, em mol(s) de cloreto de sdio consumidos por um paciente que recebeu 1.500 mL de soro fisiolgico A) 0,12. B) 0,23. C) 0,46. D) 1,35.
27
E) 13,5. 22 - 50,00 mL de uma soluo 2,0 mols/L de MgCl2 so diludos a 1,0 litro. A concentrao, em mol/L, de ons cloreto na nova soluo A) 0,1. B) 0,2. C) 1,0. D) 2,0. E) 4,0. 23 - O cido sulfrico concentrado um lquido incolor, oleoso, muito corrosivo, oxidante e desidratante. No almoxarifado de um laboatrio h disponvel o cido sulfrico de densidade 1,8 g/mL, contendo 90% de H2SO4, em massa. A massa de cido sulfrico presente em 100 mL desse cido concentrado A) 1,62 g. B) 32,4 g. C) 162 g. D) 324 g. E) 1620 g. 24 - Uma soluo de cido ascrbico (vitamina C), de frmula C6H8O6, foi preparada pela dissoluo de 17,6 g em gua suficiente para obter-se 2,0 litros de soluo. correto afirmar que, nesta soluo, A) a concentrao de 0,10 mol/L. B) em 10 mL esto contidos 5 . 10-4 mols do cido. C) para neutralizar 0,5 litros dessa soluo, seria necessrio 1,0 g de cloreto de amnio. D) adicionando mais 0,5 L de gua, a concentrao passaria para 0,4 molar. E) evaporando-se parte do solvente, de forma que o volume fosse reduzido para 0,5 L, a concentrao ficaria igual a 0,02 molar. 25 - Um qumico preparou uma soluo contendo os seguintes sais, com suas respectivas concentraes em mols/L: cloreto de potssio 0,10, cloreto de magnsio 0,20 e cloreto de cromo III 0,05. A concentrao de ons cloreto, em mol/L, nessa soluo A) 0,35. B) 045. C) 0,55. D) 0,65. E) 0,75. 26 - A adio de 90 mL de gua destilada a 10 mL de uma soluo contendo KCl e MgCl2 em concentraes iguais a 1,0 mol/L e 0,50 mol/L, respectivamente, resulta numa mistura na qual A) a concentrao de on cloreto 1,5 mol/L. B) a concentrao do ction magnsio e a de nio cloreto so, respectivamente, de 0,05 mol/l e 0,20 mol/L.
28
C) a concentrao de ction potssio e a de nio cloreto so iguais a 0,10 mol/L. D) a concentrao de ction potssio e a de ction magnsio so, respectivamente, de 0,90 mol/L e de 0,45 mol/L. E) a concentrao de ction magnsio, a de nion cloreto e a de ction potssio so iguais. 27 - Dissolveram-se 8 gramas de NaOH em uma quantidade de gua suficiente para preparar 200 mL de soluo. Indique o volume de soluo assim preparada que ser necessrio para neutralizar 50 mL de uma soluo de HNO3 0,1 mol/L. A) 1 mL. B) 5 mL. C) 10 mL. D) 25 mL. E) 50 mL. 28 - Um aditivo para radiadores de automveis composto de uma soluo aquosa de etilenoglicol. Sabendo que em um frasco de 500 mL dessa soluo existem 5 mols de etilenoglicol (C2H6O2), a concentrao comum dessa soluo, em g/L , A) 0,010. B) 0,62. C) 3,1. D) 310. E) 620. 29 - Em uma determinada amostra contendo cido palmtico gastou-se 4m,0 mL de NaOH 0,250 mol/L para neutraliz-lo. Dados: cido palmtico = CH3(CH2)14COOH Massa molecular = 256,00 u A quantidade, em gramas, de cido encontrada de A) 0,13 B) 0,26 C) 1,28 D) 2,56 E) 6,40 30 - Solues de uria, (NH2)2CO, podem ser utilizadas como fertilizantes. Uma soluo foi obtida pela mistura de 210 g de uria e 1000 g de gua. A densidade da soluo final 1,05 g/mL. A concentrao da soluo em percentual de massa de uria e em mol/L, respectivamente,
A) B) C) D) E) Percentagem em massa 17,4% 17,4% 20,0% 21,0% 21,0% Concentrao em mol/L 3,04 3,50 3,33 3,04 3,50
29
2 . EFEI T OS COL I GA T I V OS
Os Efeitos ou Propriedades Coligativas so modificaes produzidas em determinadas propriedades fsicas dos solventes quando neles dissolvemos solutos no volteis. Estas propriedades modificadas so: tenso ou presso de vapor, ponto de ebulio, ponto de congelamento e presso osmtica. Estas modificaes s dependem do nmero de partculas dissolvidas e no de sua natureza, isto : - um mol de molculas de glicose (C6H12O6) exerce o mesmo efeito que um mol de ons cloreto (Cl-) ou um mol de ons sdio (Na+). Estes efeitos so explicados pela intensificao das foras interativas moleculares, que modificam as energias envolvidas nos processos de evaporao, ebulio e congelamento das solues e, tambm, pela modificao da relao entre o nmero de partculas do soluto e solvente, na interface de separao lquido-vapor. 1) Efeito Tonomtrico ou Tonometria: mede o abaixamento relativo da presso de vapor do solvente, quando nele dissolvemos um soluto no-voltil. A presso de vapor pode ser entendida como aquela exercida pelas molculas do lquido em seu movimento espontnea e catico, contra a interface de separao lquido-vapor.
30
A presso de vapor depende da temperatura e do tipo de solvente. O quadro da pgina anterior mostra os valores das presses de vapor para diferentes tipos de lquidos, na temperatura de 25oC, tomando-se como referncia a presso atmosfrica normal. No grfico seguinte observa-se a variao da presso de vapor de diferentes lquidos, usados como solventes, em funo da temperatura.
Num grfico detalhado percebe-se como T influi na Pv da gua.
31
Como j foi dito, a adio do soluto: a) acentua ou intensifica as foras atrativas moleculares
b) diminui a superfcie de evaporao do solvente, na interface
Num frasco fechado o lquido evapora at o momento em que ocorre um estado de equilbrio entre as molculas que deixam a fase lquida para a de vapor e as molculas da fase de vapor que se condensam no lquido. Num frasco aberto tal equilbrio no ocorre mas a presena de molculas do lquido na atmosfera determina a velocidade dessa evaporao. Considerando que: P0 = presso de vapor do solvente P = presso de vapor da soluo ( < P0) D P = abaixamento absoluto da presso de vapor D P / P0 = abaixamento relativo da presso de vapor o efeito tonomtrico ser:
32
D P / P0 = Kt . W
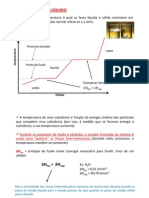
onde: Kt = constante tonomtrica (depende do solvente) W = molalidade da soluo (mol/kg) * Kt = M2 / 1000 (massa molar expressa em kg/mol) 2) Efeito Ebuliomtrico ou Ebuliometria: estuda o aumento na temperatura de ebulio do solvente quando nele dissolve-se um soluto no voltil. Considera-se: t0 = temperatura de ebulio do solvente puro t = temperatura de ebulio da soluo ( > t0) D te = aumento da temperatura de ebulio O efeito ebuliomtrico ser:
D te = Ke . W
onde: Ke = constante ebuliomtrica (depende do solvente) numericamente corresponde diferena no ponto de ebulio quando a Molalidade 1,0 mol/kg de solvente onde * Ke = R Te2 / 1000 Le
R = constante dos gases, Te = temperatura de ebulio do solvente puro e Le = calor latente de evaporao do solvente. 3) Efeito Criomtrico ou Criometria: estuda a diminuio no ponto de congelamento de um solvente quando nele dissolvemos um soluto no voltil. Considerando que: t0 = temperatura de congelamento do solvente puro t = temperatura de congelamento da soluo ( < t0) D tc = abaixamento no ponto de congelamento da soluo O efeito criomtrico ser
D tc = Kc . W
onde: Kc = constante criomtrica (depende do solvente) numericamente corresponde diferena no ponto de congelamento da soluo quando a Molalidade 1,0 mol/kg de solvente
33
* Kc = R Tc2 / 1000 Lv onde: evaporao. R = Te = temperatura de ebulio do solvente e Le = calor latente da
O diagrama de fases ao lado mostra como a adio de um soluto afeta simultaneamente a temperatura de ebulio e a de congelamento do solvente, pela adio de um soluto no voltil.
4) Efeito Osmomtrico ou Osmometria : estuda a presso osmtica de uma soluo separada de outra (ou de um solvente) por uma membrana semipermevel (m.s.p.). A Osmose consiste na migrao espontnea de solvente atravs da m.s.p., sempre que houver diferena de concentrao entre as solues, ocorrendo do meio mais diludo (hipotnico) para o meio mais concentrado (hipertnico) at o momento em que as duas concentraes se igualam. A passagem de molculas do solvente pressionam a m.s.p. e para evitar esta passagem deve-se aplicar uma presso igual e contrria, para evitar a osmose. A figura ao lado mostra que, para se estabelecer um estado de equilbrio entre as duas solues separadas pela membrana semi-permevel dever ocorrer migrao de molculas do solvente, de mais acentuado, da soluo diluda para a concentrada. Perceba-se que h movimento de molculas do solvente para ambos os lados, num processo dinmico, at o estabelecimento de um estado de equilbrio (isotonia).
34
A passagem de solvente atravs da m.s.p. pode ser evidenciada na representao abaixo.
Esta presso exercida numericamente igual Presso Osmtica (p), a qual depende da concentrao e, tambm, da temperatura absoluta. A migrao de solvente s se interrompe quando as duas solues se tornarem isotnicas.
A figura acima mostra como pode ser feita a medida experimental da presso osmtica, numa cmara osmomtria. A presso osmtica, em analogia presso dos gases, pode ser calculada pela expresso: equao dos gases ideais presso osmtica
P=
n V
RT
p = M RT
onde: R = constante universal dos gases T = temperatura absoluta
35
M = molaridade da soluo pode ser usada a Molalidade (W) se a soluo for diluda Para solutos inicos (cidos, bases e sais) os efeitos coligativos devero ser corrigidos de um fator inico, chamado fator de Vant Hoff (i), o qual depende do nmero de ons produzidos por molcula (q) e do grau de dissociao (a) da substncia e que pode ser calculado pela expresso:
i = 1 + a(q - 1)
*** se o soluto molcular: a = 0 i = 1 se o soluto um sal : a = 1 i = q Portanto, se o soluto for inico cada efeito coligativo deve ser multiplicado pelo fator i resultando as seguintes expresses. Tonometria Criometria DP / P0 = Kt . W . i D tc = Kc . W . i Ebuliometria Osmometria
p=M.R.T.i
D te = Ke . W . i
Ex e r c c i o s
1) Relacionando com o fenmeno da osmose explique quais os efeitos sobre um peixe de gua do mar se o colocarmos num aqurio de gua doce ? 2) Quando se adiciona acar a uma salada de frutas, aumenta o volume do caldo . Explique o fenmeno ocorrido. 3) Porque em pases muito frios costume adicionar sal grosso sobre a neve acumulada nas estradas ? 4) Pesquise sobre as aplicaes da osmose reversa . 5) Porque uma salada de alface murcha, aps algum tempo, se for temperada com sal ? 6) Colocando-se duas amostras lquidas de igual volume para evaporao espontnea, sendo a primeira de gua pura e a segunda de salmoura (gua e cloreto de sdio), em qual das duas se observar maior reduo de volume, por evaporao da gua ? Porque ?
36
7) Na preparao do charque, o gacho adiciona considervel quantidade de sal grosso sobre a carne, com o intuito de conserv-la. Justifique porque esse procedimento auxilia na conservao da carne. 8) A utilizao de calda para a conservao de frutas (compotas) vale-se do efeito osmtico. Investigue como funciona esse princpio de conservao. *** Sugesto: consulte um professor que atue na rea de Qumica Biolgica. 9) Considerando-se mesma temperatura, qual o sistema que apresenta maior velocidade de evaporao: a gua do mar ou de um lago ? Porque ? 10) A superfcie do Oceano Antrtico freqentemente se apresenta lquida, apesar de sua temperatura estar bem abaixo de 0o C. Como se explica esse fenmeno ? 11) Qual o abaixamento relativo da presso mxima de vapor de uma soluo que apresenta 10-3 mol de um soluto no inico , por quilograma de gua ? Resposta: 1,8 . 10-5 12) Qual a massa molar de um certo glicdio, sabendo que em certa temperatura a dissoluo de 20,0 gramas do mesmo em 500 gramas de gua causa um abaixamento relativo na presso mxima de vapor igual a 0,004 ? Resposta: 180 g/mol 13) O sangue humano tem presso osmtica 7,8 atm 37o C. Qual a massa aproximada de cloreto de sdio que deve ser dissolvida em gua, suficiente para preparar 4 litros de soluo, para que seja isotnica com o sangue ? Resposta: 36 gramas 14) Eventualmente s soluo 0,30 M de glicose utilizada como injeo intravenosa, pois tem presso osmtica prxima do sangue. Mostre que a mesma apresenta valor prximo ao referido no exerccio anterior, 37o C. 15) Dentre as solues abaixo, qual a que congela temperatura mais baixa ? 1,0 mol de glicose em 1000 g de gua; 1,0 mol de HCl em 1000 g de gua; 1,0 mol de cido actico em 1000 g de gua; 1,0 mol de cloreto de clcio em 1000 g de gua; 0,5 mol de cloreto ferroso em 1000 g de gua. Resposta: 1,0 mol de cloreto de clcio em 1000 g de gua. 16) Considere cinco solues aquosas de concentrao 0,1 mol/L, das seguintes substncias: glicose, NaCl, KCl, K2SO4 e ZnSO4. Qual a que apresenta o menor ponto de congelamento ? Resposta: K2SO4
37
17) Considere uma soluo contendo 17,1 g de sacarose (C12H22O11) em 180 g de gua. Sabendo que a presso de vapor da gua pura, 20oC, 17,5 mm Hg, qual a presso de vapor da soluo ? Resposta: 17,4 mm Hg 18) Calcule o abaixamento relativo da presso mxima de vapor de uma soluo 0,01 mol/kg de CaCl2, cujo grau de dissociao aparente 0,80. Resposta: 4,68 . 10-4 19) Um polmero de frmula geral (C2H4)n abaixou o ponto de congelamento do benzeno em 0,36o C, quando 1,0 grama do mesmo foi dissolvido em 5,0 gramas de benzeno. A constante criomtrica do benzeno vale 5,04o C.mol-1.kg. Determine o valor de n na frmula geral do polmero. Resposta: 100 20) Uma soluo aquosa de cloreto de sdio, na qual se admite o sal totalmente dissociado, ferve a uma temperatura de 101,3o C, ao nvel do mar. Qual o seu ponto de congelamento ? Resposta: - 4,65o C 21) Se uma soluo de um soluto no dissociado congela a 1,30o C, qual a sua temperatura de ebulio ? Resposta: 100,36o C 22) Isolou-se uma protena de uma amostra de soro sangneo. Uma disperso coloidal de 685 mg da referida protena dissolvida em gua suficiente para formar 10 mL tem uma presso osmtica de 0,28 atm a 7o C. Sendo a protena um composto covalente tpico, no dissociado, qual a massa molecular, aproximada, da protena ? Resposta: 5,6 . 103 u 23) Verifique se existe isotonia entre uma soluo aquosa de NaCl 0,01 M e uma soluo aquosa de sacarose (soluto no dissociado) 0,02 M, ambas na temperatura de 20o C ? 24) Para que uma soluo aquosa de glicose tenha a mesma presso osmtica que a soluo salina fisiolgica (NaCl 0,15 M), qual dever ser a concentrao, em mol/L da soluo de glicose ? Resposta: 0,30 M 25) Uma soluo de concentrao 30 g/L de um soluto no inico, de massa molar 90 g/mol, isotnica com uma soluo de sulfato frrico que contm 20 g desse soluto em 600 ml de soluo. Qual o grau de dissociao aparente do sulfato frrico ? Resposta: 0,75 ou 75 %
38
*** Testes de nivelamento (no sero corrigidos ou comentados) 1 - Qual das solues aquosas abaixo apresenta a menor presso de vapor a 250 C? A) CaCl2 0,02 mol/L B) NaCl 0,02 mol/L C) K2SO4 0,01 mol/L D) KCl 0,01 mol/L E) C12H22O11 0,03 mol/L 2 - O sangue humano tem uma presso osmtica de 7,8 atm a 370 C. A concentrao, aproximada, expressa em molaridade de uma soluo de glicose que seja isotnica com o sangue, sabendo que R = 0,082 atm.L/mol.K, A) 0,1 B) 0,3 C) 1,0 D) 3,0 E) 5,0 3 - Um dos segredos descobertos pelos qumicos, no processo de mumificao, a desidratao dos cadveres atravs da utilizao de solues salinas de alta concentrao e viscosidade. A desidratao possvel e explicada pelo fenmeno da A) salinizao. B) neutralizao. C) osmose. D) hidrlise. E) umidificao. 4 - Considere o quadro abaixo.
I II III IV V soluto MgBr2 Al(NO3)3 Ca(NO3)2 NaCl CuCl2 solvente H2O H2O H2O H2O H2O Concentrao em mols/L 1,5 1,0 2,0 3,0 2,5
As solues que apresentam, respectivamente, a maior temperatura de ebulio e a maior temperatura de congelamento so A) II e IV. B) III e I. C) III e IV. D) V e I.
39
E) V e II. 5 - A seguir so arroladas algumas solues aquosas de solutos inicos ou moleculares com suas respectivas concentraes em mol/L. I - NaCl 0,20 mol/L II - glicose 0,30 mol/L III - Al(NO3)2 0,25 mol/L IV - sacarose 0,50 mol/L V - Ca(NO3)2 0,40 mol/L A ordem crescente de ponto de congelamento das solues, admitindo-se ionizao total dos compostos inicos, corresponde sequncia A) I - III - II - V - IV. B) II - IV - I - III - V. C) IV - V - II - III - I. D) V - IV - II - I - III. E) V - III - IV - I - II. 6 - Analise as solues aquosas abaixo discriminada: I - C12H22O11 0,040 mol/L II - AgNO3 0,025 mol/L III - Na2CO3 0,020 mol/L IV - MgCl2 0,010 mol/L Qual das afirmaes abaixo correta, considerando que as espcies inicas esto 100% ionizadas? A) A presso de vapor da soluo III mais alta que a presso de vapor da soluo IV. B) O ponto de congelamento da soluo IV o mais alto de todas as solues acima. C) A presso osmtica da soluo II maior do que a presso osmtica da soluo III. D) A soluo I tem ponto de ebulio mais elevado do que o ponto de ebulio da soluo II. E) O ponto de ebulio da soluo I o mais baixo de todas as solues acima. 7 - Qual das seguintes solues aquosas apresenta maior ponto de ebulio ? A) uria 2,0 molar. B) glicose 1,5 molar. C) NaCl 1,5 molar. D) CH3COOH 1,0 molar. E) sacarose 2,5 molar. 8 - Qual das substncias abaixo, quando em soluo aquosa de idnticos graus de dissociao e concentrao, apresenta maior presso osmtica ? A) K3PO4. B) NaCl. C) NH4Cl.
40
D) C6H12O6. E) CaCl2. 9 - No quadro abaixo esto fornecidas as temperaturas de ebulio de solues aquosas de mesma concentrao molar de nitrato de amnio, sulfeto de sdio e glicose,
Soluo Temperatura.
NH4NO3 T1
Na2S T2
C6H12O6 T3
A relao entre estas temperaturas A) T1 > T2 > T3 B) T2 > T3 > T1 C) T3 > T1 > T2 D) T1 > T3 > T2 E) T2 > T1 > T3 010 - Duas solues, uma de glicose e outra de cloreto de sdio, sero isotnicas quando tiverem a mesma A) temperatura. B) concentrao em mols por litro. C) concentrao e a mesma temperatura. D) concentrao e mesmo fator de VantHoff. E) temperatura e mesmo nmero de partculas dissolvido.
41
3 . I N T RODU O T ERM ODI N M I CA
3 .1 . I n t r o d u o
A Termodinmica ocupa-se, basicamente, com as trocas de energia que acompanham os processos qumicos e fsicos. Historicamente ela se desenvolveu sem um conhecimento detalhado das estrutura da matria, sendo esse um dos seus pontos fortes. Nosso tratamento do assunto ser de maneira mais informal e fenomenolgica, evitando o formalismo matemtico complexo. A linguagem termodinmica no dispensa o uso e a interpretao correta de certos termos como: - sistema: qualquer poro isolada do universo, selecionada para investigao de propriedades; - meio externo ou ambiente: corresponde ao restante de universo, excludo o sistema; - variveis ou funes de estado: grandezas que caracterizam um determinado estado (presso, temperatura, volume, nmero de mols, etc...); - estado: conjunto de condies que caracterizam um sistema; - processo: meio atravs do qual as variveis de um estado podem ser alteradas (isotrmico, isobrico, isomtrico, adiabtico, etc...); - mudana de estado: situao na qual alguma varivel de estado sofre uma alterao (compresso, resfriamento,..); As inter-relaes que se pode estabelecer entre as variveis de estado chamamos de equao de estado. Por exemplo, para um gs ideal, as interrelaes entre as grandezas presso, volume, temperatura e massa gasosa esto expressas na equao geral dos gases PV=nRT onde R uma constante. A simples: a) b) c) termodinmica fundamentada em poucos conceitos e princpios conservao da energia; aumento da entropia; espontaneidade dos processos e equilbrio.
Na evoluo dos processos termodinmicos nada se cogita em relao velocidade com a qual os mesmos ocorrem.
42
3 .2 . T e m p e r a t u r a , Ca l o r e T r a b a l h o
A temperatura uma propriedade ou grandeza que independe da massa ou extenso do sistema e est relacionada com o grau de agitao (energia cintica) molecular.
Como escala adota-se a termodinmica ou absoluta (Kelvin) na qual
mv = 3RT E = 2 2
2 C
T (K) = T (oC) + 273,15
O Calor e o Trabalho (termelstico), por sua vez relacionam-se num princpio fundamental conhecido como 1o Princpio ou 1a Lei da Termodinmica. Calor = quantidade de energia que se transmite de um corpo para outro, devido unicamente diferena de temperatura entre ambos. Portanto: Qtrocado a DT ou
Q = C . DT
onde C a capacidade calorfica do sistema.
Capacidade calorfica e a quantidade de calor que deve ser trocada por certa massa do sistema, para proporcionar a variao de temperatura de 1 grau.
A capacidade calorfica pode ser determinada pelo produto da massa do sistema e seu calor especfico. Por exemplo, considerando que o calor especfico da gua seja 1,0 cal /g . o C ou 4,18 J / g . o C, a capacidade calorfica de 1 quilograma de gua ser C = c . m = 1000 (g) . 4,18 J /g . o C = 4180 J / o C o que significa que devem ser fornecido 4180 Joule de energia para que 1000 gramas de gua variem a sua temperatura em 1 grau. Se a massa considerada for aquela correspondente a 1,0 mol ento a capacidade calorfica ser molar. Assim, a capacidade calorfica molar da gua ser 18,0 cal / mol.grau ou 75,24 J/mol.grau. Algebricamente considera-se o calor trocado como sendo positivo quando o sistema recebe energia do meio externo e negativo quando o sistema perde energia para o meio externo. Q > 0 sistema recebe calor (T )
43
Q < 0 sistema perde calor (T ) Um processo no qual o sistema recebe calor do meio externo chama-se Endotrmico e aquele em que o sistema perde calor para o meio externo chamase Exotrmico. Trabalho = energia trocada como conseqncia de uma fora que atua entre o sistema e o meio externo ou energia que se transmite por qualquer outro modo que no seja a diferena de temperatura entre eles.
A maior parte das transformaes termodinmicas so aquelas nas quais o trabalho provm de uma variao de volume do sistema ao qual denominamos de termelsticas, sendo que as demais formas de trabalho (eltrico, magntico, etc...) no so consideradas em tais transformaes. Quando um gs expande num cilindro, temperatura constante, contra uma presso (P) que se ope, a energia trocada com o meio externo produz o trabalho de expanso, que pode ser calculado atravs de: mas donde e, portanto, Wexpanso = F . d P = F / A F = P . A Wexpanso = P . A . d DV
Logo
Wexpanso = P . D V
Para que seja realizado trabalho necessrio ocorrer variao de volume, como no exemplo da figura ao lado, na qual o gs contido no interior do pisto sofre um deslocamento (d) em relao posio inicial, contra uma presso oposta externa (atmosfrica), ocorrendo uma variao de volume ocupado pelo referido gs.
44
Quando um gs, contido no interior de um cilindro dotado com um mbolo mvel (como na figura anterior), troca calor com o meio externo, a energia se distribuir da seguinte forma: - uma parcela ir provocar aumento na temperatura do gs (DT), fazendo variar o grau de agitao das molculas ou Energia Interna (D U), a qual corresponde ao somatrio de todas as formas de energia associadas ao movimento das molculas; - outra parcela ir provocar a expanso do gs, ou seja, ir realizar um Trabalho ( W ). A relao entre essas duas grandezas conduz 1a Lei ou 1o Princpio da Termodinmica, isto ,
Qtrocado = D U + W
Como a variao da Energia Interna corresponde a calor trocado, a mesma pode ser calculada pela expresso
DU = CDT
onde C a capacidade calorfica da substncia. Aplicao Um mol de CO2 expandido de um volume inicial de 5 para 15 litros, contra uma presso externa de 2 atm, ocorrendo uma variao na temperatura de 27 para 87o C. Sabendo que a capacidade calorfica do CO2 96,5 J / mol . K, calcule a quantidade de calor trocada por esse gs nessa transformao.
3 .3 . T e r m o q u m i c a
3.3.1. Introduo
A Termoqumica tem por objetivo o estudo das variaes de energia que acompanham as reaes qumicas. Esta energia, em geral, manifesta-se sob a forma de calor, embora a luz (energia eletromagntica) tambm esteja presente em alguns processos (combusto e fotossntese). A energia envolvida nas reaes qumicas decorrente de um rearranjo das ligaes qumicas quando reagentes transformam-se em produtos. Esta energia armazenada, principalmente sob forma de ligaes, denominamos de ENTALPIA (do grego, enthalpein = calor) e simbolizamos por H (Heat = calor).
45
Numa reao qumica, portanto, ocorre uma variao de entalpia (DH), sendo as reaes classificadas em dois tipos, segundo o calor liberado ou absorvido:
(H1) ...C2H6O + 3 O2 (H2) .................................. 2 CO2 + 3 H2O (H1) ..6 CO2 + 6 H2O (H2) ...................................... C6H12O6 + 6 O2
( DH = H2 - H1 < 0 ) reao EXOTRMICA
( DH = H2 - H1 > 0 ) reao ENDOTRMICA
3.3.2. Medida de D H e unidades de energia
A variao da entalpia de uma reao qumica pode ser medida, para um certo nmero de reaes, pelo calor liberado ou absorvido durante o processo. Esta medida experimental (calorimtrica) feita utilizando-se Calormetros ou Bombas Calorimtricas (para reaes de combusto), empregando-se a equao:
Q = m.c.Dt
O nmero de reaes cuja entalpia (calor de reao) pode ser determinada diretamente em bombas calorimtricas e calormetros muito reduzido. A maior parte das reaes tem a sua entalpia calculada, valendo-se das leis da Termoqumica, principalmente a LEI DE HESS, como ser visto mais adiante.
A bomba calori mtrica um equi pamento prprio para determinar a energia (calor) das reaes de combusto e algumas reaes de formao.
A unidade mais comum a caloria (cal), que equivale a quantidade de energia absorvida por uma grama de H2O, para que a temperatura varie de 1,00 C, ou seu mltiplo quilocaloria (kcal)
46
1,0 kcal = 1.000 cal 1,0 cal = 4,18 Joules 1,0 kcal = 4,18.103 Joules
3.3.3. Equaes Termoqumicas
Uma equao termoqumica deve conter: a) a equao qumica devidamente ajustada; b) os estados fsicos de cada componente, sendo esta referncia importante porque as mudanas de estado fsico envolvem variaes de energia (entalpia): ex.: H2(g) + 1/2 O2(g) H2O(g) (libera 57,8 kcal/mol) H2(g) + 1/2 O2(g) H2O(l) (libera 68,3 kcal/mol) H2(g) + 1/2 O2(g) H2O(s) (libera 70,0 kcal/mol) c) os estados alotrpicos, quando for o caso: ex.: C(grafite) + O2(g) CO2(g) (libera 94,05 kcal/mol) C(diamante) + O2(g) CO2(g) (libera 94,51 kcal/mol) d) as condies de medida da variao de entalpia: - a variao de entalpia (DH) depende da temperatura e da presso em que foi feita a medida. A maior parte das variaes de entalpia que constam em tabelas foram medidas nas chamadas Condies Padro ou Standard (1 atm e 250C). A indicao de que uma entalpia foi medida em Condies Padro feita atravs do expoente 0 junto ao valor da mesma: ex.: H2(g) + 1/2 O2(g) H2O(l) DH0 = - 68,31 kcal/mol C(graf.) + O2(g) CO2(g) DH0 = - 94,05 kcal/mol C(graf.) + 2 H2(g) CH4(g) DH0 = - 17,81 kcal/mol 1/2 N2(g) + 1/2 O2(g) NO(g) DH0 = + 11,0 kcal/mol
3.3.4. Entalpias de Reao
1) Entalpia de Formao (DH0f): - corresponde ao calor envolvido na formao de 1,0 mol de substncia a partir de seus elementos formadores (substncias simples). ex.: C(graf.) + 2 H2(g) CH4(g) 2 C(graf.) + 3 H2(g) + 1/2 O2(g) C2H6O(l) H2(g) + O2(g) H2O(l) N2(g) + O2(g) NO(g) C(graf.) + O2(g) CO2(g) D H0 = - 17,81 kcal/mol D H0 = - 66,70 kcal/mol D H0 = - 68,31 kcal/mol D H0 = + 11,0 kcal/mol D H0 = - 94,01 kcal/mol
Obs.: considera-se nula a Entalpia de Formao de substncias simples .
47
Algumas entalpias de formao podem ser medidas diretamente em bombas calorimtricas enquanto outros somente so possveis atravs de determinaes algbricas (clculo). Outros exemplos no quadro a seguir. C(diamante) CO(g) CO2(g) C2H6(g) CCl4(g) CHCl3(l) C2H6O(l) CH3COOH(l) 0,453 - 26,41 - 94,05 - 20,24 - 24,61 - 32,14 - 66,37 - 115,80 CaCO3(arag.) CaCO3(calc.) CaO(s) Ca(OH)2(s) H2O(g) H2O(l) H2O2(l) HCl(g) - 288,45 - 288,49 - 151,90 - 235,80 - 57,79 - 68,31 - 44,88 - 22,06 NH3(g) NO(g) NO2(g) N2O4(g) NaCl(s) Na2O(s) NaOH(g) O3(g)
SUBSTNCIA
H0f (kcal/mol)
SUBSTNCIA
H0f (kcal/mol)
SUBSTNCIA
H0f (kcal/mol)
- 11,02 + 21,57 + 7,93 + 2,19 - 98,23 - 99,40 - 101,99 + 34,10
2) Entalpia de Decomposio: - corresponde ao inverso da Entalpia de Formao. 3) Entalpia de Combusto: - corresponde ao calor envolvido na reao de um mol de substncia combustvel com O2 puro. Se o combustvel for orgnico (C,H,O) a combusto completa origina como produtos CO2(g) e H2O(l) (chama azul). Na combusto incompleta ainda ocorre a formao de fuligem, carbono (chama amarela). ex.: CH4(g) + 2 O2(g) CO2(g) + 2 H2O(l) D H0 = - 212,78 kcal/mol C2H6O(l) + 3 O2(g) 2 CO2(g) + 3 H2O(l) D H0 = - 326,70 kcal/mol C6H12O6(s) + 6 O2(g) 6 CO2(g) + 6 H2O(l) D H0 = - 670,00 kcal/mol 4) Entalpia de Neutralizao: - corresponde ao calor envolvido na reao de formao de um mol de gua a partir de um mol ons H+ com um mol de ons OH-, provenientes de um cido e uma base, respectivamente, ambos em soluo aquosa e diluda. Para cidos e bases fortes a reao que ocorre sempre a mesma e a sua variao de entalpia constante: H+(aq) + OH-(aq) H2O(l) D H0 = - 13,20 kcal/mol
Se o cido ou a base for fraco a variao de entalpia ser diferente do valor acima, devido dissociao do cido ou da base devido ao deslocamento do equilbrio ocorrido na neutralizao.
48
5) Entalpia de Dissoluo - corresponde ao calor envolvido na dissoluo (por vezes acompanhada de dissociao) de um mol de determinado soluto em quantidade tal de solvente de modo que a adio do mesmo, aps determinada quantidade limite, no envolva variao de energia. HCl(g)
H2O
HCl(aquoso)
O quadro abaixo mostra a variao de calor envolvida em relao quantidade de solvente (gua) adicionado.
n1(H2O) / n2(HCl)
0
- DH (kcal/mol)
10 16,608
25 17,272
40 17,453
80 17,735
150 17,960
6) Entalpia de mudana de fase Corresponde ao calor envolvido na mudana de estado fsico ou fase cristalina. Assim, H2O(s) H2O(l) H2O(l) H2O(g) C(grafite) C(damante) S(rmbico) S(monoclnico) 7) Entalpia ou Energia de Ligao: corresponde a quantidade de calor absorvida na quebra de 1,0 mol (6,02.1023) de determinada ligao, supondo todas as substncias no estado gasoso, a 250C e 1,0 atm. DH0273 = + 1,438 kcal/mol DH0 = + 10,514 kcal/mol DH0 = + 0,451 kcal/mol DH0 = + 0,071 kcal/mol
A quebra de ligaes sempre endotrmica, enquanto a formao de ligaes sempre exotrmica. ex.: H2(g) 2 H(g) O2(g) 2 O(g) D H = + 104,2 kcal/mol de molculas D H = + 119,1 kcal/mol de molculas
Por vezes utiliza-se a metade desse valor como sendo a Entalpia de Atomizao por mol de tomos formados. Hidrognio: + 52,1 kcal/mol de tomos Oxignio: + 59,5 kcal/mol de tomos
49
A tabela abaixo mostra algumas ligaes mais importantes e suas entalpias
LIGAO
C-C C=C CC H-H O=O Cl - Cl
ENERGIA (kcal/mol)
83,2 146,8 200,6 104,2 119,1 57,9
LIGAO
C-H C-O C=O O-H H-F H - Cl
ENERGIA(kcal/mol)
98,8 85,5 178,0 110,6 135,0 103,1
Numa reao qumica, enquanto a energia absorvida na quebra de ligaes, nos reagentes, a energia liberada nos produtos (formao de ligaes). Assim: Reagentes DH1 > 0 Produtos DH2 < 0
D HRQ = DH1 + DH2 Exercicio: determinar a Entalpia de formao da gua (gasosa) atravs das entalpias de ligao, da tabela acima e comparar com o valor informado anteriormente.
3.3.5. Determinao da Entalpia e Lei de Hess.
A Entalpia de uma reao pode ser obtida de dois modos diferentes: a) por medida calorimtrica experimental (aplicvel a um pequeno nmero de reaes); b) por clculos algbricos, aplicando-se a Lei de Hess. A Lei de Hess, tambm chamada Lei da Soma dos Calores de Reao, permite prever a Entalpia mesmo daquelas reaes de difcil execuo experimental. Segundo Hess a Entalpia de uma reao no depende do modo (caminho) como a mesma executada, mas somente do estado inicial (reagentes) e do estado final (produtos). Genericamente:
A + B
DH4
DH1
L + M
DH2
C + D
DH3
E + F
50
Segundo a Lei de Hess:
DH1 = DH2 + DH3 + DH4
ou, ainda:
DHREAO = DH(f)PRODUTOS - DH(f)REAGENTES
A Lei de Hess pode ser considerada como a Lei da Conservao da Energia aplicada s reaes qumicas.
3.3.6. Entropia (DS)
A Entalpia a grandeza termodinmica relacionada com o calor envolvido nas reaes qumicas. A Entropia a grandeza termodinmica relacionada com o Grau de Desordem Molecular dos sistemas. No h processo termodinmico (fsico ou qumico) que ocorra sem variao de Entalpia e de Entropia. ex.: H2O(s) H2O(l) CaCO3(s) CaO(s) + CO2(g) DS > 0 DS > 0
3.3.7. Entropia Padro (DS0)
A Entropia Padro corresponde a variao de Entropia de uma substncia pura desde o zero absoluto (Entropia nula) at a temperatura de 250C (298 K). O quadro abaixo apresenta algumas Entropias Padro, em cal/mol.K:
Substncias
C(grafite) C (diamante) Al(s) Ca(s) Cl2(g) O2(g)
Entropia Padro
+ 1,4 + 0,6 + 6,8 + 9,9 + 53,3 + 49,0
Substncias
CO2(g) Al2O3(s) CaO(s) CaCO3(s) H2O(l) H2O(g)
Entropia Padro
+ 51,1 + 12,2 + 9,9 + 22,2 + 16,7 + 45,1
3.3.8. Energia de Gibbs (DG0)
J. Willard Gibbs, props uma grandeza termodinmica, tambm denominada Energia Livre, que, combinando a variao de Entalpia, de Entropia e a temperatura absoluta na qual ocorre o processo, permite prever a espontaneidade ou no do referido processo. Sua expresso analtica :
51
DG0 = DH0 - T DS0
(em condies padro)
Obs.: - a maioria das reaes espontneas ocorre com liberao de Calor (DH<0); - a maioria das reaes espontneas ocorre com aumento de desordem molecular (DS>0). A partir disto pode-se concluir que: * se DG < 0 processo espontneo * se DG > 0 processo no espontneo ou induzido (forado) * se DG = 0 o sistema encontra-se em estado de equilbrio Os assuntos Entropia, Entropia Padro e Energia de Gibbs sero tratados com o devido aprofundamento na disciplina de Fsico-Qumica (Termodinmica).
3 .4 . Ex e r c c i o s
1) Uma amostra de 0,100 mol de propano, um dos constituintes do GLP, foi colocada em uma bomba calorimtrica com excesso de O2 e inflamada, segundo a equao: C3H8(g) + 5 O2(g) 3 CO2(g) + 4 H2O(l) . A temperatura inicial do calormetro era de 25o C e sua capacidade calorfica era 97 kJ/o C. A reao aumentou a temperatura para 27,282o C. a) Quantos joules foram liberados pela queima do propano ? b) Qual a variao de energia interna, em kJ/mol, para o C3H8 ? Respostas: 2,22 . 105 Joules ; DU = - 2.220 kJ/mol 2) Quando 3,2 gramas de etanol (C2H5OH) so queimados em uma bomba calorimtrica, contendo 3,5 kg de gua, a temperatura sobe 5,52o C. A capacidade calorfica (ou constante calorimtrica) do calormetro vale 2550 J/oC e o calor especfico da gua 4,18 J/mol. K. Calcule o calor de combusto do etanol, em kJ/mol. Resposta: 1.897 kJ/mol 3) Costuma-se considerar que a necessidade energtica diria para uma pessoa de 50 kg seja de, aproximadamente, 2.000 kcal. Supondo que essa energia seja obtida unicamente pela queima de glicose, no metabolismo, calcule a massa de glicose a ser ingerida, por dia, sabendo que o valor energtico desse alimento de 17 kJ/grama. *** Obs.: 1 kcal = 4,18 kJ
52
4) Sabe-se que o Poder Calorfico de um combustvel a quantidade de energia (em calorias ou Joules) liberada por unidade de massa queimada (grama, quilograma ou tonelada). Consultando tabelas de entalpias de combusto, calcule o Poder Calorfico, em calorias/grama, para os seguintes combustveis: a) Hidrognio b) Etanol c) Metanol d) Glicose e) C (grafite) 5) De forma simplificada a reao de fotossntese pode ser assim representada: 6 CO2(g) + 6 H2O(v)_ C6H12O6(s) + 6 O2(g) Sabendo que as entalpias de formao do CO2, H2O e glicose valem, respectivamente, - 94,0 , - 58,0 e 242,0 kcal/mol, qual a entalpia da reao de fotossntese ? Resposta: - 540,0 kcal/mol 6) A decomposio do explosivo nitroglicerina libera grande volume de gases e considervel quantidade de calor, segundo a equao: 4 C3H5(ONO2)3(l) 12 CO2(g) + 10 H2O(g) + 6 N2(g) + O2(g) As entalpias de formao da nitroglicerina, gs carbnico e vapor dgua valem, respectivamente: - 58,0 , - 94,1 e 57,8 kcal/mol. A partir desses dados calcule a entalpia da reao na decomposio de 0,1 mol de nitroglicerina. Resposta: - 36,85 kcal. 7) As entalpias de combusto do etanol e do cido actico valem, respectivamente 326,7 e 209,4 kcal/mol. No azedamento do vinho, o etanol presente oxida-se, em presena de enzimas produzidas pelo micro-organismo Mycoderma Acceti, formando cido actico. A partir das entalpias acima, calcule a variao de entalpia envolvida na oxidao (fermentao) do etanol formando cido actico. Resposta: - 117,3 kcal/mol 8) A evaporao pela transpirao um mecanismo pelo qual o corpo se desfaz do excesso de energia trmica e regula-se para manter uma temperatura constante. Quantos quilojoules so removidos do corpo pela evaporao de 10,0 gramas de gua ? Resposta: 24 kJ. 9) A entalpia de combusto do metano vale 212,88 kcal/mol e o calor latente de vaporizao da gua 540 cal/grama. A partir desses dados, qual o volume de metano, nas CNTP, que deve ser queimado para converter 250 gramas de gua a 20o C em vapor de gua a 100o C ?
53
10) O valor energtico dos alimentos , em geral expresso, na forma de calor de combusto de carboidratos (como C6H12O6), gorduras (lipdios) e protenas, correspondendo aos valores seguintes: a) carboidratos = 17,0 kJ/grama b) gorduras = 38,0 kJ/grama c) protenas = 17,0 kJ/grama Consultando os dados indicados em alimentos industrializados que voc consome, verifique, pelas quantidades mencionadas, se os valores esto corretos ou, pelo menos, aproximados. 11) Uma vela feita de um material ao qual se pode atribuir a frmula genrica C20H42. Qual o calor liberado na combusto de 10,0 gramas dessa vela, em condies padro, sabendo que na sua combusto a entalpia envolvida correspondente a 13,3 kJoule/mol ? Resposta: 0,47 kJoule 12) A reao de combusto completa do metano libera 2,1 . 102 kcal por mol de CH4 queima, segundo a equao: CH4(g) + 2 O2(g) CO2(g) + 2 H2O(l). A fuso nuclear a partir do ltio, correspondente a : 73Li + 11H 2 42He libera uma quantidade de energia equivalente a 4,0 . 108 kcal por mol de Ltio. Para se ter a mesma quantidade de energia que liberada na produo de 1,0 mol de Hlio, qual a massa de metano que deve ser queimada ? Resposta: 16 toneladas 13) Considere a reao termoqumica de combusto do etanol lquido: C2H5OH(l) + 3 O2(g) 2 CO2(g) + 3 H2O(l) DH = - 330,0 kcal/mol Sabendo que a massa especfica do etanol 0,782 g/ml, qual o volume de etanol lquido que deve ser queimado para obter 561 kcal ? Resposta: 100 mL 14) Tanto gs natural como leo diesel so utilizados como combustveis em transportes urbanos. A combusto completa do gs natural e do leo diesel liberam, respectivamente, 9,0 . 102 kJ e 9,0 . 103 kJ por mol de hidrocarboneto. A queima desses combustveis contribui para o efeito estufa, pela produo de CO2 . Sabendo que esses dois combustveis correspondem a CH4 e C14H30, para igual energia liberada, quantas vezes a contribuio do leo diesel maior do que o metano ? Resposta: 1,4 15) A combusto do metanol e do etanol podem ser representadas pelas seguintes equaes: I CH4O(l) + 2 O2(g) CO2(g) + 2 H2O(l) DH = - 671,0 kcal/mol II C2H6O(l) + 3 O2(g) 2 CO2(g) + 3 H2O(l) DH = - l.327,0 kcal/mol Sabe-se que as densidades desses dois lquidos so praticamente iguais. Na combusto de um mesmo volume, qual libertar mais calor ? Resposta: etanol
54
*** Calores liberados: metanol = 20,96 kJ/g; etanol = 28,84 kJ/g *** Testes de nivelamento (no sero corrigidos ou comentados) 1 - O calor liberado na combusto de um mol de carbono grafite 94 kcal. O calor liberado na combusto total de 6 g de carbono grafite, em kcal, A) 25. B) 30. C) 47. D) 188. E) 282. 2 - Na reao de combusto do carvo vegetal utilizado no preparo de um churrasco, verifica-se A) absoro de calor, pois um processo exotrmico. B) liberao de calor, pois um processo endotrmico. C) variao de entalpia positiva, pois um processo exotrmico. D) transformao de energia trmica em energia qumica, pois um processo endotrmico. E) diminuio de energia dos produtos em relao aos reagentes, pois um processo exotrmico. 3 - A reao cujo efeito trmico representa o calor de formao do cido sulfrico : A) H2O(l) + SO3(g) H2SO4(l) B) H2(g) + SO2(g) + O2(g) H2SO4(l) C) H2O(l) + S(rmbico) + 3/2 O2(g) H2SO4(l) D) H2S(g) + 2 O2(g) H2SO4(l) E) H2(g) + S(rmbico) + 2 O2(g) H2SO4(l)
I. CH4 + 2 O2 CO2 + 2 H2O II. C2H6O + 3 O2 2 CO2 + 3 H2O III. C8H18 + 25/2 O2 8 CO2 + 9 H2O IV. H2 + 1/2 O2 H2O V. C + O2 CO2
4 - Dadas as equaes termoqumicas, a 1 atm e 250 C.
DHI = - 888 kJ/mol DHII = - 1373 kJ/mol DHIII = - 5110 kJ/mol DHIV = - 286 kJ/mol DHV = - 393,5 kJ/mol
o combustvel que libera a maior quantidade de calor, por grama consumido, A) CH4 B) C2H6O C) C8H18 D) H2 E) C
55
5 - A alternativa que representa uma reao que libera a maior quantidade de calor por mol de produto formado A) 4 Fe + 3 O2 2 Fe2O3 B) 3 O2 2 O3 C) H2 + Cl2 2 HCl D) H2 + I2 2 HI E) C + O2 CO2
D H = - 390 kcal D H = + 68 kcal D H = - 44,2 kcal D H = + 12,4 kcal D H = - 94,0 kcal
6 - Os processos de formao da gua no estado lquido e no estado de vapor, a 250 C e 1,0 atm, podem ser representados, respectivamente, por
I. H2(g) + O2(g) H2O(l) II. H2(g) + O2(g) H2O(g) DH = - 68,3 kcal/mol DH = - 57,8 kcal/mol
Considerando-se que a densidade da gua 1,0 g/mL, pode-se afirmar que a quantidade de calor, em kcal, necessria para ferver 1,0 litro de gua lquida A) 105,0 B) 583,3 C) 1.714,3 D) 3.211,0 E) 3.709,0 7 - A reao de fotossntese e a de combusto da glicose esto representadas nas seguintes equaes: 6 CO2(g) + 6 H2O(l) C6H12O6(s) + 6 O2(g) C6H12O6(s) + 6 O2(g) 6 CO2(g) + 6 H2O(l) A energia envolvida na combusto de um mol de glicose de 2,8 . 106 J. Ao produzir 0,1 mol de glicose, a planta A) libera 2,8 . 106 J. B) libera 1,4 . l06 J. C) absorve 2,8 . 106 J. D) absorve 2,8 . 105 J. E) absorve 1,4 . 105 J. 8 - Considere as seguintes transformaes: I. II. III. IV. V. 2 CO2(g) 2 CO(g) + O2(g) HgO(s) Hg(l) + O2(g) C2H5OH(l) + 3 O2(g) 2 CO2(g) + 3 H2O(l) H2O(l) H2O(s) Pb(s) Pb(l)
Representa uma reao qumica exotrmica a alternativa A) I B) II C) III D) IV E) V
56
9 - Dissolvendo-se NH4Cl em gua, observa-se um abaixamento de temperatura do sistema. Por outro lado dissolvendo-se NaOH em gua, ocorre um aumento de temperatura do sistema. As diferenas nesses processos podem ser explicadas considerando que A) NH4Cl sofre dissoluo exotrmica e o NaOH endotrmica. B) A entalpia de dissoluo do NH4Cl menor que zero e a do NaOH maior do que zero. C) A dissoluo do NH4Cl ocorre com absoro de calor e a do NaOH com liberao. D) As duas solues apresentam entalpia dos reagentes maior do que a dos produtos. E) NaOH uma base e o NH4Cl um sal. 10 - A transformao de 1 mol de hematita em ferro metlico representada pela seguinte equao no balanceada: 1 Fe2O3(s) + ___C(s) ___Fe(s) + ___CO(g) DH = + 491 kJ A quantidade de calor envolvida na obteno de 55,8 g de ferro , aproximadamente, igual a A) 491,5 kJ de calor liberado. B) 491,5 kJ de calor absorvido. C) 245,7 kJ de calor liberado. D) 245,7 kJ de calor absorvido. E) 983,0 kJ de calor liberado. 11 - O gs natural comea a chegar no Rio Grande do Sul. O gaseoduto de Transporte Bolvia-Brasil est em fase de implantao e transportar o gs natural diretamente de Santa Cruz de La Sierra at o solo gacho. A combusto do metano, principal componente do gs natural, representada pela seguinte equao no balanceada CH4(g) + O2(g CO2(g) + H2O(l) DH = - 882 kJ A energia, em kJ, fornecida, aps 5 minutos, por uma chama que queima metano completamente, na razo de 2,24 L/min nas C.N.T.P. , aproximadamente, A) 88 B) 441 C) 1600 D) 1764 E) 3510 12 - Durante o processo da fotossntese realizada por plantas verdes, a energia luminosa do sol fora a formao de glicose a partir do dixido de carbono e gua. Com relao a essa transformao, afirma-se que I. H formao de um glicdio e um gs combustvel. II. Ocorre com absoro de energia, portanto trata-se de um processo endotrmico. III. Ocorre transformao de energia luminosa e calorfica em energia qumica.
57
IV.
A equao que representa essa transformao C6H12O6 + 6 O2 6 CO2 + 6 H2O + Q
A alternativa que contm as afirmativas corretas A) III e IV B) II e IV C) II e III D) I e III E) I e II 13 - Ismeros so molculas que tem a mesma frmula molecular, mas diferentes arranjos dos tomos. Um composto com frmula C4H8 apresenta trs ismeros cujas entalpias de combusto esto indicadas na tabela abaixo: Nome do composto ismero Entalpia de combusto (kJ/mol) 1 buteno - 2696,7 Cis-2-buteno - 2687,5 Trans-2-buteno - 2684,2 A transformao do ismero cis-2-buteno para a trans-2-buteno apresenta uma variao de entalpia em kJ/mol de aproximadamente A) + 20,5 B) + 12,5 C) 9,2 D) 5,4 E) 3,3 14 - Quando os xidos Fe3O4 e Fe2O3 so reduzidos pelo alumnio conforme as equaes abaixo I. 3 Fe3O4 + 8 Al 4 Al2O3 + 9 Fe DH = - 800,1 kcal II. Fe2O3 + 2 Al Al2O3 + 2 Fe DH = - 203,5 kcal A quantidade de calor liberada por mol de ferro formado A) maior na reao I. B) maior na reao II. C) Igual nas duas reaes. D) Igual a 9 x 800,1 na reao I. E) Igual a 203,5 na reao II. 15 - Os valores de energia de ligao entre alguns tomos so fornecidos no quadro abaixo. LIGAO CH O=O C=O OH ENERGIA DE LIGAO (kJ/mol) 413 494 804 463
Considerando a reao representada por
58
CH4(g) + 2 O2(g) CO2(g) + 2 H2O(v) o valor aproximado de DH, em kJ, A) 820 B) 360 C) + 106 D) + 360 E) + 820 16 - Abaixo apresentado um quadro com algumas Energias de Ligao no estado gasoso:
Ligao
HH Cl Cl O=O NN H Cl H Br HI
Energia (kJ/mol) 470,7 242,5 489,2 940,8 431,5 365,9 298,6
So feitas as seguintes afirmaes I. necessrio mais energia para decompor a molcula de oxignio do que para decompor a molcula de nitrognio. II. A molcula de HCl deve ser mais estvel do que as molculas dos demais cidos halogendricos, ou seja, HBr e HI. III. Entre as molculas gasosas H2, O2 e Cl2, a molcula de Cl2 pode ser considerada a menos estvel. IV. A reao representada por H2(g) + Cl2(g) 2 HCl(g) deve ser endotrmica. Quais so corretas ? A) Apenas I e II. B) Apenas I e III. C) Apenas II e III. D) Apenas I, III e IV. E) Apenas II, III e IV. 17 - O carbeto de tungstnio WC, uma substncia muito dura e, por essa razo, utilizada na fabricao de vrias ferramentas. A variao de entalpia da reao de formao do carbeto de tungstnio a partir dos elementos Cgrafite e W (s) difcil de ser medida diretamente, pois a reao ocorre a 1.4000 C. No entanto pode-se medir com facilidade os calores de combusto dos elementos Cgrafite , W (s) e do carbeto de tungstnio, WC(s): 2 W(s) + 3 O2(g) 2 WO3(s) DH = - 1.680,6 kJ Cgrafite + O2(g) CO2(g) DH = - 393,5 kJ
59
2 WC(s) + 5 O2(g) 2 CO2(g) + 2 WO3(s) DH = - 2.391,6 kJ Pode-se, ento calcular o valor da entalpia da reao abaixo e concluir se a mesma endotrmica ou exotrmica: W(s) + Cgrafite WC(s) DH = ? A qual alternativa corresponde o valor de DH e o tipo de reao ? (A) (B) (C) (D) (E) DHreao - 878,3 kJ - 317,5 kJ - 38,0 kJ + 38,0 kJ + 317,5 Classificao da reao Exotrmica Exotrmica Exotrmica Endotrmica Endotrmica
18 - O gs natural veicular (GNV) um combustvel alternativo, menos poluente, de menor custo por quilmetro, onde o metano (CH4) o componente predominante. Sabe-se que 1 mol de metano libera cerca de 890 kJ, em uma combusto completa. A energia liberada, em kJ, na combusto total de 800 g de metano, no motor de um automvel movido por GNV , de aproximadamente, A) B) C) D) E) 2.700. 12.800. 14.240. 44.500. 712.000.
19 - O metano, principal componente do gs natural, pode sofrer combusto incompleta segundo a equao abaixo. 2 CH4(g) + 3 O2(g) 2 CO(g) + 4 H2O(l) DH = - 890,0 kJ DH = - 566,0 kJ
Considerando as seguintes equaes termoqumicas CH4(g) + 2 O2(g) 2 CO(g) + O2(g) CO2(g) + 2 H2O(l) 2 CO2(g)
Dadas essas equaes termoqumicas, possvel obter o valor de DH da equao acima. Esse valor , em kJ, A) B) C) D) E) 324,0 607,0 1.214,0 1.456,0 2.346,0
60
20 - Em nosso cotidiano ocorrem processos que podem ser endotrmicos (absorvem energia) ou exotrmicos (liberam energia). Assinale a alternativa que contm apenas fenmenos exotrmicos ou apenas fennemos endotrmicos. A) exploso de fogos de artifcio combusto em motores de automveis formao de geada. B) sacagem de roupas formao de nuvens queima do carvo. C) combusto em motores de automveis formao de geada evaporao de lagos. D) evaporao de gua nos lagos secagem de roupas exploso de fogos de artifcio. E) queima de carvo formao de geada derretimento de gelo.
61
4 . CI N T I CA E EQU I L B RI OS
4 .1 . Ci n t i c a Qu m i c a
(Qu m i c o e I n i c o )
A Cintica Qumica tem por objetivo a determinao da velocidade (mdia e instantnea) com que as reaes qumicas ocorrem, bem como os fatores que nela influem. As reaes qumicas, sob o ponto de vista cintico, podem ser classificadas segundo dois critrios distintos. I) Quanto velocidade a) rpidas: combusto, neutralizaes,... (quase instantneas) b) lentas: fermentaes, formao de ferrugem,... II) Quanto ao mecanismo a) reaes elementares: so aquelas que ocorrem numa s etapa, decorrentes de colises entre molculas dos reagentes com os produtos dando origem diretamente aos produtos. Ex.: formao de HI
H2(g) + I2(g) 2 HI(g)
b) reaes complexas: so aquelas que ocorrem em vrias etapas, segundo um mecanismo. O mecanismo segundo o qual uma reao em etapas ocorre estabelecido a partir de complexa pesquisa no sendo um de nossos propsitos para estudo. Ex.: formao do NO2
2 NO(g) + O2(g) 2 NO2(g)
1a etapa (rpida) : 2 NO(g) N2O2(g) 2a etapa (lenta) : N2O2(g) + O2(g) 2 NO2(g) reao global : 2 NO(g) + O2(g) 2 NO2(g)
*** A condio de ser reao elementar ou complexa dever ser informada no enunciado da questo ou pergunta.
62
Velocidade mdia de reao (vm)
A velocidade mdia (vm) pode ser calculada pela variao de quantidade de reagente consumido ou produto formado, em determinado intervalo de tempo. Esta quantidade pode ser expressa em massa, nmero de mols, concentrao, volume,....
vm = D m/Dt
ou Dn/Dt ou D[X]/Dt concentrao molar
Sendo conhecida a equao estequiomtrica ajustada, a velocidade mdia pode ser calculada em relao qualquer componente (R ou P) da reao. O diagrama abaixo mostra como variam as concentraes dos reagentes e dos produtos a medida que a reao progride. mols [produtos]
[reagentes] tempo Observe que: Dn(reagentes) < 0 diminui com o passar do tempo Dn(produtos) > 0 aumenta com o passar do tempo No entanto, a velocidade de uma reao sempre dever ter um valor positivo. Portanto, quando calculamos a velocidade mdia da reao, em relao aos reagentes a razo Dn/ Dt dever ser multiplicada por 1, para que no resulte um valor negativo para a velocidade mdia. Assim, para uma reao genrica: A + B L + M
As velocidades mdias em relao aos reagentes e produtos sero calculadas pelas expresses:
63
vm
Dn Dn Dn A =- B = L = M =Dt Dt Dt Dt
Dn
Exemplo: O quadro a seguir mostra a variao de massa sofrida pelo carbonato de clcio ao se decompor em xido de clcio e gs carbnico, segundo a equao:
CaCO3(s) CaO(s) + CO2(g)
m (gramas) tempo (s) 4,00 0 3,60 20 3,30 40 3,10 60 3,00 80 2,95 100
a) Calcule a velocidade mdia (em gramas/segundo), no intervalo entre 20 e 80 segundos; b) Calcule a velocidade mdia (em mols/minuto) no intervalo entre 0 e 60 segundos; c) A velocidade mdia dessa reao constante ? Porque ? Respostas:
Velocidade instantnea de reao (vi ou v)
A velocidade instantnea (vi ou v) obtida num determinado instante da reao e calculada atravs de uma lei cintica ou equao de velocidade, expressa pela LEI DA AO DAS MASSAS ATIVAS , proposta por Gulberg e Waage (1876), que alm de concluses sobre seus prprios experimentos, compilaram dados e resultados experimentais de outros fsico-qumicos da poca, entre os quais Berthelot e St. Gilles, H. Wilhelmy, S. Arrhenius,... Para uma reao genrica do tipo:
aA + bB
lL + mM
a Lei da Ao das Massas expressa pela relao:
64
v = k [A]a[B]b
na qual: * [A] e [B] representam as concentraes molares; * k = constante cintica, a qual caracterstica de cada reao, varia com a temperatura e calculada pelos dados cinticos; * a e b so as ordens de reao as quais, tambm so obtidas a partir dos dados cinticos da RQ. Quando a reao ocorre numa s etapa (elementares) as ordens coincidem com os coeficientes estequiomtricos: a = a ; b = b , .... Quando a reao ocorre em vrias etapas, segundo um mecanismo (complexas) as ordens sero iguais aos coeficientes da etapa mais lenta (etapa limitante da velocidade). O mecanismo segundo o qual uma reao ocorre algo resultante de constante pesquisa experimental, constituindo-se num dos aspectos mais complexos no estudo cintico de uma reao. A medida que os recursos tcnicos da Qumica Analtica avanam possvel analisar mais detalhadamente as reaes qumicas determinando os reais mecanismos segundo os quais as mesmas ocorrem. Algumas reaes j foram suficientemente estudadas e analisadas e, atualmente, j se sabe qual o seu mecanismo. Quando uma reao for complexa, isto , ocorrer em vrias etapas necessrio que se conhea o seu mecanismo etapa por etapa, bem como as velocidades de cada etapa. Estes aspectos, como j foi dito, demandam incansveis pesquisas experimentais sobre a cintica das reaes. Assim como para as reaes elementares, atualmente j foram elucidados os mecanismos de vrias reaes complexas, tal como a formao do HBrO2 a partir do HBr e O2.
4 HBr + O2
2 H2O + 2 Br2
Aps inmeras pesquisas experimentais, os qumicos sugeriram o seguinte mecanismo para a reao:
65
1a etapa: HBr + O2 HBrO2 2a etapa: HBrO2 + HBr 2 HBrO 3a etapa: 2 HBrO + 2 HBr 2 H2O + 2 Br2 4 HBr + O2 2 H2O + 2 Br2
lenta rpida rpida
Portanto a equao de velocidade ser dada pela etapa mais lenta (1a) e, portanto as ordens cinticas (a e b) sero 1 e 1, e a lei de velocidade ou equao cintica ficar: V = k [ HBr ]1 [ O2 ]1 Um possvel mecanismo para essa etapa mais lenta pode ser o seguinte:
Por outro lado o modo como as molculas colidem entre s para favorecer a formao dos produtos tambm um fator importante. Este modo mais favorvel como as molculas devem colidir entre s para formar os produtos denominamos de fator espacial ou fator estrico e a configurao de coliso mais adequada denominamos geometria de coliso. A figura a seguir mostra as diferentes formas de coliso que podem ocorrer entre as molculas, para a reao entre HBr e O2.
66
Estas caractersticas (reao complexa, mecanismo, etapa mais lenta,...) so indicados, habitualmente, nos enunciados das questes. As reaes complexas, em geral, so aquelas onde os coeficientes assumem valores mais elevados (3,4,...).
Por que ocorrem as reaes qumicas ?
1) Colises entre as molculas dos reagentes; Para que ocorra uma reao entre duas ou mais substncias necessrio que as molculas colidam entre s de modo que haja rompimento das ligaes nos reagentes e formao de novas ligaes constituindo os produtos As colises entre as molculas dos reagentes podem ser de dois tipos:
67
a) Colises no-efetivas ou no eficazes: so aquelas em que no h quebra de ligaes e, portanto, no h formao de produtos. As colises no- efetivas ocorrem entre molculas da mesma espcie ou de espcies diferentes sem energia suficiente para a quebra das ligaes. b) Colises efetivas ou eficazes: so aquelas em que h quebra de ligaes e formao de novas ligaes originando os produtos. Considere-se, por exemplo, a formao de HI a partir de H2 e I2 (reao elementar uma s etapa):
2) Energia mnima para reagir (Energia de Ativao) Alm de colises intermoleculares em orientao favorvel (geometria de coliso) as molculas participantes devem apresentar uma quantidade de energia cintica mnima que proporcione efetivamente as rupturas das ligaes entre as molculas reagentes e formao de novas ligaes. Portanto, seja para reaes exotrmicas ou endotrmicas necessrio um incremento de energia para inici-las. A energia de ativao representa, pois, um obstculo formao dos produtos.
Quanto maior a Eativao, mais lenta ser a reao !
O grfico a seguir mostra o caminho da reao de formao do HI relacionando-o com as variaes de energia
68
1. As molculas colidem sem energia suficiente para a reao; 2. A energia do sistema aumentou mas no em proporo suficiente para uma coliso efetiva; 3. No ponto de mais elevada energia do sistema forma-se o complexo ativado; 4. As ligaes entre os produtos consolidam-se; 5. Definitivamente os produtos esto formados. As representaes grficas da Energia de Ativao tanto para reaes exotrmicas como endotrmicas so as seguintes:
69
4 .2 . Fa t o r e s q u e i n f l u e m n a V e l o c i d a d e d a s Re a e s
a) rea de contato entre os reagentes Esse fator tem sentido quando um dos reagentes for slido. Por exemplo, quando desejamos queimar lenha, numa fogueira, iniciamos o fogo com lenha fina ou gravetos. Uma pea de palha de ao (Bombril) oxida mais facilmente do que uma chapa do mesmo metal e igual massa. Fe(prego) + H2SO4(aquoso) FeSO4(aquopso) + H2(g) (v1) Fe(limalha) + H2SO4(aquoso) FeSO4(aquopso) + H2(g) (v2)
V1 < V2
b) Concentrao dos reagentes A velocidade das reaes diretamente proporcional concentrao dos reagentes. A expresso para o clculo da velocidade conhecida com lei de velocidade, lei cintica ou lei da ao das massas, j estudada anteriormente. Relembrando, para uma reao genrica:
aA + bB lL + mM v = k [A]a.[B]b...
se a reao for elementar: a = a , b = b , ... se a reao for complexa a , b , ... so obtidos pela mecanismo da reao, o qual dever ser indicado necessariamente.
c) temperatura: as variaes de temperatura indicam variao no grau de agitao molecular. Assim: - um aumento de temperatura, aumenta a freqncia de colises entre as molculas e aumenta e energia envolvida no impacto entre as mesmas, favorecendo a quebra de ligaes entre os reagentes e a formao de novas ligaes (produtos). Um maior nmero de molculas alcana a energia mnima para a ocorrncia da reao (Energia de Ativao).
70
Por exemplo, para a melhor conservao dos alimentos os mesmos devem ser guardados em refrigeradores e freezers, diminuindo a velocidade das reaes que causam as decomposies dos mesmos (em geral processos fermentativos). d) Radiaes e descargas eltricas: atuam como fatores energticos (Energia de Ativao); e) catalisadores: so substncias que encontram caminhos alternativos para a reao, envolvendo menor energia (diminuem a Energia de Ativao) e sem serem consumidos no processo. Por exemplo, a reao do SO2 com O2, na atmosfera, formando SO3, tem velocidade quase nula e uma Eativao de 240 KJ/mol. Em presena de NO2 e velocidade aumenta consideravelmente, diminuindo a Eativao para cerca de 110 KJ/mol. Um provvel mecanismo para essa reao seria: SO2 + NO2 SO3 + NO E1 (consumo do catalisador) NO + O2 NO2 E2 (regenerao do catalisador) Reao global: SO2 + O2 SO3 E = 110 KJ/mol O catalisador participa em determinadas etapas da reao sendo regenerado nas posteriores. Por este motivo diz-se que o catalisador no se altera qualitativa e quantitavamente e por esta razo pode ser usado em pequenas quantidades, pois uma mesma partcula cataltica atua em diversos processos unitrios. O diagrama a seguir mostra que a presena do catalisador diminui a barreira energtica (Energia de Ativao), justificando o aumento na velocidade da reao.
Os catalisadores, portanto, aumentam a velocidade das reaes porque diminuem a Energia de Ativao, sem participar da sua estequiometria. Por outro lado os catalisadores no iniciam reaes mas interferem na velocidade de reaes que j ocorrem sem a sua presena.
71
Em funo do estado fsico de reagentes, produtos e catalisador, a catlise subdividida em dois tipos: a) catlise homognea: reagentes e catalisador formam um sistema monofsico.
2 SO2(g) + 1/2 O2(g)
NO2)g)
2 SO3(g)
b) catlise heterognea: reagentes e catalisador formam um sistema heterogneo.
N2(g) + 3 H2(g)
Fe(s)
2 NH3(g)
Obs.: na formao da amnia a presena de Arsnio (As) inibe a ao do catalisador (Fe) tornando a sua eficincia muito reduzida. Nesse caso o Arsnio chamada de inibidor ou veneno de catlise. Um importante exemplo de catlise heterognea ocorre nos dispositivos antipoluio instalados nos sistema de descarga dos automveis, conhecidos como conversores catalticos. Os gases oriundos da cmara de combusto dos automveis contm substncias poluentes (CO, NO, SO2,..) as quais passam atravs de uma colmia cermica que contm as substncias catalticas (Rdio, Platina, Paldio ou Irdio) que convertem esses gases em substncias no poluentes ou menos poluentes (CO2, N2, H2S,..), diminuindo a poluio atmosfrica.
72
4 .3 . Ex e r c c i o s
1) Na reao: 2 X(g) Z(g) , a concentrao de X cai de 0,50 para 0,10 mol/L em 45 minutos. Calcule a velocidade mdia em termos de a) diminuio na concentrao de X em mol/L.s. b) aumento na concentrao de Z em mol/l.min. Respostas: a) 1,5 . 10-4 mol/L.s b) 4,4 . 10-3 mol/l.min 2) Para a reao 4 HBr(g) + O2(g) 2 Br2(g) + 2 H2O(g) a equao de velocidade mais freqentemente escrita em funo do componente de coeficiente unitrio, isto , velocidade = - D[O2] / D t. Escreva equaes equivalentes a esta em funo de todos os componentes. 3) Complete a seguinte tabela para a reao 2 A(g) + Z(g) produtos, que de primeira ordem em relao aos dois reagentes: [A] (mol/L) 0,450 ----0,750 [Z] (mol/L) 0,300 0,053 0,800 k (L/mol.s) 4,0 0,32 ----V (mol/L.s) ----0,018 0,010
Respostas: 0,54 mol/L.s ; 1,1 mol/L ; 0,017 L/mol.s 4) Em determinado experimento, a reao de formao de gua ocorre com o consumo de 4,0 molsde oxignio por minuto. Qual a velocidade mdia de consumo do H2 ? Resposta: 8,0 mols/minuto 5) Experimentalmente observou-se que a velocidade de formao da substncia C, atravs da reao 2 A + B C independente da concentrao de B e quadruplica quando a concentrao de A duplicada. Representando por k a constante de velocidade, qual a expresso da lei de velocidade ? Resposta: v = k [A]2 6) A velocidade da reao de 2a ordem : 2 A produtos vale 10,0 mols/L.min, quando a concentrao de A de 2,0 mols/L. Se a concentrao baixar para a metade do valor inicial, qual a velocidade ? Resposta: 2,5 mols/L.min. 7) Para uma reao envolvendo um s reagente, os seguintes dados cinticos da mesma foram obtidos:
73
V (mol/L.min) [reagente]
0,020 0,100
0,020 0,090
0,019 0,080
0,021 0,070
Qual a ordem para essa reao ? Resposta: zero 8) Os dados abaixo referem-se reao de NO com Cl2 para formar NOCl. [Cl2] (mol/L) 0,050 0,150 0,050 a) b) c) d) [NO] (mol/L) 0,050 0,050 0,150 Velocidade (mol/L.s) 1,0 . 10-3 3,0 . 10-3 9,0 . l0-3
Qual a ordem em relao ao NO ? E ao Cl2 ? Escreva a equao de velocidade. Calcule a constante cintica. Qual a velocidade quando as concentraes de Cl2e NO valem, respectivamente 0,20 e 0,40 mol/L ? Respostas: 2 e 1 ; v = k [NO]2[Cl2]1 ; 8,0 L2/mol2.s ; 0,26 mol/L.s 9) Os seguintes dados referem-se decomposio do cloreto de etila, em fase gasosa, na temperatura de 450 K: t (min) 0 1 2 3 [EtCl] (mol/L) 0,200 0,197 0,193 0,190 t (min) 4 8 16 [EtCl] (mol/L) 0,187 0,175 0,153 -
a) Atravs de um grfico (10 x 10), em papel milimetrado, demonstre que essa reao de primeira ordem; b) Pelo grfico determine k; 10) A constante de velocidade de primeira ordem para a decomposio do C2H5Cl, na temperatura de 720 K, de 2,5 . 10-3 min-1. Partindo de uma concentrao de 0,200 mol/L calcule: a) a concentrao do C2H5Cl aps 1,0 hora; b) o tempo decorrido para que a concentrao se reduza pela metade. 11) Quando se adiciona perxido de hidrognio (gua oxigenada) sobre a pele, aparentemente nada se observa. No entanto se houver um ferimento, em presena de sangue a gua oxigenada se decompe com relativa velocidade. Pesquise a respeito da substncia presente no sangue que produz esse efeito.
Obs.: consulte um professor que atue na rea de Bioqumica.
74
12) Como cada um dos seguintes itens afetam a velocidade de uma reao ? a) A passagem do tempo. b) Diminuio do tamanho de um recipiente para uma reao em fase gasosa. c) Adio de um catalisador. 13) Usualmente diz-se que a adio de uma pequena quantidade de um catalisador produz significativos efeitos na velocidade de uma reao. Explique porque essa afirmativa verdadeira. 14) Com suas prprias palavras, explique por qu a) uma diminuio na temperatura diminui a velocidade de uma reao. b) A duplicao da concentrao de um reagente nem sempre duplica a velocidade da reao. c) Um catalisador altera a constante de velocidade. 15) Pesquise a respeito do que so enzimas e qual o seu papel em relao velocidade das reaes, de um modo geral.
Obs.: consulte um professor que atue na rea de Biotecnologia.
16) Pesquise a respeito da constituio (composio) e das principais reaes que ocorrem nos catalisadores dos automveis. 17) Uma reao apresenta uma variao de entalpia de 85 kJ/mol e uma energia de ativao de 70 kJ/mol, sem a utilizao de catalisador. Pela adio de um catalisador essa energia de ativao reduziu-se para 45 kJ/mol. Represente um diagrama dessas energias, indicando na ordenada energia e na abcissa tempo de reao. 18) Localize no diagrama do exerccio anterior o complexo ativado da reao. 19) A adio de um catalisador influi na variao de entalpia de uma reao ? Porque ? 20) Pesquise a respeito da importncia da catlise Ziegler-Natta na produo de polmeros como o polietileno.
Obs: nossa Faculdade tem em seu corpo docente especialistas na rea. Consulte-os !!
21) Para remover uma mancha de um prato de porcelana faz-se o seguinte: cobriu-se a mancha com meio copo de gua fria, adicionaram-se algumas gotas de vinagre e deixou-se por uma noite. No dia seguinte a mancha havia clareado suavemente. Usando apenas gua e vinagre, sugira duas alteraes no procedimento, de tal modo que a remoo da mancha possa ocorrer em menor tempo. Justifique cada uma das alteraes propostas. 22) Afim de adoar mais rapidamente uma xcara de ch devemos utilizar acar comum ou acar cristal ? Explique.
75
23) Na digesto de alimentos ocorre uma srie de reaes qumicas. Explique, levando em conta a velocidade das reaes qumicas, porque benfico mastigar bem os alimentos ? 24) A plvora negra uma mistura de trs slidos: carvo, salitre (KNO3) e enxofre. Porque, na plvora, esses slidos se apresentam sob forma pulverizada (p) e no apenas colocados em pedaos ? 25) Frascos contendo gua oxigenada devem ser guardados em frascos escuros e em locais de baixa temperatura. Explique tais recomendaes. *** Testes de nivelamento (no sero corrigidos ou comentados) 1 -Se a velocidade de uma reao qumica dada pela expresso v = k [A]n diz-se que a reao de ordem A) A B) 1 C) k D) v E) n 2 - A combusto da gasolina uma reao exotrmica que ocorre com uma velocidade elevada em motores a exploso. A reao iniciada por uma fasca proveniente da vela de ignio, porque A) a gasolina s queima a temperaturas elevadas. B) a reao de combusto da gasolina lenta a temperatura ambiente. C) a fasca age como oxidante enrgico. D) a combusto s ocorre em presena de oxignio atmico. E) necessrio vencer a barreira representada pela energia de ativao. 3 - O processo de oxidao numa esponja de ao muito mais rpido do que numa lmina do mesmo material. O fator que determina essa diferena A) a concentrao. B) o volume do sistema. C) a ordem da reao. D) a superficie de contato. E) a presena de um catalisador. 2 A + B produtos apresenta uma lei de velocidade expressa por v = k [A]2 Se a concentrao do reagente A for mantida constante e a de B for duplicada, a velocidade de reao fica multiplicada por um fator igual a A) 0 B) 1 C) 2 D) 4 E) 8 5 - Como maneiras eficientes de aumentar a velocidade de uma reao qumica, atravs da alterao de fatores energticos, so apresentados os seguintes: I - aumento da temperatura do sistema. 4 - A reao:
76
II - aumento da concentrao dos reagentes. III - diminuio do volume do sistema. IV - adio de um catalisador. Quais so corretas ? A) apenas I e II. B) apenas II e IV. C) apenas I e III. D) apenas I e IV. E) I, II, III e IV. 6 - Para alguns cientistas, o cloro atmico proveniente de certas substncias, entre as quais as empregadas como propelentes em aerossis, acelera a destruio da camada de oznio da atmosfera de acordo com o seguinte mecanismo: Cl(g) + O3(g) ClO(g) + O2(g) ClO(g) + O(g) Cl(g) + O2(g) Por isso, o cloro atmico age como A) ativador. B) inibidor. C) catalisador. D) veneno de catlise. E) promotor. 2 A(g) + B(g) C(g) verifica-se experimentalmente que a velocidade de formao de C independe da concentrao de B e quadruplicada quando dobra a concentrao de A. A expresso matemtica da lei de velocidade para esta reao A) k.[A]2.[B] B) k.[A].[B] C) k.[A]2 D) k.[A]4 E) k.[A]4.[B] 8 - O estudo cintico para a reao A B est representado no grfico da velocidade de reao (v), em funo da concentrao do reagente A. 7 - Para a reao
77
A A partir desse grfico pode-se dizer que a lei de velocidade para esta reao A) v = k.[A]2 B) v = k.[A] C) v = k D) v = k / [A] E) v = k / [A]2
H2 + 1/2 O2 H2O espontnea e pode ocorrer de maneira explosiva, nas condies ambientes. Em locais onde se trabalha com o gs hidrognio rigorosamente proibido fumar ou produzir fagulhas ou fogo, pois a chama A) consome o hidrognio, diminuindo a velocidade da reao. B) consome rapidamente a energia liberada na reao. C) fornece a energia de ativao necessria para que a reao ocorra. D) muda o mecanismo da reao, que ocorre mais rapidamente. E) torna a reao mais endotrmica, aumentando a sua velocidade. 10 - A isomerizao de 1,0 mol de 1,2-dicloroeteno foi realizada em um frasco fechado, obtendo-se os seguintes valores de converso em funo do tempo:
Tempo (min) mols de A
9 - A reao
0 1,00
10 0,90
20 0,81
30 0,73
A trans-1,2-dicloroeteno
B cis-1,2-dicloroeteno
Nos primeiros 10 minutos de reao a velocidade mdia de isomerizao em mol/min A) 8,00 . 10-3 B) 1,00 . 10-2 C) 9,00 . 10-2 D) 1,00 . 102 E) 1,25 . 102
78
11 - Considere a seguinte reao genrica, na qual todos os componentes encontram-se em mesma fase: A + B C + D tem-se o seguinte diagrama
H
A+B
C+D
caminho da reao
O uso do catalisador adequado A) diminui a energia de ativao e aumenta o DH da reao. B) diminui a energia de ativao e diminui o DH da reao. C) aumenta a energia de ativao e aumenta o DH da reao. D) aumenta a energia de ativao e mantm o DH constante. E) diminui a energia de ativao e mantm o DH constante. 12 - Uma reao de primeira ordem em relao ao reagente A e de primeira ordem em relao ao reagente B, sendo representada pela equao: 2 A(g) + B(g) 2 C(g) + D(g) Mantendo-se a temperatura e a massa constantes e reduzindo-se metade os volumes de A(g) e B(g), a velocidade da reao A) duplica. B) fica reduzida metade. C) quadruplica. D) fica oito vezes maior E) fica quatro vezes menor. 13 - O grfico a seguir representa a variao de concentrao de um radioistopo com o tempo
concentrao 8. 7. 6. 5. 4. 3. 2. 1. 0. . . . . . . . . . . 0 1 2 3 4 5 6 7 8 9 10 tempo(min)
79
A observao do grfico permite afirmar que a meia-vida do radioistopo igual a A) 1 min B) 2 min C) 4 min D) 5 min E) 10 min 14 - O grfico a seguir refere-se a uma reao genrica A + B R + S
energia
(kcal/mol)
40. 35. 30. 25. 20. 15. 10. 05.
. . . . . . . . . . . caminho da reao
A partir das informaes contidas na grfico, possvel afirmar que a reao em questo possui uma energia de ativao de Arrhenius de aproximadamente A) 5 kcal/mol. B) 15 kcal/mol. C) 20 kcal/mol. D) 25 kcal/mol. E) 40 kcal/mol. 15 - A poluio uma das causas da destruio da camada de oznio. Uma das reaes que pode ocorrer no ar poludo a reao do dixido de nitrognio com o oznio, representada abaixo. 2NO2(g) + O3(g) N2O5(g) + O2(g) Essa reao apresenta uma lei de velocidade expressa por: v = k [NO2].[O3] Se a concentrao de NO2 (g) for duplicada, mantendo-se constantes todos os outros fatores, a velocidade da reao A) quadruplica. B) reduz-se metade. C) duplica. D) permanece constante E) triplica
80
16 - Amnia produzida industrialmente atravs do processo Haber, equacionado por N2(g) + 3 H2(g) 2 NH3(g) Colocando-se em um reator, nitrognio e hidrognio, obtiveram-se os seguintes dados cinticos, em minutos e mol/L t (min) 0 10 [N2] (mol/L) 0,50 0,45 [H2] (mol/L) 1,50 1.35 [NH3] (mol/L) ...... 0,10
Calculando-se a velocidade mdia da reao, em relao do nitrognio consumido, em mol/L.min, obtm-se A) 3,4 . 10-6 B) 1,0 . 10-4 C) 2,3 . 10-2 D) 5,0 . 10-3 E) 1,5 . 10-2 17 - Amostras de magnsio foram colocadas em solues aquosas de cido clordrico de diversas concentraes e temperaturas, havendo total consumo do metal e desprendimento de hidrognio gasoso. Observaram-se os seguintes resultados Amostra
Massa de magnsio consumida (g) Tempo de reao (min)
I II III IV
0,20 2,00 4,00 4,00
1 5 10 20
Pela anlise dos dados contidos na tabela acima correto afirmar que A) a velocidade mdia da reao na amostra I maior que amostra II. B) a quantidade de hidrognio desprendida na amostra II maior do que na amostra IV. C) a velocidade mdia de reao na amostra III igual da amostra IV. D) a velocidade mdia de reao na amostra IV a metade da velocidade mdia de reao na amostra II. E) a quantidade de hidrognio desprendido na amostra III menor do que na amostra IV. 18 - A reao entre os gases representados na equao a seguir tem grande importncia na qumica ambiental. 2 CO(g) + O2(g) 2 CO2(g) Essa reao apresenta uma lei de velocidade expressa por v = k .[CO]2.[O2] Se a concentrao de CO(g) for duplicada e a concentrao de oxignio for reduzida metade, mantendo-se constantes todos os outros fatores, a velocidade da reao
81
A) B) C) D) E)
duplica. quadriplica. reduz-se metade. permanece constante. triplica.
19 - A reao NO + Br2 NOBr apresenta uma lei experimental de velocidade expressa por v = k.[NO]2.[Br2] . A partir dessa informao, possvel afirmar que A) a reao apresenta ordem 3/2. B) a equao dada corresponde a um processo elementar trimolecular. C) a velocidade da reao quadruplica quando a concentrao de NO dobrada. D) a concentrao de Br2 no tem influncia na velocidade da reao. E) a velocidade da reao sextuplicada ao se dobraram as concentraes de ambos os reagentes. 20 - A reao entre persulfato e iodeto, a 250 C, representada pela equao qumica S2O8-2(aq) + 3 I-(aq) 2 SO4-2(aq) + I3-(aq) e apresenta uma lei de velocidade, determinada experimentalmente, dadas pela expresso v = k . [S2O8-2(aq)] . [I-(aq)] A partir dessas informaes, considere as afirmaes a seguir, IA reao de oxirreduo. II A reao apresenta uma cintica de segunda ordem. III - A velocidade da reao diretamente proporcional concentrao dos reagentes. IV - A velocidade de consumo do S2O8-2(aq) trs vezes maior que a de I-(aq). Quais esto corretas ? A) Apenas I. B) Apenas II e IV. C) Apenas III e IV. D) Apenas I, II e III. E) Apenas II, III e IV.
82
4 .4 . EQU I L B RI OS (QU M I CO E I N I CO)
4.4.1. QUMICO ***RQ Irreversveis (ou completas) So reaes que ocorrem num s sentido. No havendo excesso estequiomtrico os reagentes so integralmente transformados em produtos. Considera-se que as mesmas tenham rendimento 100%. ex.: reaes de combusto e de neutralizao.
R P
*** RQ Reversveis (ou incompletas) So reaes que podem ocorrer no sentido direto e inverso da reao. Ao trmino da reao resta certa quantidade de reagente no transformado (rendimento inferior a 100 %). So comuns em transformaes orgnicas. ex.: esterificaes,...
Nestas reaes h uma velocidade direta, de formao de produtos, a qual vai decrescendo e uma velocidade inversa, de regenerao de reagentes, que vai aumentando, at o instante em que estas duas velocidades se tornam iguais. Este momento chamado EQUILBRIO, o qual pode ser homogneo ou heterogneo, em funo da composio do sistema: Exemplos: 2 NH3(g) N2(g) + 3 H2(g) (homogneo) (fase gasosa)
CH3COOH(aq) + C2H5OH(aq) CH3COOC2H5(aq) + H2O(l) (fase aquosa) (homogneo) CaCO3(s) CaO(s) + CO2(g) (heterogneo) (gases e slidos) (slido, lquido e gases)
6 CO2(g) + 6 H2O(l) C6H12O6(s) + 6 O2(g) (heterogneo) Para a reao homognea:
CO(g) + H2O(g)
CO2(g) + H2(g)
83
as variaes de concentrao de reagentes, produtos e das velocidades direta e inversa podem ser assim representadas:
Concentrao (mol/L) Reao com baixo rendimento
[CO] = [H2O]
[CO2] = [H2]
tempo Concentrao (mol/L) Reao com alto rendimento
[CO2] = [H2]
[CO] = [H2O]
tempo
84
velocidade
vdireta vdireta = vinversa
equilbrio qumico
vinversa
tempo
tempo decorrido para a reao entrar em equilbrio
Para uma reao genrica, em equilbrio: aA + bB xX + yY e (homognea)
vdireta = kdireta[A]a[B]b no momento do equilbrio
vinversa = kinversa[X]x[Y]y
vd = vi = kd[A]a[B]b = ki[X]x[Y]y isolando os termos semelhantes
x y d = [X] .[Y] = K k [A]a .[B]b c i
Kc = constante de equilbrio em funo de concentraes molares.
Quando dos componentes forem gasosos a constante de equilbrio pode ser calculada em funo das presses parciais exercidas pelas substncias gasosas, na seguinte forma:
Kp = constante de equilbrio em funo de presses parciais.
85
Como a presso parcial de um componente depende da sua concentrao em fase gasosa, podemos estabelecer a seguinte relao entre Kc e Kp:
Kp = Kc (RT)Dn
onde: R = constante geral dos gases T = temperatura absoluta Dn = diferena entre os coeficientes dos produtos e reagentes (gasosos) ***** Dn = (x + y) - (a + b) A constante de equilbrio tambm pode ser expressa em funo das fraes molares dos constituintes. Desse modo teremos:
y X x .X Kx = X Y X a .X b A B Kx = constante de equilbrio em funo de fraes molares
Do mesmo modo que Kc e Kp, a relao entre Kp e Kx pode ser estabelecida, resultando em
Kp = Kx . PD n
Nos equilbrios heterogneos, a constante de equilbrio no inclui os componentes slidos, porque a medida que a massa de um slido vai se reduzindo e transformando-se num produto o seu volume tambm reduz, mantendo constante a concentrao do mesmo.
Mas:
M = m1 / M . V
m1 / V =
M = m1 / M . V
m1 / V = const ant e
86
Portanto:
M
CaCO3(s) Kc = [CO2]
M
CaO(s) + CO2(g)
Kp = PCO2
4.4.2. Deslocamento do Equilbrio Qumico (Principio de Le-Chatelier fuga ante a fora) As reaes em estado de equilbrio podem sofrer modificaes nos mesmos em funo de trs fatores: - variaes nas concentraes de R ou P; - variaes na temperatura; - variaes na presso. Influncia das variaes nas Concentraes:
- a adio de um componente (R ou P) desloca o equilbrio no sentido do consumo dos mesmos; a remoo de um componente desloca o equilbrio no sentido de sua regenerao. Exemplo: sntese da amnia N2(g) + 3 H2(g) 2 NH3(g)
A constante de equilbrio ser obtida pela expresso: Kc = [NH3]2 / [N2].[H2]3 se adicionarmos, por exemplo, N2 ou H2, o denominador da expresso aumenta e a constante de equilbrio diminui; para que a constante assuma novamente o valor inicial o equilbrio desloca-se no sentido do consumo do reagente adicionado, formando mais produto e aumentando o valor de Kc;
se adicionarmos NH3 o numerador da expresso aumenta e a constante, tambm; para que a constante reduza seu valor a amnia em excesso dever ser decompor (parcialmente) formando H2 e N2, deslocando o equilbrio no sentido dos reagentes.
Resumindo: Se [N2] ento Kc ; o equilbrio se desloca para consumir N2
87
Se [NH3] ento Kc ; o equilbrio se desloca para consumir NH3 Influncia das variaes na Presso:
- o aumento da presso desloca o equilbrio (gasoso) no sentido do menor volume, ou seja, do menor nmero de mols; a reduo da presso desloca o equilbrio no sentido do maior volume, ou seja, do maior nmero de mols. Na formao da amnia, a partir do N2 e H2 ocorre uma diminuio no no de mols gasosos (contrao de volume):
contrao de volume
expanso de volume
N2g) + 3 H2(g)
2 NH3(g)
- se aumentarmos a presso o equilbrio ser deslocado no sentido da formao da amnia (menor nmero de mols e menor volume). Influncia das variaes na Temperatura:
- o aumento da temperatura, numa reao em equilbrio, desloca o mesmo no sentido Endotrmico; a reduo da temperatura (resfriamento), desloca o equilbrio no sentido Exotrmico do mesmo.
N2g) + 3 H2(g)
libera calor absorve calor
2 NH3(g)
DH < 0
Para obter um maior rendimento na produo de amnia devemos resfriar o sistema, o que provoca um deslocamento do equilbrio no sentido direto da reao.
88
4.4.3. INICO Neste caso, alm de espcies moleculares encontramos espcies inicas entre os componentes. o caso particular dos equilbrios de dissociao de cidos e bases fracas e da gua. *** Dissociao de cidos fracos. Num cido fraco a dissociao muito reduzida o que significa uma pequena quantidade de ons presentes e uma grande quantidade de molculas no dissociadas. ex.: HCN H+ + CN-
Ka = [H+] [CN-] / [HCN] = 4,0 . 10-10 -------------------------------------------------HCN HCN HCN HCN H
+
HCN CN
-
HCN HCN HCN H
+
HCN
HCN HCN CN
-
HCN HCN
HCN HCN
HCN
(predominncia de molculas) A soluo apresente pequena quantidade de ons disponveis sendo, portanto pouco cida quando comparada com outra de igual concentrao de um cido muito dissociado (ex. HCl). ex.: HCl H+ + ClKa @ 107
----------------------------------------------H H
+ + + +
Cl
-
Cl
+
H
-
Cl H
+
H Cl
-
Cl
+
Cl
HCl H Cl H
+
H Cl HCl
+
Cl
Cl Cl
-
H H
+
+ -
Cl
Cl
Cl
Cl
(predominncia de ons)
89
*** Dissociao de bases fracas. Com as bases sucede-se o mesmo que em relao aos cidos fracos. ex.: NH4OH NH4+ + OH-
Kb = [NH4+] [OH-] / [NH4OH] = 4,2 . 10-4 Obs.: quanto menor o valor de Ka ou Kb mais fraco o cido ou a base! *** Lei da Diluio de Ostwald (1893) Quando adicionamos um solvente (por exemplo, gua) a uma soluo de um cido ou base fraca o seu grau de dissociao (a) aumenta e, portanto, tal parmetro no totalmente adequado para caracterizar a fora de um cido ou de uma base. No entanto a constante de dissociao (Ka ou Kb) ser um critrio mais confivel visto que a mesma no se modifica com a diluio. A relao entre a constante de dissociao (Ka ou Kb), a concentrao molar e o grau de dissociao (a) pode ser estabelecida a partir do seguinte. Considere a dissociao genrica de um cido (ou base) fraca: HA [ HA ] M M - aM aM H+ [ H+ ] aM + A[ A- ] aM
Inicio Equilbrio Dissocia
A constante de dissociao (Ka) ser obtida por: ou, ainda, Ka = [ H+ ] . [ A- ] / [ HA ] = (aM) . (aM) / M - aM Ka = a2 M / 1 - a
Quando o valor da constante de dissociao (Ka ou Kb) for muito pequeno, o que indica fraca dissociao do cido ou da base, o denominador da frao (1 - a) ser, aproximadamente igual a 1,0 (um) e, portanto a expresso se resume a Ka = a2 M
90
Exemplo: calcule o grau de dissociao do cido actico (CH3COOH), para uma concentrao molar 0,5 mol/litro, sabendo que a sua constante de dissociao (Ka) vale 1,85 . 10-5. Resposta: a = 6,1 . 10-3 ou a% = 0,61 % *** Dissociao da gua. A gua dissocia-se fracamente, segundo o equilbrio: H2O H+ + OH-
Medidas de Condutividade Eltrica permitem estabelecer o valor desta constante, Kgua Kgua = [H+] [OH-] / [H2O] = 1,81 . 10-16 (250 C e 1 atm) Como a dissociao muito pequena, pode-se admitir que a concentrao molar da gua constante e vale 55,55.. mol/L. Lembrando: **M = m1/ M1 .V Portanto: Kgua [55,55..] = [H+][OH-] = 1,81.10-16 . 55,55 = 1,001.10-14 @ 10-14 Kw = Produto inico da gua = 10-14 (250 C e 1 atm) como [H+] = [OH-] 10-7 mols/litro (gua pura) (para V = 1,0 litro e m1 = 1000 g = 1,0 kg)
I - para solues cidas: [H+] > [OH-] [H+] < [OH-] ex.: [H+] = 10-5 e [OH-] = 10-9
II - para solues bsicas: ex.: [H+] = 10-11 e [OH-] = 10-3
4.4.4. Conceitos de pH e pOH Em 1909, o qumico dinamarqus, Soren Peer Lauritz Srensen, para evitar o uso de expresses matemticas com expoentes negativos, props um artificio matemtico, introduzindo os conceitos de pH e pOH:
91
pH = potencial Hidrogeninico = - log10 [H+] pOH = potencial Hidroxilinico = - log10 [OH-] Estes conceitos permitem expressar a acidez ou alcalinidade de solues diludas (entre os limites de 1,0 mol/L para os ons H+ ou OH-). Assim: - na gua pura: [H+] = 10-7 pH = 7 - numa soluo cida: [H+] = 10-3 pH = 3 e [OH-] = 10-11 pOH = 11 e [OH-] = 10-7 pOH = 7
- numa soluo alcalina: [H+] = 10-14 pH = 14 e [OH-] = 100 = 1,0 pOH = 0
Obs.:
- quando o cido ou a base forem fortes [H+] = [cido] e [OH-] = [base]; - Kw = Produto inico da gua = 10-14 (constante) = [H+][OH-]; - pH + pOH = 14; - assim como o equilbrio qumico, tambm o equilbrio inico pode ser deslocado, valendo os mesmos princpios.
4.4.5. Reaes de Hidrlise Quando um sal dissolvido em gua, verifica-se que a soluo resultante pode ser neutra, cida ou bsica, devido possibilidade de reao de hidrlise do sal. Hidrlise a reao inversa neutralizao, ocorrendo com sais derivados de cidos ou bases fracas. Na realidade a hidrlise ocorre com o on derivado do cido ou da base fraca, ocorrendo a liberao de ons H+ ou OH-.
92
a) hidrlise de sal derivado de cido forte com base fraca. NH4Cl + H2O NH4+ + H2O NH4OH + HCl NH4OH + H+
(cido forte)
on hidrognio liberado (diminui o pH)
b) hidrlise de sal derivado de cido fraco com base forte. NaHCO3 + H2O NaOH + H2CO3
principal constituinte do sal de frutas
(base forte) H2O + CO2
HCO3- + H2O
H2CO3 + OH
o on hidroxila liberado (aumenta o pH)
A hidrlise modifica o pH das solues !!!
Em resumo:
- sal de cido forte - sal de base forte
soluo cida (pH < 7) soluo bsica (pH > 7)
Exerccio. Escreva as equaes de hidrlise dos sais abaixo, indicando a tendncia do pH resultante: NaNO3 CuSO4 KCN NaCl CaCO3 NH4Cl
93
4.4.6. DESLOCAMENTO DO EQUILBRIO INICO (Efeito do on comum) Do mesmo modo como foi visto no equilbrio qumico, o inico tambm pode se deslocado sendo que a forma mais freqente de deslocamento pela adio de uma espcie inica comum (e, s vezes, no-comum) ao equilbrio, correspondendo adio ou retirada de um componente, na comparao com o deslocamento do equilbrio qumico. Assim, considerando a dissociao de um cido fraco, como o HCN:
HCN(aq)
H+(aq) + CN-(aq)
a) se adicionarmos um cido qualquer a essa soluo, a adio de ons H+ ir deslocar o equilbrio no sentido de consumi-lo, diminuindo a dissociao do HCN; b) se adicionarmos NaCN, o on Na+ no ir exercer efeito significativo ao sistema mas o ion CN-, por ser comum ao equilbrio tambm ir desloclo no sentido de diminuir a dissociao do HCN. Nesse caso, como conseqncia, tambm ir diminuir a acidez da soluo em virtude do consumo dos ons H+.
HCN(aq)
Exerccio
H+(aq) + CN-(aq)
Qual o efeito da adio de NH4Cl sobre o equilbrio da dissociao do hidrxido de amnio (NH4OH) ? Tambm merece ser analisado o deslocamento provocado pela adio de um on no-comum ao equilbrio, mas que possa provocar algum tipo de reao com ons presentes no mesmo. Considerando, por exemplo, a dissociao da base fraca NH4OH.
NH4OH(aq)
NH4+(aq) + OH-(aq)
Se adicionarmos ons comuns ao equilbrio (NH4+ ou OH-) o mesmo ir se deslocar no sentido de reduzir a dissociao da base fraca. No entanto se adicionarmos ao sistema um cido qualquer, ou seja, ons H+, estes iro consumir os ons OH-, pela formao de H2O, deslocando o equilbrio no sentido de regenerlos, aumentando a dissociao do NH4OH e, consequentemente, a concentrao de ons NH4+ na soluo, representado conforme abaixo:
NH4OH(aq)
NH4+(aq) + OH-(aq)
94
4.4.7. CIDOS E BASES DE BRNSTED LOWRY E LEWIS A definio de cidos e bases, em funo dos ons H+ e OH- em gua, proposta por Arrhenius, muito restrita, porque limita a discusso do fenmeno cido-base somente a solues aquosas. Alm do conceito de S. Arrhenius sobre cidos e bases, em 1923, os fsicoqumicos J. Brnsted (Dinamarca) e H. Lowry (Inglaterra), independentemente, propuserem uma teoria mais ampla relativa aos conceitos de cidos e bases, aplicvel a qualquer solvente (no apenas gua) e alguns ons. Outra abordagem foi proposta, em 1917, pelo americano G. Lewis. a) Teoria Protnica (Brnsted-Lowry) Segundo essa teoria : - cidos = qualquer espcie qumica que libera ou doa prtons (H+); - bases = qualquer espcie qumica que recebe prtons (H+). Tais conceitos evidenciam-se em sistemas inicos em equilbrio, sendo: Assim, nos equilbrios abaixo:
cido 1
HCl
+ + +
base 1
H2O
cido 2
H3O+
+ + +
base 2
Cl-
cido 1
HCN
base 1
H2O
cido 2
H3O+
base 2
CNOH-
base 1
NH3
cido 1
H2O
cido 2
NH4+
base 2
O conceito de Brnsted-Lowry mais geral do que o conceito de Arrhenius, porque no se restringe a solues aquosas, sendo que podemos encontrar reaes cido-base que ocorrem at mesmo sem a presena de um solvente. Observaes importantes sobre a Teoria Protnica *** as espcies que diferem entre s de apenas um prton (H+) so chamadas de conjugados ou pares conjugados (HCl e Cl- ; H2O e H3O+,...); *** substncias que, em funo da reao que participam, podem comportarse tanto como cidos ou bases ( o caso da gua no 10 e 30 exemplos) so denominadas anfiprticas. *** nos conjugados se o cido forte a base conjugada fraca e se o cido fraco a base conjugada forte.
95
b) Teoria Eletrnica (Lewis) Segundo essa teoria a ateno principal focalizada na base, sendo definida como uma substncia que pode doar um par de eltrons para formar a ligao covalente e o cido como a substncia que pode aceitar um par de eltrons para formar a ligao. Neste sentido molculas que doam eltrons atravs de ligaes coordenadas ou dativas sero consideradas bases segundo a teoria de Lewis. Destacam-se a amnia (NH3), as aminas (R NH2), as amidas (R CO NH2) e as espcies aninicas (Cl-, Br-, I-, OH-, etc). Como cidos, destacam-se as espcies catinicas (H+, Na+, Ca++, etc) e molculas deficitrias de eltrons , isto , que no completam o octeto (BF3, AlCl3, etc). Exemplo:
BF3 + :NH3 5 . Ex e r c c i o s
cido
BF3
base
:NH3
1) A reao reversvel em fase gasosa: CO + H2O CO2 + H2 admite os seguintes valores para a constante de equilbrio Kc T (o C) Kc 225 0,007 425 0,109 625 0,455 825 1,080 995 1,760
Partindo-se de uma mistura equimolar de CO e H2O: a) quais os compostos predominantes no equilbrio, a 225o C ? b) em qual das temperaturas mencionadas as concentraes dos reagentes e dos produtos, no equilbrio, so aproximadamente iguais ? 2) Considere a seguinte equao de oxi-reduo: Ce+4aq) + Fe+2(aq) Ce+3(aq) + Fe+3(aq) A constante de equilbrio da reao igual a 2,0 . 1011. a) Escreva a expresso que representa a constante de equilbrio. b) Calcule a concentrao de ons Ce+4 que existe em equilbrio em uma soluo cuja concentrao de Ce+3 0,1 mol/L, de Fe+3 0,1 mol/L e a de Fe+2 0,1 mol/L. Resposta: b) 5,0 . 10-13 mol/L
96
3) Um mol de H2 e um mol de Br2 so colocados em um recipiente de 10 L de capacidade, a 575o C. Atingindo-se o equilbrio a anlise do sistema mostrou que 0,20 mol de HBr est presente. Calcule o valor da constante Kc. 4) Se 1,0 mol de H2 e 1,0 mol de I2, em um recipiente de 1,0 litro, atingirem a condio de equilbrio, em temperatura adequada, observa-se que a constante do mesmo vale 49,0. Qual a concentrao de HI no equilbrio ? Resposta: 1,54 mol/L 5) N2O4 e NO2, gases poluentes do ar, encontram-se em equilbrio, como indicado na equao: N2O4(g) 2 NO2(g). Em uma experincia, nas condies ambientes, introduziu-se 1,50 mol de N2O4 em um recipiente de 2,0 litros. Estabelecido o equilbrio, a concentrao de NO2 foi de 0,060 mol/L. Qual o valor da constante desse equilbrio ? Resposta: 5,0 . 10-3 mol/L 6) Em um recipiente de 1,0 litro, colocou-se 1,0 mol de PCl5. Em fase gasosa, o PCl5 se decomps em PCl3 e Cl2, em temperatura tal que o reagente se encontra 80% dissociado. Qual a constante de equilbrio desse sistema ? Resposta: 3,20 mols/L 7) Bicarbonato cido de sdio slido usado como fermento qumico porque se decompe termicamente, produzindo gs carbnico, de acordo com a reao representada pela equao: 2 NaHCO3(s) Na2CO3(s) + CO2(g) + H2O(g). a) Escreva a expresso matemtica para a constante de equilbrio em termos das presses parciais (Kp); b) A constante de equilbrio, em termos das presses parciais, vale 0,25 atm2, na temperatura de 125o C, quando as presses so medidas em atmosferas. Quais as presses parciais do CO2 e da H2O no equilbrio ? Resposta: ambas 0,5 atm. 8) A equao qumica no balanceada: C6H12O6 + NO3- + H+ CO2 + H2O + N2 representa a reao que ocorre em solos pouco aerados e envolve a reduo de nitrato a nitrognio, em meio cido, em presena de carboidratos. O fenmeno, conhecido como desnitrificao, prejudica a fixao de NO3- pelas plantas. Assinale e apresente uma justificativa, qual das alternativas abaixo, representa uma espcie qumica capaz de aumentar a concentrao do NO3no equilbrio. a) adicionar ons OH-. b) adicionar ons H+. c) absorver CO2. d) reagir com N2. e) consumir gua.
97
9) A reao de transformao do dixido de carbono em monxido de carbono, representada pela equao abaixo, muito importante em certos processos metalrgicos: C(s) + CO2(g) 2 CO2(g) DH = 174 kJ/mol de C Qual o efeito sobre o equilbrio se: a) adicionarmos C slido ? b) aumentarmos a temperatura ? c) introduzir um catalisador adequado a essa reao ? 10) Uma das causas de incndios em florestas a combusto espontnea de compostos orgnicos, genricamente representada a seguir: composto orgnico + O2(g) CO2(g) + H2O(v) + calor Observe que o deslocamento do ponto de equilibrio da reao pode tornar a combusto mais intensa. Dois fatores, entre outros, que podem contribuir para tal fato so: 1o) o aumento da presso parcial de O2; 2o) a baixa umidade relativa do ar em dias quentes. Explique porque esses dois fatores deslocam o equilbrio no sentido da combusto ? 11) Em um recipiente de 500 mL encontram-se em equilbrio 0,48 gramas de NO2 e 2,0 gramas de N2O4, segundo a equao: 2 NO2(g) N2O4(g). Qual a constante de equilbrio ? Resposta: K = 0,01 L/mol. 12) Partindo de 0,388 mol/L de NOCl, 475 K, a reao: 2 NOCl 2 NO + Cl2 produz 0,02 mol/L de Cl2, ao atingir o equilbrio. Calcular Kc. Resposta: Kc = 2,64 . 10-4 mol/L 13) O valor assumido pela constante de equilbrio de uma reao nos d uma idia de sua extenso, isto , do avano dos reagentes em direo dos produtos. Que relaes podemos fazer entre o rendimento de uma reao e um a) valor elevado de constante Kc ? b) valor reduzido de constante Kc ? 14) A constante de equilbrio em funo das presses parciais, para uma reao gasosa, pode ser calculada a partir de grandezas termodinmicas, particularmente a Energia de Gibbs, segundo a expresso: Kp = e
- G
RT
Para a reao gasosa: 2 NO2(g) N2O4(g) a variao de energia de Gibbs, em condies padro vale 140,00 kJ/mol. Calcule a constante Kp. Resposta: 3,0 . 1024
98
15) Metanol, CH3OH, obtido comercialmente pela reao abaixo: CO(g) + 2 H2(g) CH3OH(g) A uma certa temperatura o valor da constante de equilbrio, Kc, numericamente igual a 7,3. Em que sentido a reao ser deslocada quando a mistura inicial contiver a) 0,80 mol/L de CO e 1,5 mol/L de H2 ? b) uma mistura gasosa de de 0,90 mol de metanol, 0,45 mol de CO e 0,45 mol de H2, num recipiente de 3,0 L ? 16) O cido clordrico pode ser considerado como totalmente dissociado em soluo aquosa. Se um volume de 10 litros de soluo desse cido contm 102 mols de cido dissolvidos, qual o valor do pH ? Resposta: pH = 3 17) Foram adicionados 99 litros de gua destilada a 1,0 litro de uma soluo de NaOH, de concentrao 0,1 mol/L. Qual o pH da soluo alcalina aps a diluio? Resposta: pH = 11 18) O cido carbnico apresenta uma fraca dissociao, observada pelo reduzido valor da sua constante de dissociao, Ka = 4,2 . 10-7. Qual a concentrao, aproximada dos ons H+, considerando-o como um monocido, partindo de uma soluo inicial 0,1 mol/L desse cido ? 19) cido ctrico 8,6% dissociado em uma soluo preparada pela dissoluo de 0,1 mol desse cido para 1,0 litro de soluo final. Calcule Ka para o cido ctrico. Resposta: 8,1 . 10-4 20) O bicarbonato de sdio (NaHCO3) incorretamente chamado de carbonato cido de sdio, pela presena de hidrognio na frmula. Esse sal o principal constituinte dos anticidos estomacais do tipo sal de frutas. Explique porque o mesmo atua como anticido no nosso organismo. De que modo o equilbrio de dissociao do bicarbonato afetado pelos ons H+ presentes no suco gstrico ? *** Testes de nivelamento (no sero corrigidos ou comentados) 1 - A tabela abaixo fornece os valores das constantes de ionizao de alguns cidos, em soluo aquosa e 250C. cido fluordrico actico ciandrico frmico Ka 6,70 . 10-4 1,76 . 10-5 4,93 . 10-10 1,77 . 10-4
99
A anlise dos dados da tabela permite afirmar que A) para solues aquosas de mesma concentrao, o pH do cido actico menor do que o frmico. B) entre os cidos apresentados, o mais forte o ciandrico. C) a concentrao de ons H+ maior na soluo de cido ciandrico do que na de cido fluordrico, em solues de mesma concentrao. D) o cido actico mais fraco que o fluordrico. E) as solues aquosas de qualquer um desses quatro cidos apresentam pH maior do que 7,0. 2 - Numa dada temperatura aqueceram-se 6,0 mols de HI num recipiente fechado. Ao se estabelecer o equilbrio H2 + I2 2 HI verificou-se a presena de 1,5 mols de HI. O grau de dissociao do HI, na temperatura dada, A) 15% B) 25% C) 60% D) 75% E) 85% 3 - Uma soluo aquosa A tem pH igual a oito e uma soluo aquosa B tem pH zero. Isto significa que as solues A e B so, respectivamente, A) fracamente alcalina e fortemente cida. B) fracamente alcalina e neutra. C) fortemente alcalina e fracamente cida. D) fracamente cida e fracamente alcalina. E) fortemente cida e neutra. 4 - Na ionizao do cido clordrico em soluo aquosa, representada por HCl + H2O H3O+ + Cla gua se comporta como A) um cido de Brnsted-Lowry. B) uma base de Brnsted-Lowry. C) um cido de Arrhenius. D) uma base de Arrhenius. E) um cido de Lewis. 5 - Em um sistema qumico isotrmico ocorre a reao genrica reversvel A(aq) + B(aq) C(aq) + D(aq) Partindo-se de 3 mols de A e de 3 mols de B, verifica-se que, atingindo o equilbrio, a quantidade de A presente no sistema 1/3 da quantidade inicial. A constante de equilbrio Kc para esse sistema A) 9 B) 4 C) 2 D) 1/2 E) 1/4
6 - O pH de uma soluo aquosa onde a concentrao de ons hidroxila de 0,01 mol/L igual a A) 0,01 B) 2 C) 10 D) 12 E) 13,99
100
7 - Se a concentrao de ons hidroxila, em uma soluo aquosa, for reduzida a um dcimo do valor original, o pH da soluo A) aumentar de 10 unidades. B) permanecer inalterado. C) ser reduzido metade. D) aumentar de 1 unidade. E) diminuir de 1 unidade. 8 - A reao qumica que apresenta constante de equilbrio genericamente representada por Kc = [X] / [Y].[Z]1/2 ser A) B) C) D) E) C(s) e O2(g) H2(g) e O2(g) N2(g) e O2(g) SO2(g) e O2(g) P4(s) e O2(g)
REAGENTES PRODUTO
CO2(g) H2O2(l) NO(g) SO3(g) P2O5(s)
9 - Dentre os sistemas em equilbrio apresentados abaixo, o que se desloca da direita para a esquerda quando se faz diminuir a presso 2 CO2(g) A) 2 CO(g) + O2(g) B) 2 NH3(g) N2(g) + 3 H2(g) C) N2O4(g) 2 NO2(g) D) CO2(g) + H2(g) CO(g) + H2O(g) E) CaCO3(s) CaO(s) + CO2(g) 10 - A nica das espcies abaixo que, ao ser dissolvida em gua, resulta em uma soluo com pH menor do que o solvente puro A) NaCl B) Na2CO3 C) CaCl2 D) NH3 E) (NH4)2SO4 11 - Uma constante de equilbrio elevada significa que A) o equilbrio atingido rapidamente. B) a velocidade da reao direta muito maior do que a velocidade da reao inversa. C) a concentrao dos reagentes ser bem menor que a de produtos da reao ao ser atingido o equilbrio. D) a reao irreversvel. E) o equilbrio no pode ser deslocado por modificao das concentraes. 12 - Ao adicionarem-se 99 mL de gua a 1,0 mL de NaOH 0,01 M, verifica-se que o pH da soluo A) no se altera. B) aumenta de 2 para 4. C) diminui de 10-2 para 10-4. D) aumenta de 10-2 para 102.
101
E) diminui de 12 para 10. 13 - A sntese da amnia e a sua decomposio constituem um exemplo de equilbrio qumico: N2(g) + 3 H2(g) 2 NH3(g) Como industrialmente deseja-se a reao de sntese, uma prtica recomendvel para se conseguir um maior rendimento de amnia, apenas com as informaes disponveis acima, A) adicionar um catalisador. B) aumentar a presso sobre o sistema. C) elevar a temperatura. D) retirar o excesso de hidrognio. E) trabalhar com nitrognio lquido. 14 - Quando se dissolve um mol de hidrxido de sdio em um litro de gua destilada, resulta uma soluo na qual a espcie de menor concentrao A) Na+ B) OHC) H2O D) NaOH E) H3O+ 15 - Quando se dissolvem certos sais em gua pode ocorrer que a relao entre a concentrao de ons hidrognio (H+) e a concentrao de ons hidroxila (OH-) seja alterada. Assim, dados os sais abaixo: 1 - carbonato de clcio 2 - sulfato de sdio 3 - cloreto de amnio 4 - cloreto de potssio 5 - acetato de sdio 6 - sulfato de alumnio podemos corretamente classific-los como: (A) (B) (C) (D) (E) [H+] > [OH-] [H+] = [OH-] [H+] < [OH-] 1 e 5 2 e 4 3 e 6 3, 4 e 6 1, 2 e 5 ........... ......... 2, 3 e 4 1, 5 e 6 3 e 6 2 e 4 1 e 5 2, 3 e 6 .......... 1, 4 e 5
16 - As leis de proteo ambiental de certas cidades no permitem o lanamento em rios, entre outros, de efluentes com pH inferior a 5,0 ou superior a 9,0. No que se refere acidez, os efluentes aquosos das indstrias X, Y e Z apresentam as seguintes concentraes: Indstria X Y Z Concentrao no efluente 10-3 M de H+ 10-4 M de H+ 10-6 M de OH-
102
Poderiam ser lanados em rios, sem tratamento prvio, apenas os efluentes de A) X B) Y C) Z D) X e Y E) Y e Z 17 - Recolheu-se uma amostra de gua da chuva e verificou-se que apresentava pH = 5,0. Se quisermos neutralizar 1,0 litro desta amostra com uma soluo de KOH 0,01 M, o volume de base consumido, em mL, ser A) 0,001 B) 0,01 C) 0,05 D) 1,0 E) 5,0 18 - O indicador tornassol apresenta cor rosa em meio cido e azul em meio bsico, ocorrendo a troca de cor quando a concentrao de H+ est na faixa de 105 a 10-7 M. Assinale a alternativa que apresenta a combinao correta do valor do pH da soluo e a cor do indicador a ela adicionado. A) B) C) D) E)
SOLUO FAIXA DE pH COR DO INDICADOR suco de limo 2,2 a 2,4 azul vinagre 2,6 a 3,0 azul suco de laranja 3,0 a 4,0 rosa gua do mar 8,2 a 8,3 rosa detergente com 11,8 a 12,4 rosa amonaco
19 - Tem-se duas solues aquosas I - soluo de NaOH 0,01 mol/litro II - soluo de HCl 0,01 mol/litro o quociente pH da soluo I / pH da soluo II igual a A) 1 B) 6 C) 10 D) 10-2 E) 10-10
20 - Em uma soluo aquosa de cido actico se estabelece o seguinte equilbrio H+ + CH3COOCH3COOH a adio de uma pequena quantidade de acetato de sdio (CH3COONa) a esta soluo A) diminui o seu pH. B) aumenta a concentrao dos ons H+. C) diminui o grau de ionizao do cido. D) mantm inalterado o pH. E) reduz a zero o grau de ionizao do cido actico.
103
21 - O volume, em mL, de uma soluo de cido clordrico de pH = 2, necessrio para neutralizar completamente 500 mL de uma soluo de hidrxido de potssio de pH = 11 de A) 13. B) 50. C) 100. D) 500. E) 2275. 22 - Conhecendo-se o valor da constante de equilbrio (Kc), pode-se determinar a probabilidade de uma dada reao ocorrer na natureza. Considere duas reaes possveis para a fixao do nitrognio atmosfrico, convertendo-o em compostos utilizveis pelos seres vivos.
I. N2(g) + O2(g) II. N2(g) + 3 H2(g) 2 NO(g) Kc = 1,0 . 10 a 25 C 8 0 2 NH3(g) Kc = 5,0 . 10 a 25 C
-30 0
Para uma fixao eficiente de N2, correto afirmar-se que A) a reao I no seria um processo adequado, pois a concentrao de NO no equilbrio seria extremamente pequena. B) a reao II no seria um processo adequado, pois o sistema em equilbrio consistiria, praticamente, no produto NH3. C) a reao I seria um processo adequado, pois esta reao tende a se processar no sentido da formao do NO. D) a reao II seria um processo adequado, pois no equilbrio so grandes as concentraes de N2 e H2. E) as duas reaes so processos adequados, pois quando o equilbrio atingido nas duas reaes, grande a concentrao dos produtos. 23 - Nas seguintes equaes: KOH + HCl KCl + H2O A HCl + NH3 NH4Cl B HCN + NaOH NaCN + H2O C as solues aquosas dos compostos A, B e C apresentam, respectivamente, um pH A) > 7; = 7; > 7 B) < 7; = 7; < 7 C) < 7; < 7; > 7 D) < 7; > 7; = 7 E) < 7; < 7; < 7 24 - O pH de uma soluo aquosa de cido clordrico cuja concentrao igual a 10-9 mol/L aproximadamente igual a
104
A) 1 B) 3 C) 5 D) 7 E) 9 25 - O acetato de etila um ster muito usado como solvente de vernizes. Em um recipiente de um litro, foram misturados um mol de acetato de etila e um mol de gua. Os compostos reagiram entre s formando etanol (lcool comum) e cido actico, de acordo com a equao C4H8O2 + H2O C2H5OH + C2H4O2
Depois de algum tempo, o sistema atingiu o equilbrio; o nmero de mols de ster medido foi de 0,66. O valor, aproximado, da constante de equilbrio A) 0,26 B) 1,00 C) 1,50 D) 2,60 E) 3,76 26 - Para o cultivo de azalias, o pH ideal entre 4,0 e 5,0. A anlise do solo de um jardim mostrou que o mesmo apresenta um pH igual 6,0. O composto ideal para adequar o solo ao plantio das azalias A) Al2(SO4)3 B) CaCO3 C) CaO D) NH3 E) NaOH 27 - Considere o equilbrio qumico que se estabelece em uma soluo aquosa de cido actico que pode ser representado pela equao CH3 COO-(aq) + H+(aq) CH3 COOH(aq) Mantendo-se constante a temperatura e adicionando-se uma soluo aquosa de acetato de sdio (CH3 COONa), incorreto afirmar que A) o equilbrio se desloca para a esquerda. B) aumenta a concentrao de cido actico. C) aumenta a concentrao do on CH3 COO-. D) diminui a concentrao do on H+. E) altera o valor numrico da constante de equilbrio. 28 - Um equilbrio envolvido na formao da chuva cida est representado pela equao: 2 SO3(g) 2 SO2(g) + O2(g) Em um recipiente de 1,0 litro, foram misturados 6 mols de dixido de enxofre e 5 mols de oxignio. Depois de algum tempo, o sistema atingiu o equilbrio; o nmero de
105
mols de trixido de enxofre medido foi 4. O valor aproximado da constante de equilbrio A) 0,53 B) 0,66 C) 0,75 D) 1,33 E) 2,33 29 - Considere as seguintes equaes, que representam situaes de equilbrio qumico a 298 K. I. N2 + 3 H2 2 NH3 Kp = 6,8 . 105 II. H2 + I2 2 HI Kp = 7,94 . 102 III. N2O4 2 NO2 Kp = 0,98 A) B) C) D) E) A concluso correta que se pode extrair dessas informaes que a reao I e a mais rpida das trs. a reao II praticamente no ocorre no sentido direto a 298 K. a reao II apresenta velocidade moderada. apenas a reao III atinge o equilbrio a 298 K. a reao I atinge o equilbrio com grande quantidade relativa de produtos.
30 - O acidente ocorrido recentemente com o navio Bahamas provocou o vazamento de milhares de toneladas de cido sulfrico na lagoa dos Patos. Em determinados locais, foram registrados valores de pH entre 3 e 4. Podemos afirmar que, nesses locais, a concentrao aproximada de ons hidroxila, em mol/L, foi A) maior do que 10-11. B) maior do que 10-9. C) maior do que 10-7. D) maior do que 10-5. E) maior do que 10-4.
106
5 . REFERN CI A S B I B L I OGR FI CA S
1. BRADY, J. E & HUMISTON, G. E. QUMICA GERAL . LTC Editora.1996. So Paulo. 2. MAHAN , B & MYERS, R. J. QUMICA UM CURSO UNIVERSITRIO. Editora Edgard Blcher. 3 ed. 1995. So Paulo. 3. ATKINS, P & JONES, L. PRINCPIOS DE QUMICA. Bookman Companhia Editora. 2001. Rio de Janeiro. 4. ANDRADE, M. A. G. FSICO-QUMICA. s ed. mimio. PUCRS. 2001.
107
GA B A RI T OS T EST ES DE N I V EL A M EN T O 1 . SOL U ES 01 B 02 D 03 A 04 B 05 C 06 D 07 A 08 B 09 D 10 C 11 B 12 D 13 D 14 C 15 C 16 D 17 A 18 A 19 E 20 B 21 B 22 B 23 C 24 B 25 D 26 B 27 B 28 E 29 D 30 A 2 . EFEI T OS COL I GA T I V OS 01 A 02 B 06 B 07 C 3 . T ERM OQU M I CA 01 C 06 B 11 B 16 C 02 E 07 D 12 C 17 C 03 C 08 A 03 E 08 C 13 E 18 D 03 D 08 B 13 B 18 A 04 E 09 E 04 D 09 C 14 B 19 C 04 B 09 C 14 B 19 C 04 B 09 A 14 D 19 B 24 D 29 E 05 E 10 E 05 A 10 D 15 A 20 A 05 D 10 B 15 C 20 D 05 B 10 E 15 D 20 C 25 A 30 - A
3 . CI N T I CA QU M I CA 01 E 02 E 06 C 07 C 11 E 12 C 16 D 17 D
4 . EQU I L B RI O QU M I CO E I N I CO 01 D 02 D 03 A 06 D 07 E 08 D 11 C 12 E 13 B 16 C 17 D 18 C 21 B 22 A 23 C 26 A 27 E 28 D
108
ATIVIDADES EXPERIMENTAIS
Disciplina: QUMICA GERAL E INORGNICA II Prof. M. Sc. Mateus A. G. Andrade 1. INTRODUO
1.1. OBJETIVOS DAS AULAS EXPERIMENTAIS Consideramos que, alm da familiarizao do aluno com operaes e tcnicas mais freqentes nos processos qumicos, j iniciada nas atividades experimentais de Qumica Geral I, importante o trabalho experimental com metodologias analticas (sem esgot-las), tendo em vista um dos objetivos do curso de Qumica que visa a preparao do profissional qumico analista. Tais conhecimentos bsicos constituiro o requisito para as disciplinas de Qumica Analtica (Qualitativa e Quantitativa). 1.2. INSTRUES GERAIS Ratificamos em nossa disciplina algumas instrues enfatizadas em Qumica Geral I, as quais devem ser levadas em considerao em todas as demais disciplinas do curso, entre as quais destacamos: I - no ser permitida a permanncia de alunos sem avental no laboratrio. O avental deve ser de cor branca, com mangas compridas e seu comprimento dever atingir a altura dos joelhos, confeccionados em tecido de algodo pois este mostrase mais adequado do que os tecidos sintticos por ser mais resistente ao fogo. II - alm do uso obrigatrio do avental, sugere-se, por medida de segurana, que o aluno tenha um culos de proteo e luvas de borracha para uso na preparao de solues corro sivas. oportuno, outrossim, que o aluno tenha um caderno de anotaes onde dever ser registrado o incio e o trmino de cada exprimento, assim como observaes e concluses, pois seu professor dever abster-se completamente de concluir qualquer dos experimentos, porm dever conduzir o raciocnio e a observao do aluno.
109
1.3. INSTRUES PARA O TRABALHO PRTICO Durante os trabalhos experimentais devero ser observados rigorosamente os seguintes aspectos: 01) prepare-se para realizar cada experimento lendo antes as instrues correspondentes. Siga as instrues e respeite rigorosamente as precaues recomendadas. Consulte seu professor cada vez que notar algo de anormal ou imprevisto; 02) no fume no laboratrio; 03) faa apenas o experimento recomendado e aprovado pelo professor; 04) separe os materiais necessrios e, se estiver em grupo, divida as tarefas entre seus colegas; 05) leia com ateno o rtulo do reagente antes de us-lo; 06) se qualquer cido ou produto corrosivo for derramado lave o local imediatamente com bastante gua; 07) caso voc encoste em algum cido forte limpe sua pele imediatamente com gua corrente ou soluo de bicarbonato de sdio (NaHCO3); 08) se o mesmo ocorrer com alguma base forte, limpe sua pele com gua corrente ou soluo de cido actico; 09) no toque com os dedos nos produtos qumicos, a menos que receba instrues para faz-lo; 10) para sentir odor de uma substncia, no coloque seu rosto diretamente sobre o recipiente. Em vez disto traga um pouco do vapor para voc, com sua mo; 11) tenha cuidado com os materiais inflamveis, nunca aquea um lquido inflamvel com o bico de gs, use uma manta de aquecimento ou banho-maria aquecido por resistncia eltrica; 12) qualquer incndio deve ser abafado imediatamente com um pano mido ou, dependendo da extenso do mesmo, atravs de extintores. Procure identificar a localizao e o tipo de extintor prximo; 13) caso ocorra um acidente (queimadura com fogo, salpique de produtos nos olhos, etc..) procure os dispositivos de segurana nos laboratrios; 14) trabalhe com calma, pacincia e sabedoria. 1.4. ALGUNS REAGENTES E SUAS CARACTERSTICAS Sempre que manusear compostos volteis (HCl, NH4OH, HNO3, benzeno,etc..) faa-o em local com boa ventilao ou em capela preferencialmente. Quando diluir um cido forte, adicione primeiro a gua e depois o cido!!!
110
a) cido clordrico concentrado: - formado por molculas de HCl gasoso, dissolvidas em gua. Comercialmente encontrado com impurezas e denominado de cido muritico. Como o cido clordrico apresenta alta tenso de vapor as molculas do mesmo podem facilmente escapar do lquido, reduzindo a concentrao do cido no frasco-depsito. Por esta razo o frasco deve estar bem fechado aps seu uso. Os vapores de cido clordrico so txicos e, portanto, no devem ser inspirados. b) cido ntrico concentrado: - cido forte e excelente agente oxidante. Deve ser utilizado com muito cuidado pois voltil e em contato com a pele provoca srias queimaduras. c) cido sulfrico concentrado: - cido forte e agente altamente desidratante. No voltil mas seu contato com a pele causa srias queimaduras. Sua dissoluo em gua altamente exotrmica (libera calor) e, portanto, deve ser feita com cuidado e sob constante resfriamento. d) Hidrxido de amnio concentrado: - apesar de no ser uma base forte seus vapores causam srias irritaes nas mucosas (principalmente oculares). Por serem txicos os seus vapores, do mesmo modo que o cido clordrico, o frasco deve estar bem fechado aps seu uso. e) Benzeno: - hidrocarboneto aromtico, de odor agradvel, vapores txicos e altamente inflamveis. Quando manuse-lo certifique-se que no h bicos de gs acesos prximos. O mesmo cuidado deve ser tomado no manuseio do ter etlico. 1.5. REAGENTES E SOLUES Os reagentes empregados em laboratrio em geral apresentam-se sob a forma de solues. O acondicionamento das solues feito em frascos de vidro os quais devem apresentar resistncia qumica ao ataque dos materiais neles contidos. As solues alcalinas, especialmente, atacam o vidro formando silicatos. Por esta razo equipamentos de preciso (buretas, pipetas volumtricas, etc..) no devem receber solues alcalinas. Da mesma forma que os reagentes slidos, as solues devem estar protegidas da contaminao externa. conveniente utilizar um frasco de tampa achatada com bordas cobrindo a boca do gargalo para proteger da poeira. Pores de solues retiradas do frasco e que no tenham sido usadas no devem retornar ao frasco, salvo instrues em contrrio. Solues diludas de cidos, bases e alguns sais podem ser vertidas na pia sem o risco de contaminao ao ambiente. No entanto se a soluo for de cido ou base concentrado as mesmas devem ser neutralizadas para, ento,
111
serem adicionadas na rede de esgoto. Solues de sais contaminantes (cianetos, cianatos, metais pesados, sais de cromo, etc...) devem ser colocadas em locais adequados e indicados pelo seu professor.
-o-o-o-o-o-o-o-o-o-o-o-o-o-o-o-o-o-o-
112
Experimento 1 - CARACTERSTICAS DAS SOLUES
* MATERIAL (no balco central) - NaCl slido (02 frascos) e esptula de madeira; - CH3COONa.3H2O slido (02 frascos) e esptula de madeira; * MATERIAL POR GRUPO (na bancada) - 4 copos (bequer) de 100 mL sem graduao; - 1 copo (bequer) de 250 mL; - trip para aquecimento; - tela de amianto; - 1 basto de vidro; - 1 proveta de 25 mL; - banho de gelo. - funil comum, com haste curta - suporte para funil * INTRODUO de nosso conhecimento do dia-a-dia que determinados solutos slidos (acar comum, sal de cozinha, etc...) mostram um limite mximo de solubilidade em gua (por exemplo), em dada temperatura. Define-se como Coeficiente de Solubilidade (C.S.) a quantidade mxima de um soluto slido que pode ser dissolvida em determinada quantidade de solvente, em dada temperatura. Em geral usa-se como referncia, em relao ao solvente, 100 gramas (100 mL ou 100 cm3) 250 C (condies padro), isto porque este Coeficiente de Solubilidade varia com o tipo de soluto, quantidade de solvente e temperatura. A tabela a seguir mostra exemplos de dois solutos diferentes em relao a temperatura:
temp.(0C).
m NaCl m KNO3
0 35,7 13,3
10 35,8 20,9
20 36,0 31,6
30 36,3 45,8
50 37,0 85,5
60 37,3 110
80 38,4 169
90 39,0 202
100 39,9 246
Em funo dos dados da tabela acima construa, em papel milimetrado, um grfico de solubilidade para estes dois sais, determinando em qual temperatura a solubilidade (C.S.) dos dois ser a mesma bem como proponha um processo simples de separao destes dois sais.
113
De acordo com o C.S. as solues podem ser divididas nas seguintes categorias: a) insaturadas: so aquelas em que a massa de soluto dissolvida inferior ao coeficiente de solubilidade da substncia; b) saturadas: quando a massa de soluto dissolvida igual ao coeficiente de solubilidade; c) super-saturadas: so solues em que a massa de soluto dissolvida superior ao coeficiente de solubilidade. So preparadas com tcnicas especiais e revelam-se bastante instveis, ou seja, o excesso de soluto pode depositar-se no fundo do recipiente por ao de alguns fatores fsicos (agitao mecnica, atrito, variaes bruscas de temperatura, adio de um germen de cristalizao , etc...) Em nosso experimento sero investigadas algumas propriedades destas solues, particularmente das super-saturadas. * PROCEDIMENTOS Algumas substncias possibilitam a preparao de solues supersaturadas e outras no. Num bequer pequeno (100 mL), usando uma proveta de 25 mL, adicione cerca de 20 mL de gua destilada e, aps, com o auxilio de uma esptula, adicione pequenas quantidades de NaCl slido, at que haja corpo de fundo (depsito). Aquea a mistura, sobre tela de amianto, agitando constantemente, com basto de vidro, at a ebulio. Observando dissoluo do depsito adicione, cuidadosamente, pequenas quantidades de NaCl, at completa dissoluo. Resfrie a soluo em banho de gelo e, se houver algum depsito filtre e recolha o filtrado. Aps resfriada a soluo (se for o caso o filtrado), adicione alguns cristais de NaCl e observe se ocorreu alguma modificao em relao quantidade de sal depositada no fundo recipiente. Repita os mesmos procedimentos utilizando o acetato de sdio tri-hidratado (CH3COONa.3H2O). Devido a alta solubilidade do acetato de sdio adicione quantidades maiores do mesmo, aquecendo sempre que houver depsito no fundo do recipiente. Resfrie em banho de gelo e adicione cristais do acetato, observando se ocorre alguma modificao em relao a estes. Com base nas observaes feitas responda: a) A soluo de NaCl preparada inicialmente super-saturada ? b) Como se denominam os cristais de acetato de sdio adicionados ao final do experimento ?
.o.o.o.o.o.o.o.o.o.o.o.o.o.
114
Experimento 2 - PREPARO E ACONDICIONAMENTO DE SOLUO DE CIDO CLORDRICO
* MATERIAL E REAGENTES (no balco central) - papel de filtro; - cido clordrico concentrado (na capela); - amostras de Na2CO3 (03 por grupo), de 0,300 g contidos em pesafiltros; - indicador (Verde de Bromo-cresol) * MATERIAL POR GRUPO (na bancada) - 01 balo volumtrico de 500 mL; - 01 funil de haste longa; - 01 frasco ambar de 500 mL; - 01 pipeta graduada de 5 mL; - 01 bureta de 50 mL; - 03 erlenmeyer de 250 mL - 01 basto de vidro; - 01 suporte com agarrador para bureta. * INTRODUO Na atividade de laboratrio, seja em nvel acadmico ou na prpria indstria, as substncias so utilizadas, de modo geral, na forma de solues. Numa soluo, alm da proporo entre a quantidade de soluto e de soluo (ou solvente), expressa na forma de uma concentrao , indispensvel que se conheam caractersticas especficas de cada soluto, na preparao adequada dessa soluo. Dependendo da utilizao da soluo as mesmas devem ser consideradas segundo duas caractersticas bsicas: c) solues padro: usadas para fins analticos contendo uma quantidade exatamente conhecida de um reagente qualquer, na unidade de volume. Essa concentrao expressa com exatido (quatro decimais) ex.: 0,1538 g/L (massa/volume) 0,8543 mol/L (nmero de mols/volume)
115
d) solues no padronizadas: usadas para fins no analticos sendo sua concentrao aproximada. No requerida a mesma exatido, com relao s solues padronizadas (um ou dois decimais) ex.: 0,5 g/L (massa/volume) 1,0 mol/L (nmero de mols/volume) *PREPARAO DE SOLUES PADRO O ttulo das solues padro deve ser conhecido com grande exatido. O grau de exatido requerido maior do que o correspondente aos trabalhos analticos mais comuns. Assim sendo desejvel que o ttulo das solues padro possa ser determinado com um erro inferior a 0,1 %. Maiores detalhes sero tratados nas disciplinas de Qumica Analtica Quantitativa. A preparao de uma soluo padro requer, direta ou indiretamente, o uso de um reagente quimicamente puro e com composio perfeitamente definida. Os reagentes com semelhantes caractersticas so denominados, comumente, padres primrios. So os seguintes os requisitos principais exigidos de um padro primrio: f) a substncia deve ser de fcil obteno, purificao, dessecao e conservao; g) no pode ser voltil; h) as impurezas devem ser facilmente identificveis com ensaios qualitativos de sensibilidade conhecida; i) a substncia no deve ser higroscpica (absorver umidade do ambiente) ou eflorescente; j) deve ser bastante solvel. O nmero de padres primrios relativamente limitado. So exemplos: carbonato de clcio, tetraborato de sdio, cido benzico, cloreto de sdio (aps dessecao a peso constante), nitrato de prata, tiocianato de potssio, cido oxlico, oxalato de sdio e dicromato de potssio. Quando o reagente com que se tem de preparar a soluo um padro primrio, recorre-se a tcnica direta que consiste na pesagem, em balana analtica, da massa que se requer da substncia, dissoluo e diluio a um volume conhecido em balo volumtrico aferido. No rtulo dever constar a espcie qumica, seu ttulo, a data de praparao e seu preparador, conforme modelo. *** balo volumtrico s utilizado na preparao e no no armazenamento !!! Embora o Sistema Internacional de unidades recomende para o volume a unidade metro cbico utilizamos o volume expresso em litro (L). As ilustraes a seguir indicam alguns dos equipamentos utilizados na titulaes (bureta, pipeta volumtrica, erlenmeyer,...) a tcnica correta de leitura, de transferncia de alquotas com a pipeta volumtrica e transferncia de soluo para o balo volumtrico.
116
Leitura correta da bureta
Transferncia de soluo
Transferncia de lquido para o balo
Como rotular a soluo !
FACULDADE DE QUMICA PUCRS
HCl M = 0, 2574 mol/ L
Linus Pauling 06/06/1966 Qumica Geral e Inorgnica II
Quando o reagente no padro primrio (por exemplo, o cido clordrico, os hidrxidos alcalinos e de amnio, o permanganato de potssio,...) a preparao direta da soluo no possvel. Recorre-se, ento, tcnica indireta, que consiste em preparar, inicialmente, uma soluo com concentrao aproximada desejada e, depois,
117
padroniz-la, isto , determinar com exatido o sei ttulo em relao a um padro primrio adequado ou com referncia a uma outra soluo padro. Por exemplo, o cido clordrico no padro primrio e a sua soluo pode padronizada atravs de um padro primrio, como o caso do carbonato de sdio. A seguir esta soluo (j padronizada) pode ser usada para titular hidrxidos alcalinos (como por exemplo o hidrxido de sdio). Na padronizao devem ser obedecidas as seguintes condies: d) preciso dispor de um padro primrio adequado ou soluo padronizada; e) o peso do padro primrio no pode ser demasiadamente pequeno, em virtude do erro inerente ao aparelho de pesagem; f) o volume de soluo gasto na padronizao no deve ser pequeno demais, pois cada leitura na bureta est sujeita a um erro de 0,01 mL e um erro de escoamento de 0,02 mL, podendo o erro total chegar a 0,04 mL e, portanto, para garantir uma exatido de 0,1% preciso que o volume de soluo gasto na titulao no seja inferior a 40 mL. *** Obs.: como o objetivo em nossa disciplina no esgotar o assunto e sim mostrar caractersticas principais no prepa ro de solues, eventualmente o critrio acima poder no ser verificado !!! *CONSERVAO DAS SOLUES PADRO Como j afirmamos anteriormente as solues no so conservadas em bales volumtricos (so usados somente na preparao). As solues padro devem ser conservadas de maneira a manter inalterado seu ttulo tanto quanto possvel. Algumas solues so altamente estveis e outras no. Por exemplo, uma soluo 0,1 eqg/L de dicromato de potssio indefinidamente estvel. As solues de cido clordrico, ntrico e hidrxido de amnio, por serem estes solutos volteis, tem durao limitada. As solues de hidrxidos alcalinos reagem com o CO2 presente no ar formando carbonatos. Estes carbonatos solidificam no gargalo dos frascos de depsito e se os mesmos tiverem tampas de vidro esmerilhado, a presena de carbonatos ir emperrar as referidas tampas, sendo aconselhvel o uso de tampas com rolha de borracha ou polietileno ou rosqueadas. Aconselha-se o frasco escuro para evitar a decomposio fotoqumica, o que ocorre com facilidade em solues de perxido de hidrognio e permanganato de potssio.
118
* PROCEDIMENTOS I Preparao de uma soluo cida a partir do cido concentrado. Nosso objetivo, inicialmente, preparar 500 mL de uma soluo de cido clordrico, de concentrao 0,2 mol/L ou 0,2 eqg/L (visto que estas expresses de concentrao se equivalem), a partir do cido concentrado, cujas caractersticas (Ttulo em massa, massa especfica e massa molar) voc dever reconhecer no rtulo do referido cido. Calcule a massa de HCl puro que ser necessria para a preparao da soluo acima e, a seguir, calcule o volume de cido concentrado que contm a massa necessria para o preparo da soluo. Adicione, a seguir, gua destilada ao balo volumtrico at cerca da metade de seu volume. Mea, com pipeta graduada, o volume de cido concentrado que voc calculou e transfira para o balo volumtrico. Agite a soluo e acrescente gua destilada ao balo at cerca de 0,5 cm abaixo da marca de referncia. Com a pipeta graduada (limpa) complete com gua at o trao de referncia, seguindo as tcnicas de leitura. Para homogeneizar a soluo inverta e agite o balo algumas vezes. Para acondicionar a soluo no frasco de depsito, lave o mesmo com gua e detergente, enxaguando-o com gua da torneira e aps com gua destilada. Finalmente, com uma pequena poro (cerca de 5 mL) enxaguar o frasco depsito com a soluo preparada de HCl, ficando o frasco molhado pela prpria soluo. Transfira a soluo preparada do balo para o frasco de depsito. A soluo recm preparada um padro primrio ? Porque ? II Padronizao da soluo de cido clordrico, usando como padro primrio o carbonato de sdio anidro. Nesta 2a parte do experimento nosso objetivo determinar com exatido a concentrao do HCl, usando a reao com um padro primrio, conforme equao a seguir 2 HCl(aq) + Na2CO3(s) 2 NaCl(aq) + H2O(l) + CO2(g)
Ser utilizada uma massa exata deste padro primrio (previamente determinada pelo monitor), a qual voc dever registrar em seus apontamentos para posteriores clculos. Cada grupo dever utilizar, pelo menos, trs amostras de Na2CO3, para efetuar seus ensaios.
119
Inicialmente complete a bureta at o zero, com a soluo preparada de HCl, tomando o cuidado para que no fiquem bolhas de ar entre a torneira e a extremidade inferior da bureta. Transferir cada amostra de Na2CO3 para um erlenmeyer, adicionando gua destilada suficiente para a dissoluo do sal. Aps a dissoluo do carbonato adicione 2 a 3 gotas do indicador. Proceda na adio lenta do cido contido na bureta, at a mudana de colorao do indicador. O manuseio correto da torneira da bureta est indicado na ilustrao ao lado. Quando perceber prxima a mudana de colorao do indicador adicione a soluo cida gota a gota, com constante agitao. Para melhor obervar a mudana de colorao do indicador coloque um papel filtro sobre o suporte da bureta, abaixo de erlenmeyer. O mais indicado um azulejo de cor branca, o qual no fica empreganado de substncias coloridas que mascaram a visualizao do ponto final da reao.
Anote o volume gasto da soluo cida. Complete a bureta com a soluo cida, tome outra amostra de Na2CO3 e repita a titulao, fazendo o mesmo com a ltima amostra. Para cada uma das trs titulaes calcule: a) a massa, em gramas, do HCl necessrio para a reo como carbonato, verificando se esta quantidade est de acordo com a estequiometria prevista; b) conhecida a massa e o volume de HCl necessrio para a neutralizao, determine a concentrao a concentrao em mol/L para a soluo de HCl, rotule a mesma e guarde esta soluo que ser utilizada no prximo experimento.
120
Experimento 3 PREPARAO E ACONDICIONAMENTO DE SOLUES ALCALINAS.
* OBJETIVOS Nosso objetivo, neste experimento, a preparao, padronizao e acondicionamento de uma soluo alcalina, a partir de um reagente slido. Em nosso caso o soluto ser o hidrxido de sdio. Esta soluo, aps a padronizao ser utilizada na titulao de amostras cidas (cido sulfrico e actico vinagre). * MATERIAL E REAGENTES (no balco central) - hidrxido de sdio slido - soluo de cido clordrico 0,2 mol/L - indicador (verde bromo-cresol ou fenolfatelena) * MATERIAL POR GRUPO (bancada) - vidro de relgio - esptula de madeira - bequer pequeno sem graduao (100 mL) - basto de vidro - balo volumtrico de 1000 mL - pipeta graduada de 5 mL - pipeta volumtrica de 25 mL - bureta - suporte a agarrador para bureta - 3 frascos erlenmeyer de 250 mL - frasco mbar para acondicionar a soluo 1000 mL - balana semi-analtica - bequer de 250 mL - funil de haste longa - papel-filtro - etiquetas, cola,...
121
* INTRODUO Os reagentes usados na preparao de solues padro alcalinas so os hidrxidos de sdio, potssio e brio. O mais empregado o de sdio. As solues de bases fortes absorvem CO2 do ar, contaminando-se, por formao de carbonatos. Portanto os frascos de solues destas bases devem permanecer o menor tempo possvel abertos. As solues fortemente alcalinas, quando conservadas em frascos de vidro tambm sofrem contaminao devido formao de silicatos, em ataque ao vidro. recomendvel a conservao em frascos de polietileno. Como j alertamos anteriormente no devem ser usados frascos de vidro com tampa esmerilhada, para evitar a formao de carbonatos slidos, quando a soluo vertida, dificultando e at impossibilitando a abertura do referido frasco. Embora no completamente satisfatrias so usadas rolhas de borracha para vedar estas solues. * PREPARAO DE SOLUES ALCALINAS (NaOH) Tendo em vista que o hidrxido de sdio bastante higroscpico, no se constituindo num padro primrio, sua soluo preparada pelo mtodo indireto e sua concentrao aproximada. Para a determinao exata de sua concentrao necessrio padroniz-la, atravs de um padro primrio ou de uma soluo cida padronizada. Calcule a massa de NaOH necessria para a preparao de 1000 mL (1,0 L) de soluo 0,2 mol/L ou 0,2 eqg/L. Pesar a quantidade acima calculada, sobre um vidro de relgio, em balana semi-analtica. Transfira o soluto para um bequer de 250 mL e adicione gua destilada at a metade do volume, agitando com um basto de vidro at total dissoluo. Com o auxlio de um funil de haste longa transfira a soluo para um balo volumtrico de 1000 mL, de modo que a soluo no entre em contato com a parte superior do gargalo, acima da marca de referncia. Lave o bequer com pequennas pores de gua, reunindo-as no balo. Complete o volume do balo volumtrico com gua destilada at cerca de 0,5 cm abaixo da marca de referncia. A poro restante do volume complete, com cuidado, usando a pipeta graduada de 5 mL, sem ultrapassar a marca do gargalo. Homogeneizar a soluo e acondicion-la em frasco prprio.
122
* PADRONIZAO DA SOLUO ALCALINA As solues alcalinas podem ser padronizadas com solues de cido clordrico de concentrao definida. Em nosso experimento ser utilizada a soluo de HCl j padronizada no experimento anterior ou outra definida pelo professor. Mea 25 mL de soluo de NaOH, com pipeta volumtrica, adicionando em frascos erlenmeyer. Prepare 03 amostras. Adicione 2 a 3 gotas de indicador. Na bureta coloque a soluo de cido clordrico padronizada. Proceda na titulao at mudana de colorao do indicador, ultimando-a gota a gota. Realize a titulao com as trs amostras. Valendo-se da mdia dos volumes gastos determine a concentrao em mol/L ou eqg/L, da soluo alcalina. Guarde a soluo alcalina para experimentos posteriores. -o-o-o-o-o-o-o-o-o-o-o-o-o-o-o-o-o-
123
Experimento 4 PREPARAO E PADRONIZAO DE SOLUO DE CIDO SULFRICO
*MATERIAL E REAGENTES (somente no balco central) - cido sulfrico concentrado (04 frascos) - solues padronizadas de hidrxido de sdio - indicador (Verde de Bromo-cresol ou Fenolftalena) - bales volumtricos de 500 mL (01 por grupo) - pipetas volumtricas de 25 mL (01 por grupo) - 04 pipetas graduadas (para o cido sulfrico) - frascos erlenmeyer de 250 mL (03 por grupo) - buretas de 50 mL (01 por grupo) - suportes com agarrador para buretas - bastes de vidro - funis com haste longa (01 por grupo) - copos de 100 mL sem graduao (02 por grupo) - copos graduados de 250 mL (02 por grupo) - frascos mbar de 500 mL para armazenar a soluo (01 por grupo) - papel-filtro - etiquetas, cola *OBJETIVOS E PROCEDIMENTOS Neste experimento, nosso objetivo preparar e padronizar uma soluo de cido sulfrico de concentrao 0,10 mol/L, que corresponde a 0,2 eqg/L. Valendo-se de procedimentos semelhantes queles adotados na preparao e padronizao da soluo de cido clordrico voc ir fazer o mesmo em relao a soluo de cido sulfrico. A nica diferena prende-se ao fato de utilizar como padro uma soluo de hidrxido de sdio que voc mesmo preparou e padronizou em experimento anterior. Calcule, inicialmente, o volume de cido sulfrico concentrado necessrio para preparar 500 mL de soluo, na concentrao acima referida (vide dados do rtulo do cido sulfrico: Ttulo, massa especfica e massa molar). Dilua adicionando o cido em pequenas pores em gua, contida num bequer, transferindo para o balo volumtrico, com o funil de haste longa. Colha as amostras de NaOH com a pipeta volumtrica, transferindo-as para os frascos erlenmeyer.
124
vidro.
O cido deve ficar na bureta, pois solues alcalinas atacam lentamente o Proceda nas titulaes e apresente os resultados ao final.
-o-o-o-o-o-o-o-o-o-o-o-o-o-o-
125
Experimento 5 DETERMINAO DO TEOR DE CIDO ACTICO (CH3COOH) NO VINAGRE COMERCIAL.
* MATERIAL E REAGENTES (somente no balco central) - vinagre comercial (02 frascos) - solues padronizadas de hidrxido de sdio - indicador (Fenolftalena) - bales volumtricos de 250 mL (01 por grupo) - pipetas volumtricas de 25 mL (01 por grupo) - frascos erlenmeyer de 250 mL (03 por grupo) - buretas de 50 mL (01 por grupo) - suportes para bureta com agarrador - bastes de vidro - copos de 100 mL, sem graduao (02 por grupo) - copos graduados de 250 mL, com graduao (02 por grupo) - papel-filtro - etiquetas, cola. - funil de haste longa * OBJETIVOS E PROCEDIMENTOS Neste experimento nosso objetivo determinar o teor de cido actico (percentual) no vinagre comercial, utilizando para esta titulao a soluo padronizada de hidrxido de sdio. Tendo em vista a concentrao do cido actico no vinagre, teremos que dilu-lo inicialmente. Para tanto voc ir colher com pipeta volumtrica de 25 mL uma alquota de vinagre e dilu-la a 10%, num balo volumtrico de 250 mL, por adio de gua destilada, em quantidade adequada. Aps a homogeneizao da soluo cida voc ir colher 03 amostras de 25 mL, atravs de pipeta volumtrica, transferindo-as para os frascos erlenmeyer. Com a soluo alcalina na bureta (embora este procedimento no seja aconselhvel) proceda na titulao do cido actico. Levando em conta as diluies feitas, calcule o teor de cido actico no vinagre e apresente seus clculos para o professor. Para este clculo percentual
126
considere que a soluo aquosa de vinagre, por ser bastante diluda, tenha massa especfica igual a da gua, ou seja, 1,0 grama/cm3. Aps a realizao do experimento, lave com muita gua a bureta, para no deixar resduos da soluo alcalina na mesma. Lembre-se que a soluo alcalina reage com o gs carbnico do ambiente formando depsito slido de carbonato de sdio, impedindo o movimento da torneira.
-o-o-o-o-o-o-o-o-o-o-o-o-o-o-o-o-o-o-
127
Experimento 6 DETERMINAO DE CALORES DE REAO E LEI DE HESS.
* REAGENTES E SOLUES (balco central) - hidrxido de sdio slido (02 frascos) - esptula de madeira - soluo de cido clordrico 0,50 mol/litro - soluo de cido clordrico 1,00 mol/litro - soluo de hidrxido de sdio 1,00 mol/litro * MATERIAL POR GRUPO (bancada) - 01 frasco erlenmeyer de 250 mL - 01 bequer de 250 mL - 01 basto de vidro - 01 vidro de relgio mdio - etiquetas adesivas (tamanho pequeno) - balana semi-analtica * INTRODUO Neste experimento nosso objetivo determinar a entalpia de algumas reaes (dissoluo com dissociao e neutralizao), aplicando aos resultados obtidos a Lei de Hess. Voc vai usar um frasco erlenmeyer de 250 mL que servir como recipiente para a reao e como calormetro simples para medir o calor envolvido nas reaes. O ideal seria utilizar um frasco de reao isolado termicamente do meio externo (frasco Dewer ou garrafa trmica). No entanto, como a medida ocorre em lapso de tempo curto, pode-se considerar que no ocorrem perdas significativas de calor para o meio externo, podendo, portanto, ser utilizado um frasco aberto e no isolado, como calormetro. O calor envolvido ir modificar a temperatura da soluo e do frasco, considerando que so desprezveis as perdas de calor para o ambiente, como j afirmamos anteriormente. Considere que: - calor especfico da gua (soluo) = 1,0 cal/grama.grau - calor especfico do vidro = 0,2 cal/grama.grau - calor total = calor absorvido pela gua + calor absorvido pelo calormetro (erlenmeyer)
128
Qtotal = mgua.cgua.Dt + merlenmeyer.cvidro.Dt
No h necessidade de determinar a massa de gua se levarmos em conta que sua massa especfica 1,0 grama/mL, sendo pois necessrio determinar apenas o volume, com preciso. A atividade experimental consiste em medir e comparar a quantidade de calor envolvida em trs reaes: Reao 1: hidrxido de sdio slido dissolvendo-se em gua formando soluo aquosa de ons. NaOH(s) + aquoso Na+(aq) + OH-(aq)
DH1 = - x calorias Reao 2: hidrxido de sdio slido reagindo com soluo aquosa de cloreto de hidrognio, formando gua e soluo aquosa de cloreto de sdio. NaOH(s) + H+(aq) + Cl-(aq) H2O(l) + Na+(aq) + Cl-(aq) DH2 = - y calorias Reao 3: soluo aquosa de hidrxido de sdio reagindo com soluo aquosa de cloreto de hidrognio, formando gua e soluo aquosa de cloreto de sdio. Na+(aq) + OH-(aq) + H+(aq) + Cl-(aq) Na+(aq) + Cl-(aq) + H2O(l) DH3 = - z calorias
129
* PROCEDIMENTOS a) Determinao do Calor da Reao 1. Em balana analtica determine a massa de um frasco erlenmeyer de 250 mL, limpo e seco. Coloque no frasco 200 mL de gua destilada. Deixe em repouso por alguns minutos (3 min. ) para que a gua e o frasco entrem em equilbrio trmico com o ambiente. Com um termmetro de preciso determine a temperatura desse sistema. Para evitar erros instrumentais utiliza-se sempre o mesmo termmetro. Num vidro de relgio determine a massa de aproximadamente 4,0 gramas de NaOH, transferindo, a seguir, esta quantidade para a gua contida no erlenmeyer. Coloque o termmetro na gua e agite o frasco at total dissoluo do hidrxido, anotando a temperatura mais extrema alcanada na dissoluo. Lave bem o frasco erlenmeyer antes de passar para a reao 2. b) Determinao do Calor da Reao 2. Repita as operaes iniciais do item (a) anterior, substituindo a gua destilada por 200 mL de soluo de cido clordrico de concentrao 0,50 mol/litro. Lave novamente o frasco erlenmeyer antes de passar etapa seguinte. c) Determinao do Calor da Reao 3. No frasco erlenmeyer de 250 mL, coloque 100 mL de soluo 1,00 mol/litro de HCl e, num bequer de 250 mL, coloque 100 mL de soluo 1,00 mol/litro de NaOH. As duas solues devem estar mesma temperatura antes de mistur-las. Para tanto deixe-as em repouso por alguns minutos em contato com o ambiente para alcanar o equilbrio trmico. Se houver pequena diferena de temperatura entre ambas o professor lhe dar instrues como proceder para alcanar em ambas valor igual de temperatura. Anote a temperatura inicial, reuna as duas solues e anote a temperatura mais extrema. d) Clculos * Em cada uma das reaes calcule: - a variao de temperatura; - a quantidade de calor absorvida pela soluo; - a quantidade de calor absorvida pelo frasco; - a quantidade total de calor absorvida; - o nmero de mols de NaOH usados em cada reao; - a quantidade total de calor por mol de NaOH.
130
* Exprima seus resultados como Calores de Reao: DH1 , DH2 e DH3. * Compare DH2 com (DH1 + DH3) e procure explicar. * Calcule a diferena (desvio) percentual entre DH2 e (DH1 considerando que DH2 esteja correto. + DH3),
* Havendo significativas diferenas entre os valores calculados no item anterior, procure explicar as provveis causas para as mesmas. -o-o-o-o-o-o-o-o-o-o-o-o-o-o-o-
131
Referncias Bibliogrficas
1. Andrade, M. A. G. Prticas de Qumica Geral - Editora Integral, s.d. Porto Alegre. 2. Ramos, M. G. Aulas Experimentais de Laboratrio de Qumica para Engenheiros II Editora Integral, s.d. Porto Alegre. 3. Maynard & Taylor Experiments in General Chemistry - D. Van Nos trand, N. York, 1981, U.S.A. 4. Ohlweiler, O. A. Qumica Analtica Quantitativa Vol. 1, Livros Tcnicos e Cientficos Editora, 1979, S. Paulo, Brasil. 5. C.H.E.M.S. Qumica, uma Cincia Experimental EDART (Vol. 3), So Paulo, Brasil. 6. Semishin, V. Prcticas de Qumica General Editora Muir, 1979, Moscou, U.R.S.S. 7. Cruz, R. Experimentos de Qumica em Microescala - Editora Scipione, 1995, So Paulo, Brasil.
You might also like
- Estudo Dos SDDocument10 pagesEstudo Dos SDDorivaldoNo ratings yet
- Teoria SoluçõesDocument18 pagesTeoria SoluçõesGiorgio AntoniolliNo ratings yet
- Biofísica para ciências biomédicas – 4ª ediçãoFrom EverandBiofísica para ciências biomédicas – 4ª ediçãoNo ratings yet
- Apostila Físico-Química1Document29 pagesApostila Físico-Química1Diego E MarinaNo ratings yet
- Análise de DispersõesDocument17 pagesAnálise de DispersõesMax NunesNo ratings yet
- Biofísica IDocument88 pagesBiofísica Ireginalddvictor.sNo ratings yet
- Soluções Equilíbrio HeterogêneoDocument7 pagesSoluções Equilíbrio HeterogêneoLaura MonteiroNo ratings yet
- Aula 11 - Notas de AulaDocument17 pagesAula 11 - Notas de AulaDanielNo ratings yet
- Apostila 1 de Química X - Prof Zila - UERJ PDFDocument58 pagesApostila 1 de Química X - Prof Zila - UERJ PDFIsabelle ChristineNo ratings yet
- Modelo - Slides - ISPB - 2023 - (1) (1) 1aula # 6 Liquidos e Solucoes 2Document16 pagesModelo - Slides - ISPB - 2023 - (1) (1) 1aula # 6 Liquidos e Solucoes 2Jackson CacondaNo ratings yet
- Soluções e suas propriedadesDocument13 pagesSoluções e suas propriedadesTardio Valter100% (1)
- Equilíbrio Químico SoluçõesDocument57 pagesEquilíbrio Químico SoluçõesAntonio Da Costa FreireNo ratings yet
- Conferencia #7. Disoluciones PTDocument13 pagesConferencia #7. Disoluciones PTFreddy HermesNo ratings yet
- QuimimimimiDocument4 pagesQuimimimimiRudney CarreiraNo ratings yet
- SolubilidadeDocument4 pagesSolubilidadeDmingos JúniorNo ratings yet
- DispersoesDocument31 pagesDispersoesCristiane Da Silva SobrinhoNo ratings yet
- Curso 11186 Aula 11 v1Document29 pagesCurso 11186 Aula 11 v1Moises CorsiNo ratings yet
- Química SoluçõesDocument11 pagesQuímica SoluçõesHellen PatriciaNo ratings yet
- Estudo das dispersõesDocument2 pagesEstudo das dispersõesChristtianne Lima100% (1)
- 03 - SoluçõesDocument5 pages03 - Soluçõescleyton_775918781No ratings yet
- Analítica - Solubilidade e Precipitação 1Document9 pagesAnalítica - Solubilidade e Precipitação 1Rayanne FrotaNo ratings yet
- Soluções químicasDocument18 pagesSoluções químicasRayfson OliveiraNo ratings yet
- Siepe AP Quim 2ano Soluções IDocument2 pagesSiepe AP Quim 2ano Soluções INow UnitedNo ratings yet
- Exp Solubilidade 3Document17 pagesExp Solubilidade 3Lucy FortesNo ratings yet
- Propriedades Coligativas SoluçõesDocument25 pagesPropriedades Coligativas SoluçõesAline Viaro50% (2)
- Soluções e suas propriedadesDocument8 pagesSoluções e suas propriedadesmonlysNo ratings yet
- Por Que Todos Os Nitratos São SolúveisDocument7 pagesPor Que Todos Os Nitratos São SolúveistinamarquesNo ratings yet
- Estudo de Solubilidade de Sais em ÁguaDocument8 pagesEstudo de Solubilidade de Sais em ÁguaPaulo Alexandre ZunguzeNo ratings yet
- Relatorio 3 OrganicaDocument19 pagesRelatorio 3 OrganicaLucimara MagalhaesNo ratings yet
- DISPERSOES Prof. CleberDocument62 pagesDISPERSOES Prof. CleberceliogardeonNo ratings yet
- Solubilidade Dos Compostos Orgânicos.Document15 pagesSolubilidade Dos Compostos Orgânicos.Carol RobainaNo ratings yet
- Quimica 18Document29 pagesQuimica 18ascatanho100% (1)
- Misturas e Soluções-Texto ComplementarDocument6 pagesMisturas e Soluções-Texto ComplementarcaoNo ratings yet
- AULA VI SOLUCOESDocument18 pagesAULA VI SOLUCOESCharlene MaboteNo ratings yet
- Solubilidade e TemperaturaDocument7 pagesSolubilidade e TemperaturaDiego E. MaylaNo ratings yet
- SOLUÇÕESDocument98 pagesSOLUÇÕESSidney JesusNo ratings yet
- Propriedades Coligativas Das SolucoesDocument2 pagesPropriedades Coligativas Das SolucoesAvelino Vagner Da SilvaNo ratings yet
- Soluções (Slide)Document58 pagesSoluções (Slide)Felipe QueirozNo ratings yet
- Estudo Dos Sistemas DispersosDocument7 pagesEstudo Dos Sistemas DispersosnailtonandradesousaNo ratings yet
- Jy 6 Ynjj 7 Uuuyhhy 66666Document23 pagesJy 6 Ynjj 7 Uuuyhhy 66666hicaroribeiro.gamesNo ratings yet
- Resumo Sobre SoluçõesDocument19 pagesResumo Sobre SoluçõesFabíola FelixNo ratings yet
- Soluções Químicas: Conceitos e CálculosDocument11 pagesSoluções Químicas: Conceitos e CálculosJohn RodriguesNo ratings yet
- Soluções 2018 V01Document102 pagesSoluções 2018 V01RomeuComastriAbdalaNo ratings yet
- Aula 02 - 2ºano - SOLUÇÕES - 01 - 2023Document34 pagesAula 02 - 2ºano - SOLUÇÕES - 01 - 2023Ágata LohanaNo ratings yet
- 11 - Química Geral - SoluçõesDocument46 pages11 - Química Geral - SoluçõesSousa RodriguesNo ratings yet
- Química experimental IIDocument44 pagesQuímica experimental IIBeatriz Carvalho RodriguesNo ratings yet
- Soluções - Parte 1 - Classificação de SoluçõesDocument2 pagesSoluções - Parte 1 - Classificação de SoluçõesLyeniferNo ratings yet
- Estudo SoluçõesDocument24 pagesEstudo Soluçõesneyzanata5043No ratings yet
- SoluçõesDocument5 pagesSoluçõesarturzau20No ratings yet
- Fundamentos dos fluidos de perfuração: classificação e conceitos-chave de sistemas dispersosDocument122 pagesFundamentos dos fluidos de perfuração: classificação e conceitos-chave de sistemas dispersosValécia Dantas100% (2)
- Soluções e concentraçãoDocument31 pagesSoluções e concentraçãosardinha2No ratings yet
- Relatório 1 - Solubilidade de Compostos OrgânicosDocument13 pagesRelatório 1 - Solubilidade de Compostos Orgânicosaldorenan94% (17)
- Texto Atividade5Document18 pagesTexto Atividade5Chadrekzy January PungosNo ratings yet
- Memorial cálculo instalações GLPDocument9 pagesMemorial cálculo instalações GLPBartolomeu Muniz GranjaNo ratings yet
- Tabela de Propriedades Térmicas de Materiais de ConstruçãoDocument6 pagesTabela de Propriedades Térmicas de Materiais de ConstruçãoBruno de RossoNo ratings yet
- Catalogo Elos Fusa VeisDocument28 pagesCatalogo Elos Fusa VeisGlauco Vitiello FabianoNo ratings yet
- NBR 7347 (Abr 1982) - Limpeza de Superfícies de Aço Com Ferramentas MecânicasDocument2 pagesNBR 7347 (Abr 1982) - Limpeza de Superfícies de Aço Com Ferramentas MecânicasYuri Bahia de VasconcelosNo ratings yet
- Nióbio: Propriedades e AplicaçõesDocument10 pagesNióbio: Propriedades e AplicaçõesfocaultNo ratings yet
- ProvaDocument3 pagesProvaElves SilvaNo ratings yet
- Revisão, Hdrocarbonetos, Derivados HalogenadosDocument62 pagesRevisão, Hdrocarbonetos, Derivados HalogenadosLeyde PederNo ratings yet
- Refrigerant NameDocument2 pagesRefrigerant NameErdinc KlimaNo ratings yet
- Coral Esmalte Sintetico Alto Brilho LaranjaDocument9 pagesCoral Esmalte Sintetico Alto Brilho Laranjagean1407No ratings yet
- Apostila Fisico-Quimica - FarmáciaDocument20 pagesApostila Fisico-Quimica - FarmáciaPaula KnupferNo ratings yet
- Q10 Preparacao de Solucoes A Partir de Soluto SolidoDocument10 pagesQ10 Preparacao de Solucoes A Partir de Soluto SolidoCatiões Partilha com EnergiaNo ratings yet
- Ligação CovalenteDocument35 pagesLigação CovalenteDangley CoserNo ratings yet
- Catalogo-Tecnico - FacilitDocument34 pagesCatalogo-Tecnico - FacilitRafael CardosoNo ratings yet
- Processo de tratamento de água da ETA ComusaDocument9 pagesProcesso de tratamento de água da ETA ComusaDani LombaNo ratings yet
- Prática de EnzimasDocument5 pagesPrática de EnzimasAldayr Melo100% (1)
- Tabela Torque ParafusosDocument15 pagesTabela Torque ParafusosHELIO SANTOS JUNIOR100% (4)
- Tabela Dos IonsDocument1 pageTabela Dos IonsMatheus AlvesNo ratings yet
- Atividade Domiciliar 6º Ano - CiênciasDocument5 pagesAtividade Domiciliar 6º Ano - CiênciasAnderson Carlos100% (1)
- Aplicação Da Técnica de Voltametria CíclicaDocument5 pagesAplicação Da Técnica de Voltametria CíclicaS_avyoNo ratings yet
- E-Book Peeling de Vitamina C-5Document13 pagesE-Book Peeling de Vitamina C-5Fernanda CostaNo ratings yet
- Especificação Técnica Aço AISI P20Document1 pageEspecificação Técnica Aço AISI P20Rafael SalvagniNo ratings yet
- Quimica 2015Document3 pagesQuimica 2015Andrey CabralNo ratings yet
- Ensaio de precipitação e solubilidadeDocument3 pagesEnsaio de precipitação e solubilidadeGeovane SouzaNo ratings yet
- Processo Haber-Bosch sintetiza amoníacoDocument2 pagesProcesso Haber-Bosch sintetiza amoníacoMaykkkowNo ratings yet
- UFCD 6710 - Ficha de Trabalho 1Document4 pagesUFCD 6710 - Ficha de Trabalho 1Cristina LopesNo ratings yet
- Tabela de condutividade térmica de materiais de construçãoDocument3 pagesTabela de condutividade térmica de materiais de construçãoLuNo ratings yet
- Reações do Al e ClAlDocument4 pagesReações do Al e ClAlVINICIUSferreira100% (1)
- 2 Lista de ExercíciosDocument3 pages2 Lista de ExercíciosWagner DieringsNo ratings yet
- Ácidos Carboxílicos e AnidridosDocument16 pagesÁcidos Carboxílicos e AnidridosKevin GomesNo ratings yet
- Agentes químicos e exposições ocupacionaisDocument6 pagesAgentes químicos e exposições ocupacionaisBarbara GeraldinoNo ratings yet