Professional Documents
Culture Documents
Sintesis de para Nitroanilina
Uploaded by
kory_scOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Sintesis de para Nitroanilina
Uploaded by
kory_scCopyright:
Available Formats
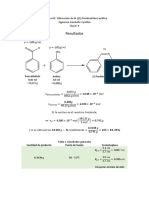
Castillo G. German y Prez S. Cristian A.
Mecanismo de nitracin para la obtencin de metaSNTESIS DE PARA- NITROANILINA
nitroanilina.
Se realiz la sntesis de para-nitroanilina. El proceso que se llev acabo consta de tres pasos, en el primer paso a
partir de 3 g de Acetanilina mediante una reaccin de Sustitucin Electroflica Aromtica se obtuvo paranitroacetanilida, el electrfilo involucrado en dicha reaccin fue el ion nitronio el cual se form mediante una
mezcla de 3 mL de cido sulfrico y 3 mL de cido ntrico. Posteriormente se realiz la hidrolisis del compuesto
obtenido adicionando 15 mL de agua y 15 mL de cido clorhdrico concentrado en un sistema a reflujo durante
30 minutos, por ltimo se agreg 16 mL de una solucin de hidrxido de sodio al 40% hasta alcanzar un pH 10,
con esto finalizo el proceso y se obtuvo el producto deseado, para-nitroanilina. Finalmente se determin el punto
de fusin para su identificacin y se realiz el clculo de rendimiento.
INTRODUCCIN
Realizar la sntesis de para-nitroanilina involucra la
nitracin de un compuesto aromtico sustituido, esta
reaccin es una Sustitucin Electroflica Aromtica, la
reaccin global es la sustitucin de un protn (H +) por
un ion nitronio en el anillo aromtico. La formacin del
ion nitronio el cual es el electrfilo en cuestin se
obtiene mediante la mezcla de cido sulfrico y cido
ntrico, siguiendo el siguiente mecanismo. [1]
El mecanismo inicia con la desprotonacin de un
hidrogeno del cido sulfrico con pKa -5.2 aceptado por
un tomo de oxigeno del cido ntrico con pKa -1.44 el
cual acta como base [1] as en el intermediario [2] el
tomo de oxgeno con carga (+) por efecto de
resonancia puede desprenderse en forma de agua y de
esta manera se obtiene la formacin de ion nitronio [3].
Considerando la estructura del producto deseado
(Figura 1), es fcil suponer que el compuesto aromtico
a nitrar fuera la anilina (Figura 2)
Sin embargo la anilina en presencia de cido sulfrico
se protona [1] y en el intermediario [2] el nitrgeno con
carga (+) es un centro atrayente de densidad
electrnica, de manera que desactiva el ciclo
aromtico y con ello la sustitucin en posiciones ortopara, as el ataque electroflico del ion nitronio se
orienta a una posicin meta [3] formando el complejo
sigma [4], el agua acta como base y sustrae el
hidrogeno unido al carbono con hibridacin Sp3 as los
electrones pi estabilizan al carbocatin adyacente [5]
finalmente la desprotonacin de un hidrogeno unido al
tomo de nitrgeno estabiliza el anillo y regenera la
aromaticidad obteniendo
meta- nitroanilina [6].
De acuerdo a lo anterior fue mejor partir de una anilida
ya que no generara un centro atrayente de densidad
electrnica al reaccionar con el cido sulfrico, se
utiliz Acetanilina un compuesto activador, orientador
orto-para.
Discusin de resultados
Se verti 3g de Acetanilina y 7 mL de cido sulfrico en
un matraz baln hasta la disolucin completa, en esta
operacin ocurre un intercambio de protones entre las
especies participantes. Por otra parte se prepar en un
embudo de separacin una mezcla de 3 mL de cido
ntrico y 3 mL de cido sulfrico, as se form el ion
nitronio descrito con anterioridad.
Castillo G. German y Prez S. Cristian A.
Una vez realizados los pasos anteriores se coloc la
Acetanilina disuelta en un bao de hielo y se verti
gota a gota la mezcla de cido ntrico y cido sulfrico.
Mecanismo de hidrolisis de la para-nitroacetanilida
Mecanismo de nitracin para la obtencin de paranitroacetanilida
La adiccin de la mezcla de cidos a la acetanilida [1]
se realiz con cautela ya que al adicionar rpidamente
se tendra la formacin de productos de oxidacin no
deseados,
y
verificando
constantemente
la
temperatura, debido a que la reaccin es sumamente
exotrmica. Dicha mezcla de cidos forma el ion
nitronio el cual realiza un ataque electroflico [2] con
orientacin orto- para, la sustitucin en dichas
posiciones se debe a que en el complejo sigma el
carbocatin estabilizado por resonancia se encuentra
adyacente al tomo de nitrgeno el cual tiene un par
de electrones de no enlace que dona al carbocatin
mediante un enlace pi [3] formando un intermediario
muy estable. Sin embargo la sustitucin en posicin
orto est impedida fsicamente debido al factor
estrico del grupo acetilo. El ltimo paso de la reaccin
es la prdida del protn unido al carbono tetradrico
[4] debido a que el agua acta como base y lo sustrae,
as se obtiene para-nitroacetanilida la cual es poco
soluble en agua [5]. Despus de la nitracin se dio el
tiempo necesario para que la para-nitroacetanilida
precipitara y se filtr al vaco con 2 porciones de 50 mL
de agua fra ya que la base conjugada del cido
sulfrico y el ion hidronio son solubles en agua.
En este punto se obtuvo para-nitroacetanilida, el
siguiente paso del proceso fue eliminar el grupo acetilo
de la estructura efectuando una hidrolisis acida. Se
agreg la para- nitroacetanilida en 15 mL de agua
hasta tener una pasta fina en un matraz,
posteriormente se adiciono lentamente 15 mL de cido
clorhdrico y se calent a reflujo durante 30 minutos.
El mecanismo inicia con la protonacin [1] del oxgeno
del carbonilo de la para-nitroacetanilida para formar el
intermediario que por efecto de resonancia genera un
carbocatin y este recibe un ataque nucleoflico por
una molcula de agua [2] este otro intermediario
pierde un protn y el oxgeno con carga positiva
adquiere carga neutra [3], despus los electrones de
no enlace del tomo de nitrgeno aceptan un protn
presente en el medio [4] y esto origina mediante un
movimiento de electrones la perdida de una molcula
de cido actico protonada [5] y se obtiene paranitroanilina que se protona [6] para dar clorhidrato de
para-nitroanilonio mas cido actico [7].
Finalmente se realiz una reaccin acido-base con la
adicin de 16 mL de una solucin de hidrxido de sodio
al 40% para alcalinizar hasta un pH 10 y transformar la
sal obtenida del proceso anterior en el producto
deseado.
Mecanismo de reaccin cido- base.
Despus de la hidrolisis al adicionar hidrxido de sodio
esta base sustrae un protn de la sal de clorhidrato de
para-nitroanilonio [1] formando agua, el cido actico
es desprotonado por la molcula de agua y mediante
fuerzas electroestticas atrae al ion de sodio libre en el
medio [2] as se genera el ion nitronio el cual sigue
siendo una especie acida [3] que se desprotona
fcilmente en presencia de hidrxido de sodio [4],
finalmente se obtiene como productos
para-
Castillo G. German y Prez S. Cristian A.
nitroanilina, acetato de sodio y cloruro de sodio
disuelto en agua[5].
La para- nitroanilina tiene una solubilidad en agua de
0.08 g/100 mL, por otra parte el acetato de sodio es
muy soluble en agua, de esta manera basto con
realizar una filtracin al vaco para obtener el producto
deseado. Se obtuvo como producto 2.2 g de un polvo
amarillo y se determin un punto de fusin del mismo,
el cual fue de 147-148 C, este concuerda con el
reportado en la literatura de 147.5C, as se confirm la
sntesis de para-nitroanilina con un rendimiento de
73.3% debido a que en la nitracin de acetanilida se
generan productos de oxidacin.
CONCLUSIONES
En la sntesis de para-nitroanilina llevada a cabo el
grupo acetilo presente en la acetanilida ofrece una
proteccin al anillo aromtico evitando la formacin de
un centro deficiente de densidad electrnica que
desactive al ciclo, la acetanilida es un activador de la
posicin orto-para, pero debido al efecto estrico
proporcionado por el grupo acetilo la sustitucin de un
protn por un ion nitronio en el anillo aromtico se
orienta preferentemente en posicin para.
Se
confirm
la
sntesis
de
para-nitroanilina
determinando el punto de fusin del producto obtenido
el cual fue de 147-148C.
BIBLIOGRAFA
[1] L. G. Wade. Qumica Orgnica Volumen 1. Pearson Educacin,
Mxico 2011
pp751-772
You might also like
- 2,4 Dinitrofenilhidrazina y 2,4 DinitrofenilanilinaDocument5 pages2,4 Dinitrofenilhidrazina y 2,4 Dinitrofenilanilinacharly_sixtie100% (1)
- Estampado Textil PDFDocument266 pagesEstampado Textil PDFMichael Chamorro100% (2)
- Síntesis de para NitroanilinaDocument2 pagesSíntesis de para NitroanilinaCristobal Cruz Cabrera100% (1)
- Síntesis de Alcohol Bencilico y Ácido BenzoicoDocument35 pagesSíntesis de Alcohol Bencilico y Ácido BenzoicoGabrielVazquezOlvera100% (2)
- Práctica 5 Nitración Del Benzoato de MetiloDocument3 pagesPráctica 5 Nitración Del Benzoato de MetiloErik Melo0% (1)
- Práctica 2 Sintesis de BenzalacetofenonaDocument2 pagesPráctica 2 Sintesis de BenzalacetofenonaJason Téllez AndradeNo ratings yet
- Practica 7 Org4Document5 pagesPractica 7 Org4almuchis12No ratings yet
- Practica 4 Condensación de Claisen-Schmidt. Obtencion de DibenzalacetonaDocument18 pagesPractica 4 Condensación de Claisen-Schmidt. Obtencion de DibenzalacetonaLizeth Paola TellezNo ratings yet
- Obtención de Anaranjado de MetiloDocument5 pagesObtención de Anaranjado de MetiloLuis Valente RamírezNo ratings yet
- Práctica 9 - BenciloDocument4 pagesPráctica 9 - BenciloBrigitteMoran0% (1)
- Sintesis de M NitroanilinaDocument14 pagesSintesis de M NitroanilinaMaria Mathews100% (2)
- Síntesis de 2 4-Dietoxicarbonil-3, 5-DimetilpirrolDocument6 pagesSíntesis de 2 4-Dietoxicarbonil-3, 5-Dimetilpirrolleonardo porras narvaezNo ratings yet
- Síntesis de ácido bencílico a partir de benzaldehídoDocument5 pagesSíntesis de ácido bencílico a partir de benzaldehídoZoledad Tavera100% (1)
- Marco Teórico EnzimasDocument3 pagesMarco Teórico EnzimasAnonymous 8Q0fcdq100% (1)
- Diagrama de Bloques de Procesos PetroquimicosDocument11 pagesDiagrama de Bloques de Procesos PetroquimicosRafael RamirezNo ratings yet
- BENCILO PrevioDocument5 pagesBENCILO PrevioDaniel Bautista100% (1)
- Practica 1 Sintesis ParanitroanilinaDocument5 pagesPractica 1 Sintesis ParanitroanilinaRocio100% (1)
- Síntesis de 2,3-difenilquinoxalinaDocument10 pagesSíntesis de 2,3-difenilquinoxalinaAndy AldamaNo ratings yet
- Reporte Ácido FenoxiáceticoDocument3 pagesReporte Ácido FenoxiáceticotertbutilNo ratings yet
- Síntesis de epóxido de menadiona y apertura a ftiocolDocument2 pagesSíntesis de epóxido de menadiona y apertura a ftiocolFrancisco QuirozNo ratings yet
- Síntesis dibenzalacetonaDocument5 pagesSíntesis dibenzalacetonaLuis RomeroNo ratings yet
- Investigacion Previa BenciloDocument2 pagesInvestigacion Previa BenciloEve TenorioNo ratings yet
- Previo para P-NitroanilinaDocument10 pagesPrevio para P-NitroanilinaCarlos CastilloNo ratings yet
- Práctica 2 - Obtención de Furfural y Reacción de CannizzaroDocument7 pagesPráctica 2 - Obtención de Furfural y Reacción de CannizzaroJose Manuel OrtizNo ratings yet
- Reacción de Claisen SchmidtDocument3 pagesReacción de Claisen SchmidtKimberly TorresNo ratings yet
- Síntesis de Colorantes Azoicos: Orange II, Sudan I, Rojo paraDocument2 pagesSíntesis de Colorantes Azoicos: Orange II, Sudan I, Rojo paraparis100% (2)
- Prev 6Document6 pagesPrev 6Gabriela HernandezNo ratings yet
- Cuestionario Previo 16 BenciloDocument5 pagesCuestionario Previo 16 BenciloDavid AquinoNo ratings yet
- Practica 7 NitroanilinaDocument4 pagesPractica 7 NitroanilinaRomano100% (1)
- Ácido PícricoDocument2 pagesÁcido PícricoViiry Salazar75% (4)
- Reporte FurfuralDocument9 pagesReporte FurfuralMary FallNo ratings yet
- PRÁCTICA No. 4: OBTENCIÓN DE 5,5-DIFENILHIDANTOINADocument7 pagesPRÁCTICA No. 4: OBTENCIÓN DE 5,5-DIFENILHIDANTOINADiana HMNo ratings yet
- Acido Fenoxiacetico Previo y ReporteDocument5 pagesAcido Fenoxiacetico Previo y Reportebrayan gutierrezNo ratings yet
- Dibenzalacetona PracticaDocument4 pagesDibenzalacetona PracticaBrayan Efrain Orozco SoteloNo ratings yet
- Previo 5 Q.O IIIDocument2 pagesPrevio 5 Q.O IIIMichell Maximiliano Santillan HerrejonNo ratings yet
- Practica Furfural FinalDocument5 pagesPractica Furfural Finalfcbarcelona-08hotmail.comNo ratings yet
- Previo BenciloDocument6 pagesPrevio BenciloHeber Daniel Andrade Rivera100% (1)
- Previo 6 Sintesis de Hantzsch para PiridinasDocument3 pagesPrevio 6 Sintesis de Hantzsch para PiridinasJulio Cesar Venegas Muñoz50% (2)
- Practica 9: Preparación de BencimidazolDocument4 pagesPractica 9: Preparación de BencimidazolGuillermo CasillasNo ratings yet
- p1 Obtencion Del Epoxido de MenadionaDocument6 pagesp1 Obtencion Del Epoxido de MenadionadanielNo ratings yet
- Obtencion de FurfuralDocument3 pagesObtencion de FurfuralAdrian PINo ratings yet
- Previo Condensación AldolicaDocument7 pagesPrevio Condensación AldolicaRodrigo Colin100% (1)
- Previo HidantoínasDocument9 pagesPrevio HidantoínasUriel RamosNo ratings yet
- Reporte 9Document9 pagesReporte 9ivanovich hernandezNo ratings yet
- BenzoínaDocument13 pagesBenzoínadany_289No ratings yet
- Practica 12 y Ensayos para Proteinas y AminoacidosDocument2 pagesPractica 12 y Ensayos para Proteinas y AminoacidosElCaballero Modesto0% (1)
- Preparación Del Sistema Indol. Síntesis de 2 Fenilindol 1Document2 pagesPreparación Del Sistema Indol. Síntesis de 2 Fenilindol 1Evelyn Jim 3295No ratings yet
- Practica 4 Sintesis de 1-Fenil-3metilpirazol-5-OnaDocument2 pagesPractica 4 Sintesis de 1-Fenil-3metilpirazol-5-OnaJackCrack1221No ratings yet
- DIBENZALACETONADocument7 pagesDIBENZALACETONACrash TinocoNo ratings yet
- Reporte P-Nitroanilina 1.1Document12 pagesReporte P-Nitroanilina 1.1Jesus Belmont VazquezNo ratings yet
- Síntesis de 2,4-Dietoxicarbonil 3,5 DimetilpirrolDocument25 pagesSíntesis de 2,4-Dietoxicarbonil 3,5 DimetilpirrolEdgar ArmandoNo ratings yet
- Obtencion de N - Z - Fenilmetilen AnilinaDocument5 pagesObtencion de N - Z - Fenilmetilen AnilinaJuanDavidPBNo ratings yet
- AzocompuestosDocument11 pagesAzocompuestosIsabel Centeno100% (1)
- Síntesis de CannizzaroDocument8 pagesSíntesis de CannizzaroAbraham MartinezNo ratings yet
- Azocompuestos Anaranjado de MetiloDocument8 pagesAzocompuestos Anaranjado de MetiloChristian MontielNo ratings yet
- Reporte Practica 3 Furfural. .Document2 pagesReporte Practica 3 Furfural. .marbellapedroza100% (1)
- Reporte Sintesis de Cumarina 2Document4 pagesReporte Sintesis de Cumarina 2Ana Luz Tovar Lopez0% (1)
- Reporte 5 PirazolonasDocument4 pagesReporte 5 PirazolonasAnonymous enA4SSNo ratings yet
- 1 Fenil 3 Metil 5 PirazolonaDocument6 pages1 Fenil 3 Metil 5 PirazolonaSaraLHerreraNo ratings yet
- Síntesis p-nitroanilinaDocument5 pagesSíntesis p-nitroanilinaCésar Mendiola San Róman0% (1)
- Práctica 9Document3 pagesPráctica 9Vane Trejo0% (1)
- SÍNTESIS DE Para-NitroanilinaDocument9 pagesSÍNTESIS DE Para-NitroanilinaTowerNo ratings yet
- AnilinaDocument10 pagesAnilinahairmonNo ratings yet
- Síntesis de ParanitroanilinaDocument1 pageSíntesis de Paranitroanilinakory_scNo ratings yet
- Sintesis de para NitroanilinaDocument3 pagesSintesis de para Nitroanilinakory_sc100% (5)
- Práctica CarbohidratosDocument4 pagesPráctica Carbohidratoskory_scNo ratings yet
- Práctica CarbohidratosDocument4 pagesPráctica Carbohidratoskory_scNo ratings yet
- Hidrolisis de Una Proteína y Ensayos para Proteínas y AminoácidosDocument3 pagesHidrolisis de Una Proteína y Ensayos para Proteínas y Aminoácidoskory_sc82% (11)
- c3 Agua QMC 1104Document2 pagesc3 Agua QMC 1104sergio sarzuri mamaniNo ratings yet
- BERROCAL FLORES, Lizet Paola y BOZA ESTEBAN, Kathlin (I.Q)Document22 pagesBERROCAL FLORES, Lizet Paola y BOZA ESTEBAN, Kathlin (I.Q)Katerin Boz EstebanNo ratings yet
- Iram-Ias U 500-42Document13 pagesIram-Ias U 500-42Andres Nicolas BouvierNo ratings yet
- Relacion Problemas Tema 7Document6 pagesRelacion Problemas Tema 7zafiro TorresNo ratings yet
- Act. 1 Cuadro Comparativo PlásticosDocument11 pagesAct. 1 Cuadro Comparativo PlásticosChanolol FerrariNo ratings yet
- Solubilidad y preparación de soluciones 0.1 MDocument14 pagesSolubilidad y preparación de soluciones 0.1 MPABLO ANDRES YUJRA SARAVIANo ratings yet
- Practica 3 de OrganicaDocument9 pagesPractica 3 de OrganicaEver LuisNo ratings yet
- Nomenclatura InorgánicaDocument36 pagesNomenclatura InorgánicaRosita PerezNo ratings yet
- Oxoacidos - Formulacion y NomenclaturaDocument2 pagesOxoacidos - Formulacion y Nomenclaturamarina morales100% (1)
- Monografia de QuimicaDocument69 pagesMonografia de QuimicaEdwin Ruben Caceres Caquiamarca100% (1)
- 02 - QuimicaDocument8 pages02 - QuimicaLevis Pomalaza MarceloNo ratings yet
- Taller SolucionesDocument4 pagesTaller SolucionesPaola gutierrez gilNo ratings yet
- Grupo 1-Informe de Lluvia Ácida en El SueloDocument35 pagesGrupo 1-Informe de Lluvia Ácida en El SueloFERRER WALDE ANGEL ALEXANDERNo ratings yet
- Nomenclatura y Reactividad de Derivados de Ac - CarboxílicosDocument3 pagesNomenclatura y Reactividad de Derivados de Ac - CarboxílicosPilar MonsalvoNo ratings yet
- Rubigen: desinfectante orgánico de origen cítricoDocument2 pagesRubigen: desinfectante orgánico de origen cítriconeronciNo ratings yet
- Presentacion Tierras Raras AyDocument31 pagesPresentacion Tierras Raras AySelenio simoms100% (1)
- Deber 1Document11 pagesDeber 1Alex ReaNo ratings yet
- Alcoholes y FenolesDocument10 pagesAlcoholes y FenolesCAROLNo ratings yet
- Mapa Conceptual-BiologiaDocument1 pageMapa Conceptual-Biologializ alvaradoNo ratings yet
- Solución Práctica Derivados HidrocarburosDocument48 pagesSolución Práctica Derivados HidrocarburoshecfermeNo ratings yet
- Parcial 2 BioquimicaDocument30 pagesParcial 2 BioquimicaJoya NohraNo ratings yet
- Funciones Químicas y NomenclaturaDocument13 pagesFunciones Químicas y NomenclaturaJairo RodriguezNo ratings yet
- Tincion Diferecial Acido ResistenteDocument45 pagesTincion Diferecial Acido ResistenteTania Angelica Cencara RojasNo ratings yet
- Recurtido y NeutralizadoDocument15 pagesRecurtido y NeutralizadoMarco Antonio Paco ArcaniNo ratings yet
- Reactividad Organica, Isomería, PetróleoDocument7 pagesReactividad Organica, Isomería, PetróleoBeatriz Arancibia CifuentesNo ratings yet
- Reducciones Sintéticas MetDocument16 pagesReducciones Sintéticas MetJorge Alberto Estrada TorresNo ratings yet
- SOLUCIONARIO TALLER 2 GasesDocument4 pagesSOLUCIONARIO TALLER 2 GasesMelani SuárezNo ratings yet